主族元素光控配位數:偶氮苯對主族元素取代基性質的影響和它們的應用
- 2012-08-13
- 專題
1、引述
每個主族元素在主族化合物通常都有它自己的特定的配位數、氧化數和粘結狀態。異常的化合價可以通過合適的分子設計和合成方法實現,并且像這樣有異常化合價的元素具有獨特的特征、特殊的結構和性質。化合物的主要基團的反應能力明顯依賴于它們的配位數。例如,硅是14號元素,在周期表中位于碳元素的下方,通常它的配位數像sp3雜化的碳為4。硅也可以處于高配位數狀態,例如在合適的條件下,硅在合適的配體中配位數為5或6。在高配位數的硅分子中,處于分子中心的硅原子具有比4配位數硅強的親電性,并且與硅原子相連的基團的親核性也隨之增強(圖1)。因此,一些合成方法已經被開發通過利用高配位數的硅的性質,作為他們的中間體或過度狀態,正如已被證實的Tamao氧化反應中表現的性質。1)另外其他例子如有機磷分子中的中心原子P顯三價,它的配位數也為3,在過渡金屬中已廣泛應用于配體。當磷顯示五價并且四面體型配位或者顯示五價且配位數為5,磷的有效性將大大減少。
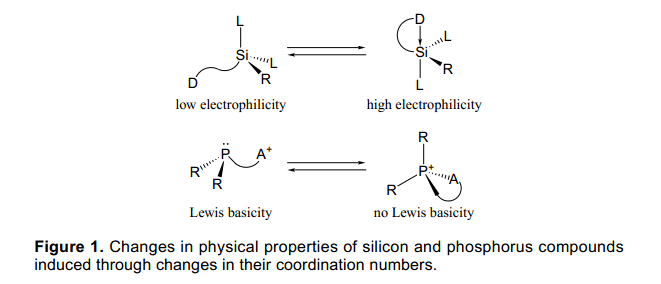
考慮到元素的性質與配位數的關系、氧化態的控制、主族元素的配位數,使用外部刺激很有意義。這將會產生新的方法通過控制物理性質和分子中主要基團性質來控制有機反應。例如,如果配位狀態很容易被改變,可以讓一個元素在特定階段表現一種處于激活狀態的配位數,而在另一階段則表現為非激活狀態,這將對共聚反應規則非常有用。此外,如果這可以作為原料,它也可以作為一種新的保護方法或脫保護的配體。
然而,主族元素處于非常態的配位狀態通常是不穩定的,而在實際應用中有時是需要穩定的狀態。例如,空間位阻常被用來來保護低配位數主族元素分子,通過在主族元素上引入體積較大的基團以防止化合物的聚合。此外,處于高配位數狀態的元素被認為容易發生消去反應,因為它們在有機反應中常是反應過程中的中間體。因此,需要引入吸電子基團來減弱中心原子的電子密度,并且增強極性鍵的穩定性,多齒狀的配體應該被用于有利的熵。在主族元素分子的非常態配位狀態下,分子穩定性的設計中有許多限制因素。為了可逆的控制配位數,控制中心原子與配體之間的關系顯得很重要。為了達到和這個目的,作為配體的取代基必須有這些滿足這些要求和可控性。因為這些可控性,不可能預先在主要組成化合物上開發出特殊基團來滿足接下來的兩點要求:1)穩定的異常配位狀態;2)結構控制可以由外部因素激活。
一個可控的方法是通過外部因素激活:光照。已有幾種分子被證明他們的結構隨著光照而改變。在它們當中,偶氮苯作為光敏分子已被廣泛報道可以在各種類型的光照反應中被光異性化。2)我們已經將注意力定向在偶氮苯的這個性質上,也就是,偶氮苯的一種結構具備一定的剛度并能感光異構,以及偶氮基團可以起到路易斯堿或利用試劑作為親電體。我們希望當偶氮苯作為分子內配體時,可以在(E)—和(Z)—之間可逆的光異構化來控制主族元素的配位數。首先,我們在偶氮苯的2號位引入一個主族元素基團,因此,我們可以利用偶氮基團作為光敏點、配位點或親電點。我們實驗的結果是主族元素的碳、硅、磷的配位數在光照條件下可以控制,并且他們的結構、物理性質和反應活性在幾種體系中均可很好的光控。在這篇論文中,我們主要關注這幾種方法的發展、介紹幾種控制主族元素配位數的控制方法以及他們的應用,我們也討論了偶氮苯自身作為取代基的性質。
2.硅烷和硅酸鹽的光控結構以硅元素的配位數為基礎
一個2-(苯偶氮基)苯基引入到硅元素上是通過一個有機鋰衍生物,它的制備是在-105°C的條件下,2-碘基偶氮苯(E)-1在丁基鋰的作用下進行的(如圖2)。3,4)硅的配位態是很容易通過29Si的核磁共振波譜確認的。2 -(苯偶氮基)苯基衍生物和與此相似的苯基衍生物的化學位移的差異只有±2ppm,這表明硅元素提供了一個4配位態,其偶氮基團的配位態幾乎沒有變化。因此,期望硅的親電性通過氟化作用會增加,單氟硅烷(E)-3e和(E)-3f的制備是通過單氫硅烷(E)-2e 和(E)-2f分別與氟化銀反應的。雙乙氧基硅烷(E)-2g和三乙氧基硅烷(E)-2d分別與BF3?OEt2反應制取雙氟硅烷(E)-3g和三氟硅烷(E)-3d。(E)-3d-g中硅元素的配位態與類似的苯基衍生物通過29Si的核磁共振來相比較,就會發現(E)-3d-g的化學位移高出11 ppm多。科學家發現硅原子的5配位態通過偶碳基團協調作用,氟硅烷衍生物在溶液明顯表現出光譜屬性。是否存在這種配位作用是經x-線衍射單晶分析確認的 。若化合物中沒有氟原子,體積龐大的硅取代基是被發現位于氮原子的對位。通過對比,結果表明,在硅原子上存在至少一個氟原子,五配位態的硅原子可以與一對孤對氮原子相互作用,導致硅原子周圍的的周圍形成一個扭曲的三方雙錐體結構。形成一個N-Si配鍵誘導代換氟原子是歸因于增加親電性的硅原子和電負性氟原子,正如在前面報道的,有機硅烷的配體數不同于偶氮基團。
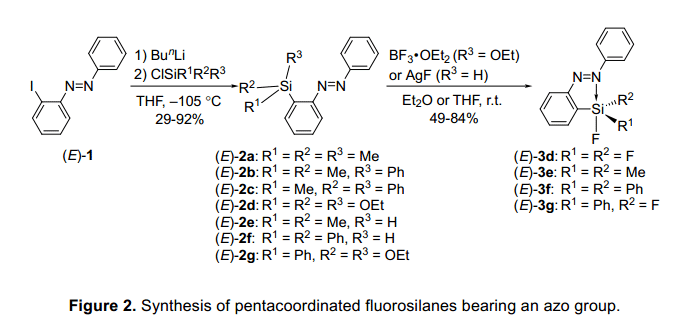
硅原子不同的配位狀態可以通過化合物的晶體顏色很容易地區別出來。四配位態的含硅偶氮苯且沒有氟原子,顯示一個紅色或橙色的色彩,五配位態的含硅偶氮苯(E)-3d-g顯示黃色。通過紫外/可見光譜觀察在二氯甲烷的溶液里的四配位態(E)-2a-g化合物,他們的吸收最大值歸結為p-p* 和n-p*,分別轉換為325-327nm和441-456nm。與沒有取代基的偶氮苯(p-p* 318nm ,n-p* 轉換為441nm)相比,四配位態(E)-2a-g化合物略紅移,這種紅移證明通過有機硅基團的供電子基的誘導效應提高了n-和p-軌道的能級。相比之下,在偶氮苯(E)-3d-g與五配位態的硅取代基,最大吸收值歸結為p-p*躍遷觀察到的紅移約336-349nm,而最大吸收值歸結為n-p*躍遷觀察到相對藍光偏移。因此,不容易發現化合物(E)-3d或者(E)-3g存在n-p *躍遷吸收光譜,可能是因為這是藏在p-p*躍遷。這些結果表明,氮原子和硅原子形成一個配位鍵穩定了n軌道并且π軌道變得比π*軌道相對不穩定。
當(E)-3d-g用波長為p-p*躍遷(l=360nm)的紫外燈照射時,使用超高壓水銀燈和一個彩色的玻璃過濾器,他們異構化成相應的化合物(Z)-3d-g,并且具有81~99%的高收益率(如圖3)。異構化作用后,產生這些化合物顯示橙色。最大吸收值在大約340nm處下降,與此同時在440nm處有一個最大吸收值,這是因為p-p*躍遷增加了。此外,當(Z)-異構體用波長為l=431nm紫外燈照射,(Z)-異構體能被可逆地轉變為(E)-異構體。
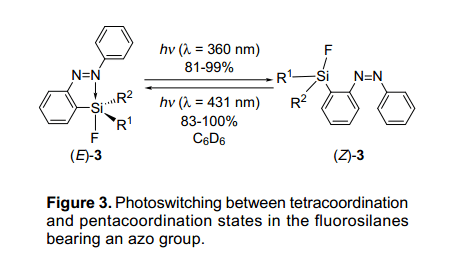
(Z)-異構體在光異構化作用后的配位態可以通過Si NMR檢測。(Z)-同分異構體與相應的(E)-同分異構體相比其化學位移要低些,但和苯基衍生物的化學位移相似,這說明(Z)—同分異構體具有四配位態。特別是,氟代甲硅烷基聯苯衍生物的兩個(E)-3f 和(Z)-3f同分異構體可能被孤立,這表明同分異構體(E)-3f和(Z)-3f的硅原子分別具有五配位態和四配位態。這兩種結構通過x-射線衍射單晶分析被進一步證實了,通過光異構化進一步展示了硅原子的結構變化。
由于我們成功地光轉化氟代硅烷的五配位態和四配位態,我們下一步試圖通過類似的方法用不同配位態的硅原子開發各種光轉化條件。緊接著是五配位態的研究,下一步是研究六配位態。一個硅酸鹽和分子配位很容易形成六配位態。我們試圖進一步產生更高的配位態的硅原子通過把(E)-3d轉換成硅酸鹽。我們分析三氟硅烷(E)-3d的氟化作用通過添加氟化鉀和18-冠-6醚和已制取的硅酸鹽(E)-4d(圖4)。5)當用波長類似為偶氮基團的p-p*躍遷的紫外燈照射黃色硅酸鹽(E)-4d時,異構化幾乎定量進行,形成了紅橙色硅酸鹽(Z)-4d。異構化的(Z)-4d異構體也定量轉變成(E)-4d異構體,暗示(E)-和 (Z)-同分異構體可能定量的進行光異構化。低溫條件下19F和29Si核磁共振光譜和x-射線衍射單晶分析表明(E)-4d的六配位態的硅原子有一個扭曲的八面體結構,盡管(Z)-4d五配位態硅原子顯示一個三角形的雙錐體結構(圖5)。最戲劇性的變結構化在被發現在F-Si-F角度,這E)-4d異構體的角度是99.47(5)°和163.73(6)°,雖然(Z)-4d異構體的鍵角度分別是117.77(19)°和126.67(19)°。此外,(E)-4d,的F-Si-F鍵角是95.76(5)變為115.53(6)°。這是值得注意的是,光致輻照獨自誘導這樣一個偉大的結構變化并且在硅原子的周圍沒有添加任何化學試劑。因此,我們已經成功地通過光致輻照五和六配位態硅酸鹽4d控制配位數變化,這一直伴隨控制硅原子周圍的構象。
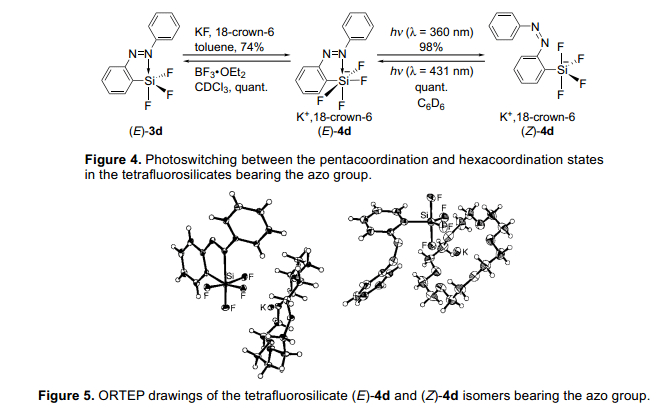
有許多的報告中,化合物物理屬性的光轉化是通過使用偶氮苯的光異構化。在這之前研究,在大多數情況下取代基是位于偶氮基的對位或間位,2)通過調(E)和(Z)同分異構體的每個取代基位置關系或方向,尋找光控條件獲得化合物的物理性質。與這些以前光轉化系統不同,然而,我們在這里介紹的光轉化系統是獨特的,硅原子結構可以交換使用在硅和孤對氮原子之間的位置關系的變化。即使化合物的有機軸承取代基的硅原子,如果取代基的方向可以交換通過使用這個方法并且這合成的物質進一步結合定向調控的偶基團的對位取代基,這個系統可能會應用于各種類型物理性質的光轉變條件。
3.二氧化硅基于硅原子的配位數變化而導致光轉換活性的變化
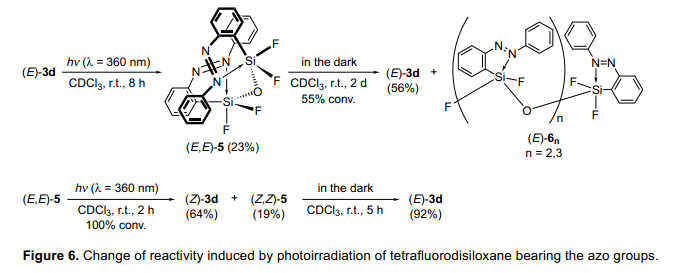
在前面兩部分中,我們已經介紹光照可以控制含硅分子的生成結構。那么,接下來的問題已經出現,“我們能否控制他們的反應活性?”當(E)-3d三氟硅烷的穩定性被測定后,研究發現(E)-3d三氟硅烷在(E,E)-5-1,1,3,3,—四氟二甲硅醚漸漸水解了。(圖6)(E,E)-5在其分子內連接了兩分子的偶氮苯。考慮到偶氮苯可以輕松的堆疊成結晶狀態,兩分子偶氮苯利用Si-O-Si之間的間隔可以并排在兩個苯環的3.4—3.6?空間內。在避光條件室溫下,(E,E)-5二甲硅烷醚在兩天內進一步降解,形成(E)3d和(E)-6n(n=2,3)低聚硅氧烷的混合物。光照可以催化(E,E)-5的降解,并且光照2h后,(E,E)-5全部降解,由于這個反應,四配位數的(Z,Z)-5二甲硅氧醚的兩個偶氮基團被異構化,除了生成(Z)-3d。當(E,E)-5在避光室溫條件下將生成(E)-3d,并且由(Z,Z)-5的合成速率比(E,E)-5的大。
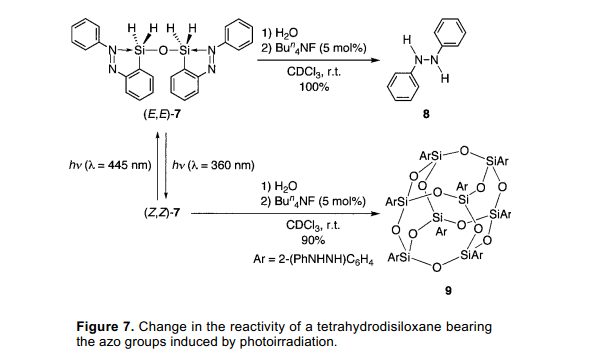
對于(E,E)-7分子,相應的(E,E)-5的四氫衍生物的反應活性在光照前后有明顯的變化。在一定量的四丁胺氟化物催化下,(E,E)-7被水解成二苯肼8伴隨著C-Si鍵的斷裂。(圖7)7)另外,當嘗試類似的方法使用四配位數的硅化物(E,E)-7可以定量的光照(Z,Z)-7制得。倍半硅氧烷9的制備沒有C-Si鍵的斷裂,盡管偶氮基團減少了。因此,反應活性的改變伴隨著C-Si鍵的斷裂可以被光照條件控制。
4.光變對丙烯硅烷反應活性的影響:改變硅原子的配位數
正如在前面章節中展示的,眾周所知,有機硅分子的活性因其配位數的不同而明顯不同。盡管這里在我們沒有詳細討論它們的反應機理,不同的活性伴隨不同的配位數有如下原因。相比于電荷形式,硅與取代基鍵顯示極性,三中心四電子鍵存在于五或六配位數狀態。這將導致取代基親電性的增強,并且取代基活性也比四配位狀態強。一般來說,硅原子的配位數可以由四配位狀態改良為更高的五或六配位狀態,通常是增加一種試劑到反應體系來產生一個高活性的配位物質。然而,正如上面所描述的,控制配位數很容易實現,只需要光照偶氮基團而不需要添加其他任何化學試劑。下一步,我們嘗試著控制Hosomi-Sakura反應,這是一個著名的利用硅試劑的反應,并研究光控烯丙硅烷的活性對偶氮基的影響。
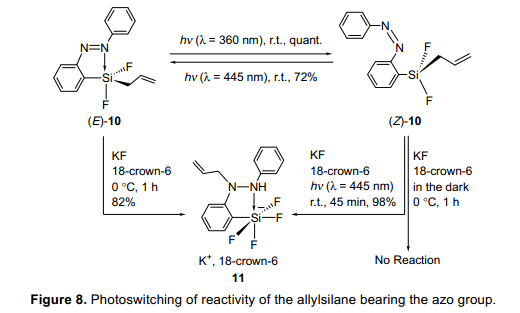
具有偶氮基團的烯丙基雙氟代硅烷(E)-10被合成,其協配位態通過使用多核磁共振光譜和x-射線衍射單晶分析被研究。正如預期的那樣,這是證明(E)-10的硅原子顯示五配位態,而光異構化得到的(Z)-10的硅原子顯示四配位態。苯甲醛新增了一項親電基,但是沒有反應的進行。因此,在18-冠-6醚存在的條件下,氟化鉀與(E)-10反應是為了激活(E)-10,結果導致N-烯丙基硅酸鹽11(N-allylated silicate 11)的產生(圖8)。另一方面,緊接著(E)-10被光異構化成(Z)-10,其次是在黑暗條件下氟化鉀存在于18-crown-6沒有反應。有趣的是,光致輻照誘導了反應繼續并生成化合物11,類似的例子(E)-10。由于在光致輻照條件下,五配位態的(E)-10和四配位態的(Z)-10可能是相互的轉化的;這些結果表明光致輻照條件可以控制烯丙基硅烷的反應性。結果從幾個控制的實驗顯示從(E)-10形成化合物11是一個分子內反應,在這個反應中,烯丙基基團從硅原子轉移到氮原子上在g位。這說明,氮配位誘導增加烯丙基基團的親核性,也增加了硅原子的親電性,增強偶氮基團的極化并且六元環過渡態都在這些反應的過程扮演著一個重要的角色。
當偶氮集團被認為是一種反應底物,(Z)-和(E)-同分異構體可以分別被認為對應被保護和脫保護的基團,這適用于多步反應包括上面描述的烯丙基化反應。換句話說,保護和脫保護的反應基團是通過使用不同波長的光輻射。
5.硼化合物的劉易斯酸光轉化攻擊偶氮基團
作為主族元素的一個實際應用,除了增加取代基的親核性,有其他一些方法可以修改主族元素本身的屬性,譬如硅化合物。例如,有機硼化合物具有劉易斯酸的性能和該性能已被廣泛應用于各種有機合成反應。作為一個基本研究控制與硼化合物反應的反應性例如路易斯酸催化劑,我們調查了光是否控制配位數,兒茶酚硼烷攻擊偶氮苯的一部分及其劉易斯酸,評價劉易斯酸的變化使用與吡啶生成絡合物作為其反應指數。
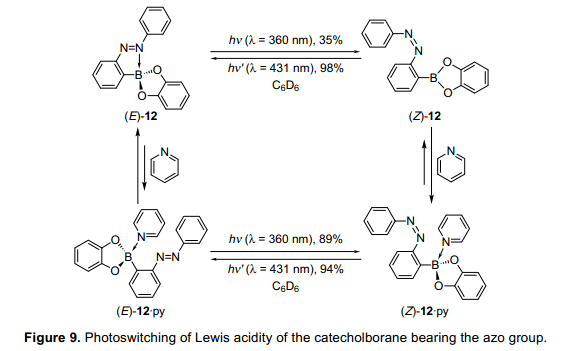
硼酸與偶氮苯基團發生脫水縮合反應,生成兒茶酚硼烷(E)-12。光致輻照條件下,(E)-12在苯溶液中可逆地進行光異構化,盡管其異構化效率不高(圖9)。等摩爾數的吡啶與兒茶酚硼烷(Z)-12反應,11B核磁共振的結果顯示在前場的明顯轉變,這是證明了一個復雜的成立,吡啶作為一個路易斯堿存在這種異構體。相比之下,當(E)-12的異構體與吡啶反應,化學位移沒有顯著的變化,表明(E)-12的分子內配位可能會擾亂吡啶分子間配位,導致(E)-12與吡啶不能形成絡合物。此外,光異構化反應可逆地進行,甚至在吡啶過量的條件下。即,當用紫外燈照射(Z)-12?py時,(E)-12?py和(E)-12之間的平衡是明顯轉向(E)-12的。這些結果顯示,大多數吡啶分子形成復合物而兒茶酚硼烷可能被釋放硼原子和變得自由。當改變等摩爾數吡啶后,通過11B核磁共振估計化學位移值,來測量絡合物的絡合值。我們發現,絡合物增加了大約300倍,通過光異構化使(E)-12轉變為(Z)-12。因此,由結果判斷與吡啶分子形成絡合物,通過劉易斯酸在硼化合物被成功執行。
6.膦基偶氮苯和分子內鏻鹽之間的平衡控制
在上面所描述的硅或硼化合物,偶氮基團在這些化合物中擔任親核試劑的作用。然后我們考慮是否有可能控制主族元素的配位數,當偶氮基團也作為一個親電試劑。有機磷化合物是一個主族化合物作為一個親核試劑或者一個路易斯堿在一個正常的配位態下。例如,磷化氫已經被廣泛的用作與過渡金屬形成配體。如果我們能表明我們可以控制有機磷化合物的配位數,那是可以預期,我們也許能夠控制化合物的配位能力通過過渡金屬和由他們合成的催化劑活性。
2-鋰基偶氮苯被二苯氯化磷接受并且膦類化合物的合成嘗試通過類似反應使用硅和硼。然而,沒有獲得相應的膦類化合物。經過反復嘗試的過程,我們發現2-碘基偶氮苯(E)-1被轉換成磷氫基硫化物(E)-14通過與二苯肼(E)-13反應。(E)-14與三丁基磷化氫經過脫硫作用導致2-雙苯基膦基偶氮苯(E)-15的合成(圖10)。12)化合物(E)-14也可以得到通過2-鋰基偶氮苯與雙苯基硫代磷酸化異煙酸氯化物(13)的反應。自膦基基團通常作為一個親核試劑,但不是一個親電體,估計偶氮基團可能作為一個電子受體。然而,化合物(E)-15顯示一個磷化氫結構,其中在晶體狀態中偶氮基團沒有交互氮和磷原子。化合物(E)-15在甲苯溶液中顯示熱致變色和在100°C下顯示一個紅色的顏色,但在低溫條件如-78°C時變成黑色,這樣的情況和通常的偶氮苯是不同的。此外,化合物(E)-15的31P核磁共振化學位移表現出明顯的溫度依賴性。在溫度高于60°C時,它在-9.2ppm顯示一個單線態,在20°C和-60 °C之間顯示一個廣泛的信號,并且低于-60°C時在30.1 ppm和-10.3 ppm處呈單譜線。在強磁場信號屬于膦結構,而信號低場屬于分子內磷鹽16基于比較觀測到的化學變化和這些估計的GIAO計算。這表明分子內磷鹽16應該是分子內磷化氫基團攻擊偶氮基團產生的物質。黑顏色是在較低的溫度下對應的陰陽離子16的過渡分子內電荷轉移的,而紅顏色是歸因于在高溫度下偶氮基團的p-p*躍遷。
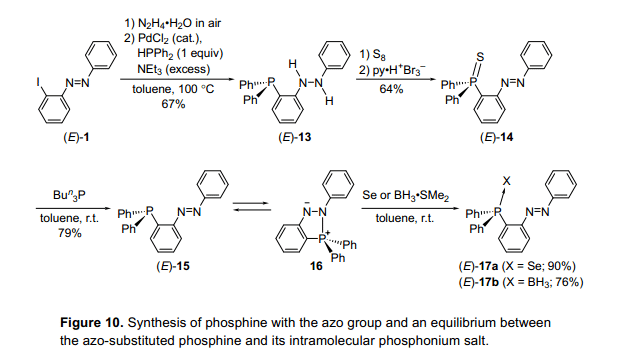
考慮到所有這些結果,在室溫下磷化氫化合物(E)-15和分子內磷鹽16形成一個平衡。 當溫度升高,平衡是轉向(E)-15,而低溫度導致轉向化合物16。這證明了我們可以成功地通過改變溫度控制膦(E)-15和磷鹽16的平衡。當反應在一個平衡溶液是使用是與硒BH3?SMe2、磷化氫硒化物(E)-17a和磷化氫硼烷(E)-17b反應形成,表明這個磷化氫有普遍的反應性。它可以很容易地與水反應而不像往常膦類化合物。例如,類似的衍生物(E)-15’在4位有一個甲基,存在一個很少量的水促進磷化氫氧化物18的聯苯肼基的形成。分子內磷鹽來源于2-膦基偶氮苯,顯示與Mitsunobu反應的一個中間體相似的性能。14)它們的反應性也支持膦類化合物和分子內季磷鹽存在一個平衡。
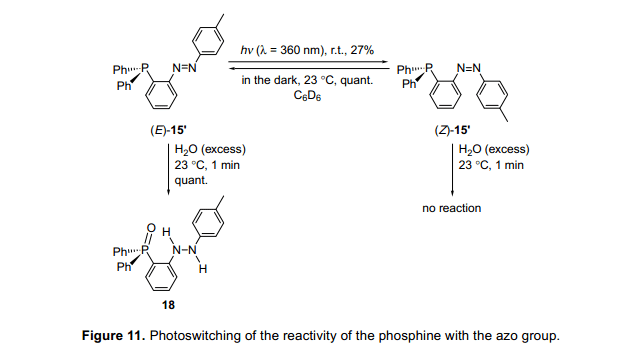
然后,我們懷疑這些膦化合物的配位數可能受光致輻照的控制,光致輻照(E)-15發并現沒有異構化發生。然而,有一個甲基(E)-15''經光輻射,光異構化后產生(Z)-15”(圖11)。13)然后我們監控(E)-15”或(Z)-15”與水的反應。(E)-15'與水迅速反應,一分鐘后完全消失,盡管沒有觀察到(Z)-15'的變化。最后,在很長的一段時間的反應之后(Z)-15”也產生了18,這是由于它的熱異構化。因此,磷化氫的反應性能是在一個有限的時間內可以控制光致輻照分子內磷鹽向水均衡。
7.開發的熒光偶氮苯與硼取代基
在前面的章節中討論的一樣,在2位置含有主族元素取代基的偶氮苯顯示各種各樣的顏色如黃色、橙色、紅色和黑色。實際上,通過修改偶氮苯取代基,偶氮苯可以進一步顯示各種不同的顏色,并且偶氮苯的這個性能已被用作偶氮染料的基本結構性能。偶氮染料幾乎占了全球一半的工業染料生產,并且在印染行業中占據著重要的地位。一些顏料,它被稱為熒光染料,不用吸收一個特定光譜的光線,但也能發出光作為熒光。然而,在室溫下,偶氮苯一般不會發出任何重要的熒光產生光致輻照,因為光異構化通常在偶氮苯中是收益的。據報道,一些含鈀化合物與偶氮苯作為一個配體15)和一些聚合體16)攻擊偶氮苯,作為一個組件可以異常發出弱熒光。這含有偶氮苯的鈀配合物作為配體,然而,熒光量子收益率只有10-5到10-3。
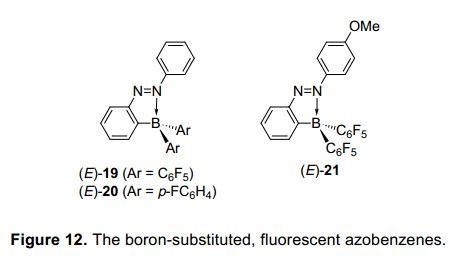
我們已經合成偶氮苯的化合物,這可以接受光異構化,而不受互動的含氮原子的偶氮基團和主族元素的限制。對于含有2—硼取代基的偶氮苯的異構化產量與硅相比很低。這是需要找到一種硼取代基偶氮苯,可以更有效地在光致輻照條件下異構化。在這個隨后的研究中,我們調查了大量含偶氮苯基團或硼原子的芳環上不同的取代基,并檢查了取代基之間的關系類型和他們的光學性質。因此,我們發現一個平衡在三配位態和四配位態,傾向于轉向四配位態,當有一個化合物有供電子偶氮苯基團的4位上或一個吸電子基在硼原子上,這將導致增加可吸收光譜。此外,它也表明了他們配價鍵增強,異構化率降低,并且有一些化合物未能進行異構化。這些結果表明,硼取代偶氮苯化合物不適合配位數的控制,這也成為我們最重要的目標。然而進一步詳細分析了,表明在各種硼取代基的偶氮苯基團不能光異構化,在室內光線下2(五氟苯酚)-硼基-偶氮苯(E)-19在溶液中發出綠色熒光(圖12)。17)在室溫下在己烷溶液中,熒光量子產率為0.23,這相對偶氮苯是較高的。然而,化合物(E)-20的五氟苯酚基團被對氟苯酚基團所取代,但是不發射任何熒光。這些結果表明,N-B共價鍵的鍵能和熒光強度之間可能有關系。因此,我們接下來調查了芳環上的不同取代基,發現化合物(E)-21有一個甲氧基在偶氮苯的4位上具有更強的熒光,并且在室溫下己烷溶液中它的量子產率是0.76。在曾被報道偶氮苯衍生物中,這個熒光量子產率值是最高的。它表明,(E)-21發射熒光比未被取代的偶氮苯發射的30000倍還強。
因此,我們下一步試圖從理論和實驗上確定硼取代偶氮苯化合物發射的熒光原因。這是推測,N-B配位鍵可能不會只抑制偶氮苯的結構變化,也相對提高p軌道的能級通過降低n軌道的能級。這倒逆轉變化能級會使p-p*躍遷從基態躍遷到到最低的能級。因此,從最低的能級躍遷到基態是容易發生的,這進一步導致在一個高產率下吸收光能產生熒光。在最開始的研究中,我們沒有設想,引入硼取代基到偶氮苯會誘導熒光發射。然而,這里所介紹的硼取代偶氮苯比報道鈀配合物發出更強烈的熒光。主族元素獨特的性質提供了偶氮苯的更強烈的熒光,而沒有使用昂貴的鈀。
8.總結
我們介紹了一個模型系統,可以變換主族化合物的物理性質和結構,通過使用光致輻照誘導偶氮苯的異構化作用,作為一個關鍵的反應。這種方法同樣被認為是適用于其他主族元素,它被高度期望動態地控制元素特定的物理性質而不僅僅是以上描述的那些。如果我們能進一步開發新的方法,可以直接控制主族化合物的配位數,并基于上述闡述的概念,我們相信這種方法的應用將打開一個新方法控制有機反應,這激活/失活方法的使用類似主族元素的配位態的方法。最近報道,一個新的有效合成方法已開發使用,掩蔽和暴露硼元素,18)對于這樣的目的如果這里介紹的方法能夠得到應用,這個新方法它是可行的。當前的研究結果的理論和實驗,并且等同于實際使用和應用在一個在實踐層面上。我們認為,然而,我們在這里的概念與傳統的是不同的。因此,我們將會很高興如果這個獨特的概念可以用來控制有機反應或化學過程,如保護胺。非常值得一提的是,在研究主族化合物時,我們發現一個意想不到的,令人驚訝的產品——熒光偶氮苯。我們確信主族化合物一定存在很大的研究價值,等待我們去發現和利用。
參考文獻
1. (a) Tamao, K.; Ishida, N.; Tanaka, T.; Kumada, M.Organometallics 1983, 2, 1694. (b) Tamao, K., J. Synth.Org. Chem. Japan, 1988, 46, 861.
2. (a) Molecular Switches; Feringa, B. L., Ed.; Wiley-VCH:Weinheim, 2001. (b) Balzani, V.; Credi, A.; Raymo, F.M.; Stoddart, J. F. Angew. Chem., Int. Ed. 2000, 39,3348. (c) Feringa, B. L.; van Delden, R. A.; Koumura,N.; Geertsema, E. M. Chem. Rev. 2000, 100, 1789. (d)Ichimura, K. Chem. Rev. 2000, 100, 1847.
3. Kano, N.; Komatsu, F.; Kawashima, T. Chem. Lett.2001, 338.
4. Kano, N.; Komatsu, F.; Yamamura, M.; Kawashima, T.J. Am. Chem. Soc. 2006, 128, 7097.
5. Kano, N.; Komatsu, F.; Kawashima, T. J. Am. Chem.Soc. 2001, 123, 10778.
6. Kano, N.; Yamamura, M.; Komatsu, F.; Kawashima, T.J. Organomet. Chem. 2003, 686, 192.
7. Yamamura, M.; Kano, N.; Kawashima, T. TetrahedronLett. 2007, 48, 4033.
8. (a) Hosomi, A.; Sakurai, H. Tetrahedron Lett. 1976,1295. (b) Hosomi, A. Acc. Chem. Res. 1988, 21, 200.
9. Kano, N.; Yamamura, M.; Kawashima, T. J. Am. Chem.Soc. 2004, 126, 6250.
10. Yamamura, M.; Kano, N.; Kawashima, T. J. Organomet.Chem. 2007, 692, 313.
11. Kano, N.; Yoshino, J.; Kawashima, T. Org. Lett. 2005,7, 3909.
12. Yamamura, M.; Kano, N.; Kawashima, T. Inorg. Chem.2007, 45, 6497.
13. Yamamura, M.; Kano, N.; Kawashima, T. J. Am. Chem.Soc. 2005, 127, 11954.
14. (a) Mitsunobu, O. Synthesis 1981, 1, 1. (b) Hughes, D.L. Organic Reactions; Wiley: New York, 1992; Vol. 42,pp 335-656.
15. (a) Wakatsuki, Y.; Yamazaki, H.; Grutsch, P. A.;Santhanam, M.; Kutal, C. J. Am. Chem. Soc. 1985,107, 8153. (b) Ghedini, M.; Pucci, D.; Crispini, A.; Aiello,I.; Barigelletti, F.; Gessi, A.; Francescangeli, O. Appl.
Organomet. Chem. 1999, 13, 565.
16. (a) Shimomura, M.; Kunitake, T. J. Am. Chem. Soc.1987, 109, 5175. (b) Han, M.; Hara, M. J. Am. Chem.Soc. 2005, 127, 10951.
17. Yoshino, J.; Kano, N.; Kawashima, T. Chem. Commun.2007, 559.
18. Noguchi, H.; Hojo, K.; Suginome M. J. Am. Chem. Soc.1985, 107, 8153.
注:本文為提供者整理翻譯的,由于知識所限,錯誤在所難免,敬請原諒。如有問題可以查找原文。
統計數據
共收錄化學品數據
147579 條



 滬公網安備 31010602001115號
滬公網安備 31010602001115號