一種具有催化作用的碳自由基的新發現和它在有機合成上的應用
- 2012-04-11
- 專題
1. 前言
碳自由基有較高的化學反應活性,它是烷基自由基的典型例證。近年來,生成碳自由基的各種方法被積極研究,并廣泛應用于有機合成方面。生成烷基自由基的典型方法是通過自由基引發劑例如AIBN存在下,引發烷基鹵化物與Bu3SnH或 (Me3Si)3SiH反應;巴頓酯類或酰基過氧化物的熱解;或者金屬離子的單電子氧化反應1)。然而,這些反應都是化學計量反應,適用于小規模的實驗室使用,但很難應用于大規模的工業合成。工業上有一些產生烷基自由基的方法,例如在自由基引發劑下或光致輻照下引發烷烴的反應,這些方法被用于鏈烷烴的自氧化。然而,自氧化反應過程需要嚴格的反應條件,尤其應在高溫下完成。在如此高的溫度下,鏈烷烴不但發生C-H鍵的均裂,而且有C-C鍵的均裂,其中C-C鍵能比C-H鍵能低。因此,這類反應的選擇性低并且反應效率不足2)。至今,還沒有令人滿意的常規方法能在溫和條件下,使得鏈烷烴中C-H鍵均裂而生成有選擇性的碳自由基。為了實現這一目標,需要一種新方法能在溫和條件下產生碳自由基。這一方法將成為有機合成中一種不可缺少的工具。
最近,我們發現由N-羥基鄰苯二甲酰亞胺生成的苯鄰二甲酰亞胺N-氧基(PINO)自由基能夠在溫和的條件下取代多種碳氫化合物(如:烷烴,醇,醚,縮醛和醛)C-H鍵上的氫原子而生成相應的碳自由基,這些自由基都具有高的選擇性和較高的催化效率3)。NHPI被命名為“產生碳自由基的催化劑”(簡寫成CRPC)。利用CRPC能夠合成含氧化合物,例如由烷烴來合成相應酮和羧酸。CRPC同時還有力地促進了官能團在溫和條件下加成到烷烴分子上生成具有高選擇性的硝基烷烴,烷基磺酸及氧化烷烴,其中這些反應在以前均難以實現。同樣也使合成二元羧酸變為可能,例如己二酸常由硝酸氧化而制得,如今利用分子氧經一步反應氧化環己烷就能生成高產率的己二酸。N2O是溫室氣體中的一種化合物,它所產生的溫室效應是CO2的300倍乃至更高,而采用硝酸氧化的方法不可避免的產生溫室氣體N2O。從綠色化學的角度來講尋找一種制造己二酸且不產生N2O副產物新的合成方法尤為重要。用CRPC催化烷烴反應生成烷基自由基是一種創新方法并將對化工行業產生重大影響。一些用CRPC催化的反應已經實現了工業化。
2. 催化碳自由基產生方法的新發現
Grochowski和他同事在1977年首次報道了NHPI催化應用,催化乙醚加成到偶氮二羧酸二乙酯(DEAD)上的反應4)。當時并未詳盡的描述此反應,也未用實驗證明PINO的生成。然而,由于自由基清除劑的存在以至于該反應沒有任何進展,公認的反應過程如(合成方案 1)所示。NHPI上羥基酰亞胺基團上的氫原子轉加到DEAD上,爾后跟生成的產物N-氧基鄰苯二甲酰亞胺和新自由基形成平衡。這一步生成的PINO使α碳上的氫原子分離到醚氧上,產生新的自由基A,A加到DEAD上生成一個新的加成自由基B,自由基B取代醚上的氫原子生成加和物C和自由基A。
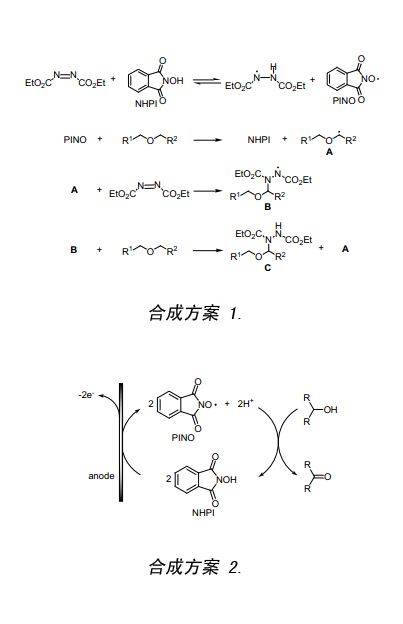
另外,Masui等人在1983年報道NHPI作為電解氧化二級醇生成酮的中間產物5)。大家認為在陽極上產生的PINO使醇α碳上的氫原子分離,進而催化其氧化產物生成酮(合成方案 2)。
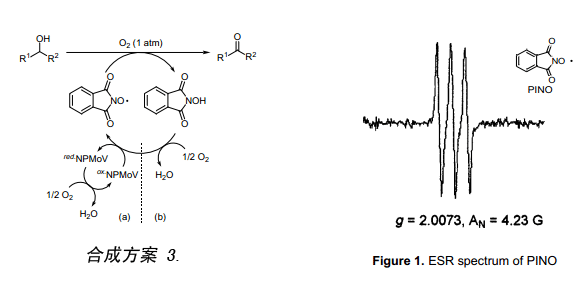
在研究用鉬釩磷酸鹽(NPMoV)催化醇和分子氧氧化反應過程中,可以形成一個平均成分表示為(NH4)5H6PV8Mo4O40,我們認為單獨采用NPMoV催化劑不能引發此反應,但是其如果能與NHPI結合將會增強此反應(合成方案 3)。發現反應過程跟預期設想的一樣(路徑 a),同時還意外地發現在沒有NPMoV存在的情況下NHPI催化醇發生氧化反應過程(路徑 b)。該氧化反應是由分子氧(一種三重自由基分子)和NHPI發生反應而致并產生PINO,而后PINO取代醇上的氫原子生成相應的酮。為了證實NHPI產生PINO,在苯甲腈體系中將NHPI與氧分子接觸,采用ESR波譜儀觀測到PINO生成的一個三重態圖譜如圖一所示((Figure 1)。
人們發現PINO具有跟CRPC一樣的功能,能夠在溫和的條件下選擇性取代有機基質C-H鍵上的氫原子生成碳自由基,其本身恢復為NHPI。因碳自由基是活性化學物質,所以采用不同種類的分子(例如氧分子)捕獲它能夠引入不同的官能團。下文詳盡敘述了NHPI所催化的多種催化反應,還包括在傳統有機合成中未曾出現的新的概念等,因此,NHPI催化也將是化學合成的重大突破。
3. 分子氧氧化烷烴
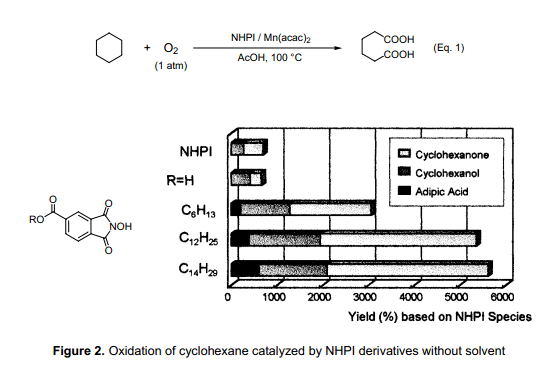
目前,采用環己烷自氧化法來合成尼龍-66每年至少需要2,000,000噸己二酸原料。如今還廣泛采用如下兩個步驟反應:Co鹽存在下,經空氣氧化環己烷首先轉化成環己酮/環己醇(K/A油),然后再用硝酸K/A油來合成己二酸6a)。本合成方法在1940年由杜邦公司開發,原則上一直延續到今天還在使用。反應第一步需要C-H鍵斷裂(C-H鍵裂解能:99.5 kcal mol-1),C-H鍵必須在劇烈的反應條件下(高壓,150~170℃)才能斷裂。為了避免產生副反應,環己烷的轉發率必須控制在3%~5%,從而使得該反應效率不盡如人意。反應第二步采用硝酸氧化產生大量副產物N2O。因為N2O是一種促進全球變暖的物質,所以工業上急需尋求一種不用硝酸氧化就能合成己二酸的新方法。沿著這些思路發展,已經有報道關于采用過氧化氫作氧化劑氧化環己烷生成己二酸,該合成方案作為綠色合成路線引起眾多人的關注6b)。
我們發現用NHPI與少量的Mn絡合物催化O2(1大氣壓)氧化環己烷生成己二酸(Eq.1)7),但僅僅采用NHPI卻很難使該氧化反應進行。然而, 加入少量的Mn絡合物(0.5mol%)后生成己二酸具有很高的選擇性,轉化率達到70%左右。近年來,不使用任何溶劑就能成功地將環己烷氧化8)。由于NHPI很難溶解于非極性溶劑(例如環己烷)中,因此在沒有溶劑的情況下很難有效地催化空氣氧化環己烷。結果表明,制備一種親脂性的NHPI衍生物并拿它作催化劑,在沒有溶劑的條件下就能高效地催化空氣氧化環己烷((Figure 2)。
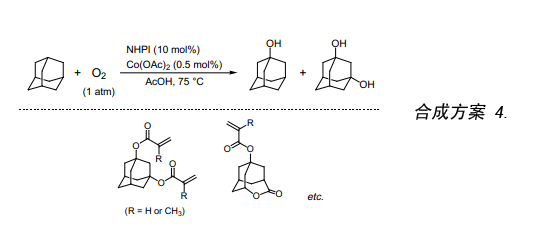
金剛烷具有一種獨特的結構,而功能化的金剛烷又是生產高性能材料的重要原料。盡管已有很多化學家嘗試用氧分子來氧化金剛烷,但尚無一人獲得足夠的收率及具有現實目的的選擇性。在NHPI/Co催化劑體系、醋酸存在下,分子氧在75℃氧化金剛烷生成產率為85%金剛醇和少量的金剛酮(合成方案 4)9)。就反應條件選擇上允許反應生成高選擇性的單醇或二元醇。經此合成方法由二醇或三醇合成的丙烯酸和甲基丙烯酸樹脂又是合成光刻膠的重要原料。
叔丁醇常用作增加汽油辛烷值的一種添加劑以及高純度的有機溶劑,工業上采用異丁烯水合的方法制備叔丁醇。異丁烷氧化直接來合成異丁醇是一個更為合理的方法,而采用傳統的自氧化過程就是為了合成過氧化叔丁醇,傳統合成方法在高壓(10大氣壓),200℃左右的高溫下才能產生過氧化叔丁醇(產率大約75%),叔丁醇(產率21%左右)以及8%轉化率的丙酮(約2%)10)。在苯甲腈體系中高壓條件下用NHPI催化劑催化氧化異丁烷生成產率為80%的叔丁醇(Eq. 2)11)。
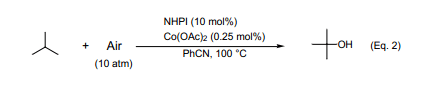
4. 烷基苯的氧化
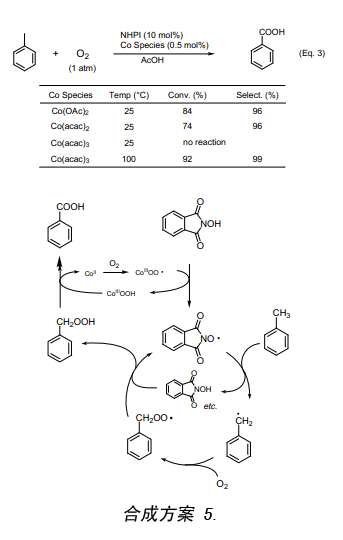
分子氧氧化烷基苯合成羧酸是工業上一種重要的有機合成反應。Co催化劑在高壓下130到160℃催化氧化甲苯生成相應的苯甲酸,其轉化率為50%,苯甲酸的選擇性大約為80%12)。然而采用NHPI和少量的Co(OAc)2作催化劑在1大氣壓室溫條件下就能催化分子氧氧化甲苯生成較高產率的苯甲酸(產率81%)和微量不純的苯甲醛(Eq. 3)13)。在這些反應條件下,用Co(Ⅲ)替代Co(Ⅱ)后卻不能引發該反應,實驗證明Co(Ⅱ)鹽和氧氣反應生成的Co(Ⅲ)氧絡合物才能引發此反應(合成方案 5);而用Co(Ⅲ)卻不能產生引發反應所必須的Co(Ⅲ)氧絡合物,因此在室溫下本反應并不發生。當溫度升高后Co(Ⅲ)被底物還原成Co(Ⅱ)繼而生成的Co(Ⅱ)與氧分子反應形成Co(Ⅲ)氧絡合物來引發該反應。因此,使用Co(Ⅲ)時可以觀察到反應誘導期。事實證明在常溫常壓下用分子氧催化氧化烴類如甲苯等對于氧化化學來說有著重要的意義。
對苯二甲酸是合成PET樹脂的原料因而其生產量很大,并且在不久的將來其需求量還會增加。如今,用Co/Mn/Br作催化劑在高溫高壓下經對二甲苯的自氧化來合成對苯二甲酸,此合成方法是由英國阿莫科石油公司開發研制的,其缺點是往氣相體系排放溴,腐蝕反應設備,因此人們急切希望研制一種無鹵素催化體系的催化劑。
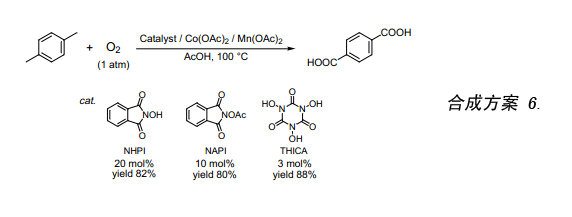
我們采用NHPI催化劑開發了一種無鹵素催化氧化反應,該反應用分子氧來氧化對二甲苯生成對苯二甲酸(合成方案 6)。再者,往NHPI上增加一個乙酰基生成N-乙酰基鄰苯二甲酰亞胺(NAPI)具有與NHPI相似的高催化活性。實驗發現如果我們采用NAPI作催化劑來催化生成相同量的對苯二甲酸所需的催化劑量是NHPI催化劑量的二分之一14)。此外,我們最近還發現三羥基亞氨基氰尿酸(THICA)具有很高的催化活性。NHPI催化氧化對二甲苯經一步反應合成產率為80%的對苯二甲酸需要NHPI催化劑20mol%,而采用THICA催化劑3mol%催化氧化就能得到同樣的效果。
氧化烷基雜環化合物所合成的羧酸被廣泛用作制藥藥物合成中間體,例如氧化甲基吡啶合成的煙酸是合成維生素的重要原料。目前,硝酸在高溫高壓下氧化5-乙基-2-甲基吡啶生成煙酸,可是,關鍵問題是同時還產生了大量的氮氧化物。與此同時還有報道用Co/Mn/Br催化劑催化甲基吡啶自氧化法合成煙酸,不過其反應條件比較苛刻且選擇性非常低15)。
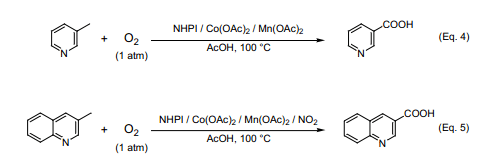
在催化量的NHPI和衡量的Co(OAc)2和Mn(OAc)2存在條件下醋酸環境里,我們用常壓的氧氣進行β-甲基吡啶氧化實驗,結果獲得較高產率的煙酸,而且產率可以達到77%(Eq. 4)16a)。NHPI/Co/Mn催化劑催化反應是一個不產生氮氧化物的無污染反應過程,可能在工業合成上非常有用。另外,3-甲基喹啉的氧化產物3-喹啉羧酸在自然界廣泛存在,已有很多關于其藥理活性的相關報道。但是,在過去很多重金屬鹽如KMnO4、CrO3常被用作氧化劑,發現往NHPI/Co/Mn催化劑體系中加入少量的NO2催化氧化分子氧跟3-甲基喹啉反應生成較高產率的喹啉羧酸(產率75%)(Eq. 5)16b)。還發現即便不存在過渡金屬鹽仍然可以采用NHPI/NO2催化分子氧氧化喹啉。尚未發現采用分子氧氧化喹啉的例子,本反應是迄今為止唯一一個成功的用分子氧氧化喹啉的氧化反應。
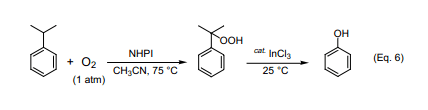
工業合成苯酚采用兩步法合成,合成步驟如下:在壓縮空氣(5到7個大氣壓)下90到120℃異丙苯在弱堿性體系里自氧化成異丙苯過氧化氫(產率20~30%),然后把未反應的異丙苯從反應溶液中分離、濃縮,再用稀硫酸處理濃縮產物生成苯酚和丙酮。盡管此方法早在20世紀40年代就已經確立應用了,但其至今仍是工業合成苯酚的主要方法。但是,該反應第一步的效率比較低。如果能提高異丙苯轉化成異丙苯過氧化氫的產率,該反應還會有更大的用處。發現在沒有重金屬鹽的乙腈體系里向反應溶液中加入少量的氯化銦,在NHPI催化劑跟自由基引發劑AIBN共同作用下可以獲得產率為77%的苯酚(Eq. 6)17)。
5. 分子氧氧化烯烴和炔烴
5.1 過氧化氫的合成及烯烴的環氧化反應
烯烴的環氧化反應尤其是采用分子氧作氧化劑氧化丙烯已具有一定的工業規模。最常用的方法是Halcon法(間接氧化法),該合成方法有兩個步驟:第一步是乙苯自氧化生成乙苯過氧化物,第二步在Mo催化劑催化下乙苯過氧化物作為環氧化反應的氧化劑完成烯烴的環氧化反應。
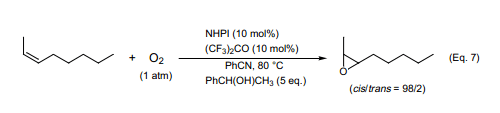
在此之前,我們發現NHPI催化劑催化分子氧氧化仲醇生成過氧化氫和酮19),反應中生成的過氧化氫用于烯烴的環氧化反應。在催化量的NHPI和六氟丙酮存在下1-苯乙醇和順-2-辛烯在常壓下氧化氣氛反應,再由生成的過氧化氫加成到六氟丙酮上而生成相應的氫過氧化物,隨后氫過氧化物做真正的氧化劑反應生成產率為87%的順-環氧化物(Eq. 7)20)。經自由基中間體生成的醛進展作用于分子氧氧化順-烯烴發生環氧化反應生成相應的順或反-環氧化物混合物21)。因而,分子氧氧化順-烯烴的立體選擇性環氧化反應在現實中比較困難。
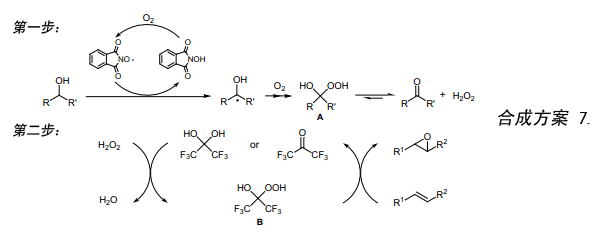
環氧化反應包含兩個過程:(i)NHPI催化醇和氧氣反應經過中間物α-羥基氫過氧化物(A)生成過氧化氫,這步反應是自由基反應;(ii)由過氧化氫與六氟丙酮反應生成的α-羥基氫過氧化物(B)來氧化烯烴進行環氧化反應(合成方案 7)。NHPI催化劑催化氧化仲醇也可以被用來作為一個極好的合成方法用于合成過氧化氫22)。
5.2 向炔烴的炔丙基位引入氧
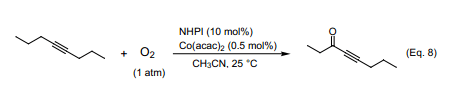
炔烴中炔丙基位上C-H鍵的離解能大約是85 kcal mol-1,大致等于烯烴中烯丙基位上C-H鍵離解能量(~87 kcal mol-1 )23)。因此,可以預期的是如果采用NHPI催化劑催化O2來氧化炔烴,炔丙基位可以被選擇性氧化,生成相應的α-炔基酮。正如我們所知的在含有NHPI(10mol%)催化劑和微量的Co絡合物乙腈體系中,4-辛炔跟O2分子在室溫下就能反應生成4-辛炔-3酮,并且產率可達75%(Eq.8)24)。炔酮通常是由一種金屬乙炔化物跟酰化試劑發生偶聯反應合成制得。將氧引入到炔丙基位置的文獻報道非常少,有一個例子是在SeO2催化下叔丁基過氧醇的氧化反應25)。本論文所報道的反應首次成功的把氧氣分子中的氧引入反應。
6. 氧氣分子氧化K/A油
K/A油是由環己酮和環己醇組成的混合物,是石油工業化學中一種重要的中間體還是用于生產己二酸的原料。拜爾—維立格氧化反應可以把環酮類化合物轉化成內酯類化合物。至今,未有關于采用氧氣分子作氧化劑的催化拜爾—維立格氧化反應的文獻報道,ε-己內酯是由環己酮與過氧乙酸經拜爾—維立格氧化合成而來。假如ε-己內酯的合成不是采用過氧乙酸實現的,而是利用氧氣分子作氧化劑K/A油經催化拜爾—維立格氧化反應合成的,那么,此反應由于其可以避免使用有害的過氧乙酸而變得尤為重要。
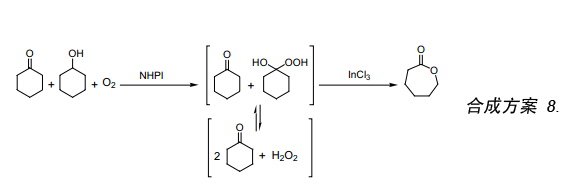
我們已經提出NHPI作為二級醇有氧氧化的一種高效催化劑。NHPI催化氧化二級醇通過形成羥基過氧化物中間體而產生酮和過氧化氫19)。至此,我們利用存在于K/A油中氧氣分子氧化二級醇生成過氧化氫,所生成的過氧化氫用作拜爾—維立格反應的氧化劑。該反應產生的ε-己內酯經有氧氧化反應首先將K/A油體系中的環己醇轉化成過氧化氫和環己酮。然后由過氧化氫和InCl3(合成方案 8)26)催化環己酮發生拜爾—維立格氧化反應。三氯化銦是路易斯酸其在水中比較穩定,如果反應后恢復還可以重復使用。
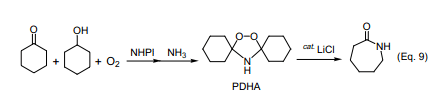
在催化量NHPI存在下,在乙酸乙酯中K/A油先經選擇性較好的有氧氧化反應,隨后經過氨氣處理生成過氧二環己基胺(Eq. 9)。眾所周知,PDHA很容易轉化成高收率的ε-己內酰胺。此反應是利用氧氣分子合成ε-己內酰胺前驅體的一種新方法,由于它不產生反應副產物硫酸銨而顯得更加有趣。
7. 使用NHPI催化劑將官能團加到烷烴分子上
7.1 CO引入到金剛烷上
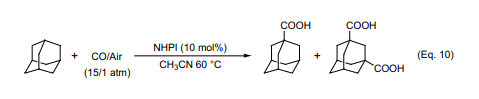
在CO/O2環境中采用NHPI作催化劑金剛烷經徹底的羧化且具有相對較高的選擇性。在60℃,NHPI(10%)和CO/Air(15/1大氣壓)存在條件下金剛烷反應生成金剛羧酸和少量的具有56%選擇性的氧化產物(轉化率為75%)(Eq. 10)27)。飽和烴經由CO的羰基化反應很難。因此,迄今為止,幾乎沒有關于烷烴催化自由基羰化反應的文獻報道。可以在文獻中發現一些采用過硫酸和光引發反應的報道28)。
7.2 烷烴的催化硝化和磺化氧化
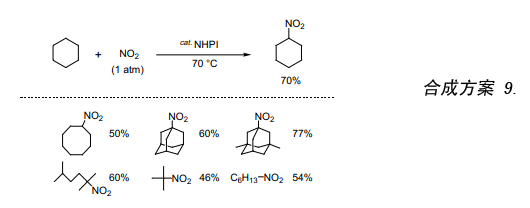
芳香族化合物的硝化和磺化氧化反應是已經確認的反應。但是,至今對于硝化和磺化氧化反應尚未有一個較好的通用型方法。在工業上烷烴的硝化是一個重要的反應,采用硝酸或NO2作硝化劑在溫度高達250~400℃方可反應。不過,在這么高的溫度下,C-C鍵的斷裂也容易發生,因此,致使硝化反應的選擇性相當差。例如,環己烷在240℃與NO2發生硝化反應生成硝基環己烷,其產率僅有16%29)。在催化量的NHPI和O2存在條件下,我們將環己烷跟NO2反應,發現在70℃時就能平穩地反應而且硝基環己烷的產率可以達到70%((合成方案 9)。再者,在反應后經過簡單的過濾該催化劑可一定量的收集30)。我們還成功的實現了用硝酸代替NO2作硝化劑進行這類硝化反應31)。
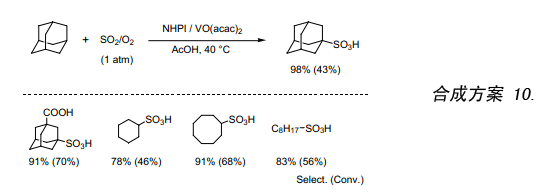
只有少數報道關于烷烴磺化氧化反應的研究。其中一個例子是在SO2/O2存在下烷烴經光引發而反應。但是,該反應的效率很低以至于沒有后續的研究報道。我們發現金剛烷跟極少量的VO(acac)2,在SO2/O2環境中用NHPI催化劑催化反應生成產率較高的金剛烷磺酸(合成方案 10)。此外,我們還發現該反應僅由VO(acac)2催化。更進一步說,低碳數烷烴如丙烷在室溫下就能用此方法有效的被磺化氧化32)。
7.3 烷烴的肟化反應
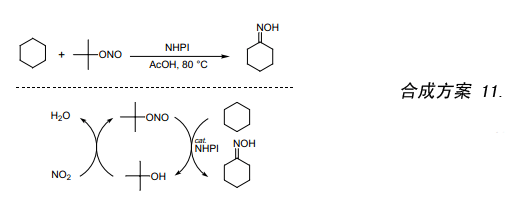
環己酮肟是生產尼龍-6的主要原料之一,其制備方法是先將環己烷氧化成環己酮,然后再與羥胺鹽反應。然而,該方法因其反應過程中產生大量的副產物硫酸銨而有很多缺陷。我們發現在氬氣作保護氣條件下,環己烷與亞硝酸叔丁酯、醋酸在80℃經一步反應生成環己酮肟(合成方案 11)。該反應是合成肟的新方法優點是不產生副產物硫酸銨。此外,一步反應合成環己酮肟已是可能的,并有望成為一種具有突破性的合成方法。再者由于叔丁醇跟NO2很容易反應合成亞硝酸叔丁酯,以及叔丁醇在反應后能夠再生并被多次重復使用,此反應具有很高的原子效率。
7.4 NHPI催化劑催化烷烴生成烷基陽離子
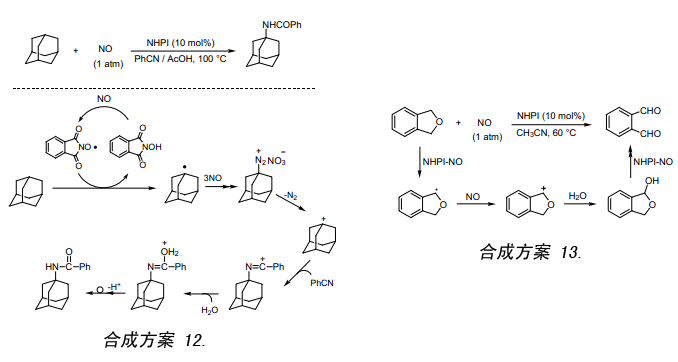
NO是雙原子分子常以自由基的形式存在。如果能從NHPI上脫去氫原子生成PINO,那么也同樣可以脫去氧分子,這樣它可以作為一種新的NO合成反應而應用。我們嘗試用NHPI作催化劑,金剛烷跟NO及含有少量醋酸的芐睛反應獲得產率為65%的N-1-金剛烷苯甲酰胺(合成方案12)33a)。此外,我們還發現1,3-二氫化異苯并呋喃跟乙腈中的NO反應生成鄰苯二甲醛(合成方案13)33b)。鄰苯二甲醛還可以通過源于鄰二甲苯的四溴鄰二甲苯水解得到34)。大家都知道至今還沒有直接從1,3-二氫化異苯并呋喃合成鄰苯二甲醛的例子。在此反應中,生成的碳正離子作為中間體與親核試劑水反應生成半縮醛,半縮醛再經相似的反應過程被氧化成鄰苯二甲醛。
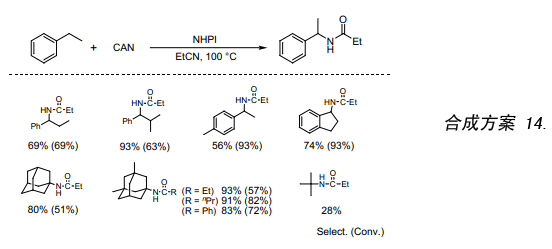
我們發現用NHPI催化劑催化,與硝酸鈰銨復鹽(CAN)反應產生的烷基自由基再經單電子氧化可以生成烷基陽離子((合成方案 14)。很明顯此反應過程中的PINO是由NHPI和CAN反應而生成。在這些條件下,過去在苯甲基位置上發生里特反應比較困難,如今采用本合成方法里特反應變得尤為簡單35)。
7.5 NHPI作為極性逆轉催化劑
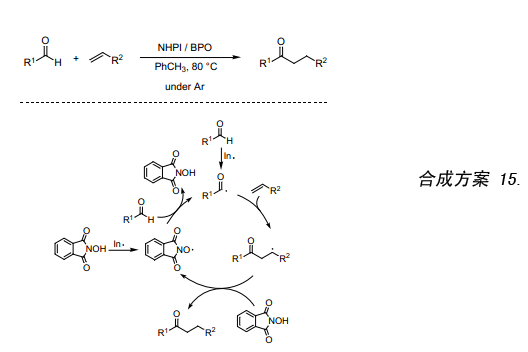
在氬氣氣氛下,催化量的NHPI ,甲苯作溶劑,BPO引發醛跟烯烴反應生成高產率的相應酮。如(合成方案15)顯示的該反應過程類似自由基反應,NHPI做極性逆轉催化劑36)。通過將酰基自由基加成到烯烴上生成一個加成自由基,而加成自由基具有親核性以至于其取代NHPI上的H原子比取代醛上的容易,從而使鏈反應更加平穩的進行。
8. 基于生成催化碳自由基的C-C鍵形成反應
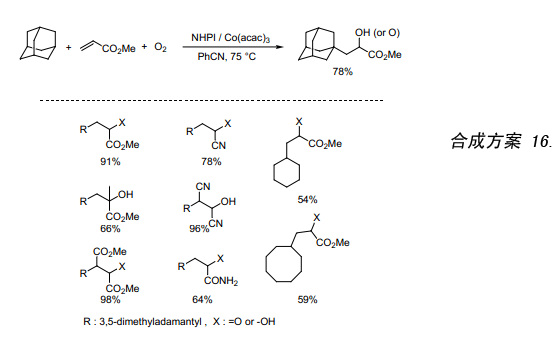
在有機合成中自由基偶合反應是形成C-C鍵的非常有用的方法。我們已發現有可能采用NHPI/O2體系催化烷烴生成相應的烷基自由基。因此,我們利用烯烴來捕獲產生的自由基,我們測試了NHPI/O2催化烷烴與α,β-不飽和酯的反應。在空氣氣氛下,NHPI/Co(acac)3作催化劑催化金剛烷跟丙烯酸甲酯反應。發現獲得了高產率帶有分子氧的三元耦合產物,隨后金剛烷基自由基加成到丙烯酸甲酯的雙鍵上(合成方案 16)37)。本反應被認為是烷烴的烷氧基化反應且一種新的自由基偶合反應,反應中氧原子的引入與C-C鍵的形成同時進行。
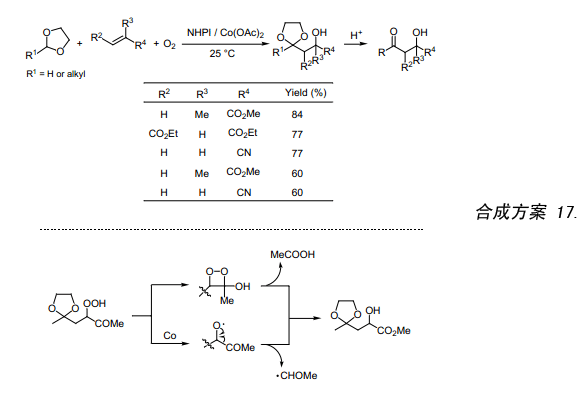
NHPI/O2催化1,3—二氧戊環與丙烯酸甲酯反應,該反應在室溫下就能順利的進行并生成相應的β-羥基縮醛(合成方案 17)。耦合產物上的縮醛經酸處理后很容易轉變成相應的酮。此反應是與烯烴加成類似的酰基自由基加成反應,也對烯烴氧化烷基化反應至關重要38)。
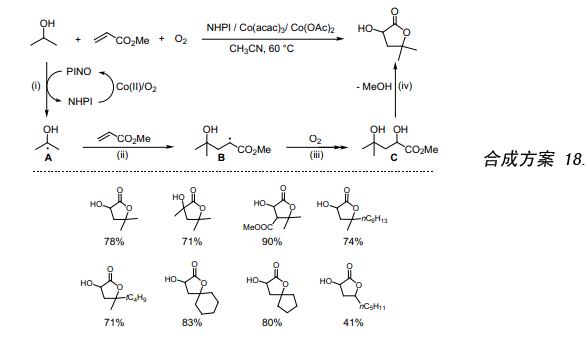
如上所示,NHPI/O2還可以催化醇生成α-羥基碳自由基。因此,嘗試用α,β-不飽和酯捕獲所生成的α-羥基碳自由基并發現能夠合成α-羥基-γ-內酯,在過去α-羥基-γ-內酯用其他合成方法很難得到。在催化量的NHPI和Co鹽存在條件下,異丙醇與丙烯酸甲酯反應生成α-羥基-γ,γ-二甲基-γ-丁內酯(合成方案 18)。在本反應中,(i)經NHPI/Co(Ⅱ)催化在氧存在情況下,醇上的氫原子被取代生成α-羥基碳自由基(A),(ii)A加成到丙烯酸甲酯上生成B,(iii)然后把氧原子引入生成二醇C,(iv)C發生分子內環化作用生成內酯。
參考文獻
1. (a) Curran, D. P. Comprehensive Organic Synthesis; Trost, B.; Fleming, I. M., Eds.; Pergamon, 1991; Vol. 4, Chapters 4.1 and 4.2 (b) Ryu, I.; Sonoda, N.; Curran, D. P. Chem. Rev. 1996, 96, 172. (c) Renaud, P.; Sibi, M. P. Radicals in Organic Synthesis; Wiley-VCH, 2001; Vol. 1, Basic principles, and Vol. 2, Applications.
2. (a) Sheldon, R. A.; Kochi, J. K. Metal-Catalyzed Oxidations of Organic Compounds; Academic Press, 1981. (b) Hill, C. L. Activation and Functionalization of Alkanes; Academic Press, 1989. (c) The Activation of Dioxygen and Homogeneous Catalytic Oxidation; Barton, D. H. R.; Martell, A. E.; Sawyer, D. T., Eds.; Plenum Press, 1993.
3. (a) Ishii, Y.; Sakaguchi, S.; Iwahama, T. Adv. Synth. Catal. 2001, 343, 393. (b) Ishii, Y. Yuki Gosei Kagaku Kyokaishi (J. Synth. Org. Chem. Jpn) 2000, 59, 1. (c) Ishii, Y.; Sakaguchi, S.; Iwahama, T. Yuki Gosei Kagaku Kyokaishi (J. Synth. Org. Chem. Jpn) 1999, 57, 24.
4. Grochowski, E.; Boleslawska, T.; Jurczak, J. Synthesis 1977, 718.
5. Masui, M.; Ueshima, T.; Ozaki, S. Chem. Commun. 1983, 479.
6. (a) Davis, D. D. Ullman’s Encyclopedia of Industrial Chemistry, 5th ed.; Gerhartz, W., Ed.; John Wiley and Sons: New York, 1985; Vol. A1, pp 270-272. (b) Sato, K.; Aoki, M.; Noyori, R. Science 1998, 281, 1646.
7. (a) Ishii, Y.; Iwahama, T.; Sakaguchi, S.; Nakayama, K.; Nishiyama, Y. J. Org. Chem. 1996, 61, 4520. (b) Iwahama, T.; Shoujo, K.; Sakaguchi, S.; Ishii, Y. Org. Process Res. Dev. 1998, 2, 255.
8. Sawatari, N.; Yokota, T.; Sakaguchi, S.; Ishii, Y. J. Org. Chem. 2001, 66, 7889.
9. Ishii, Y.; Kato, S.; Iwahama, T.; Sakaguchi, S. Tetrahedron Lett. 1996, 37, 4993.
10. Winlker, D. E.; Hearne, G. W. Ind. Eng. Chem. 1961, 53, 655.
11. Sakaguchi, S.; Kato, S.; Iwahama, T.; Ishii, Y. Bull. Chem. Soc. Jpn. 1998, 71, 1237.
12. Parshall, G. W.; Ittel, S. D. Homogeous Catalysis, 2nd ed.; John Wiley and Sons: New York, 1992; pp 255-261.
13. Yoshino, Y.; Hayashi, Y.; Iwahama, T.; Sakaguchi, S.; Ishii, Y. J. Org. Chem. 1997, 62, 6810.
14. Tashiro, Y.; Iwahama, T.; Sakaguchi, S.; Ishii, Y. Adv. Synth. Catal. 2001, 343, 220.
15. (a) Davis, D. D. Ullman’s Encyclopedia of Industrial Chemistry, 5th ed.; Gerhartz, W., Ed.; John Wiley and Sons: New York, 1985; Vol. A27, p 587. (b) Mukhopadhyay, S.; Chandalia, S. B. Org. Process Res. Dev. 1999, 3, 455.
16. (a) Shibamoto, A.; Sakaguchi, S.; Ishii, Y. Org. Process Res. Dev. 2000, 4, 505. (b) Sakaguchi, S.; Shibamoto, A.; Ishii, Y. Chem. Commun. 2002, 180.
17. Fukuda, O.; Sakaguchi, S.; Ishii, Y. Adv. Synth. Catal. 2001, 343, 809.
18. Kitabatake, M.; Ishioka, R. Yuki Kasankabutsu: Sono kagaku to kogyoteki riyou (Organic peroxide: chemistry and industrial application); Kagaku Kogyo Sya: Tokyo, 1972.
19. (a) Iwahama, T.; Sakaguchi, S.; Nishiyama, Y.; Ishii, Y. Tetrahedron Lett. 1995, 36, 6923. (b) Iwahama, T.; Yoshino, Y.; Keitoku, T.; Sakaguchi, S.; Ishii, Y. J. Org. Chem. 2000, 65, 6502.
20. Iwahama, T.; Sakaguchi, S.; Ishii, Y. Chem. Commun. 1999, 727.
21. Mukaiyama, T.; Takai, T.; Yamada, T.; Rhode, O. Chem. Lett. 1990, 1661.
22. Iwahama, T.; Sakaguchi, S.; Ishii, Y. Org. Process Res. Dev. 2000, 4, 94.
23. Golden, D. M. Ann. Rev. Phys. Chem. 1982, 33, 493.
24. Sakaguchi, S.; Takase, T.; Iwahama, T.; Ishii, Y. Chem. Commun. 1998, 2037.
25. Chabaud, B.; Sharpless, K. B. J. Org. Chem. 1979, 44, 4202.
26. Fukuda, O.; Iwahama, T.; Sakaguchi, S.; Ishii, Y. Tetrahedron Lett. 2001, 42, 3479.
27. Kato, S.; Iwahama, T.; Sakaguchi, S.; Ishii, Y. J. Org. Chem. 1998, 63, 222.
28. (a) Barton, D. H. R.; Doller, D. Acc. Chem. Res. 1992, 25, 504. (b) Arndtsen, B. A.; Bergman, R. G.; Mobley, T. A.; Peterson, T. H. Acc. Chem. Res. 1995, 28, 154.
29. Markofsky, S. B. Ullmann’s Encyclopedia Industrial Organic Chemicals; Wiley-VCH: Weinheim, 1999; Vol. 6, p 3487.
30. Sakaguchi, S.; Nishiwaki, Y.; Kitamura, T.; Ishii, Y. Angew. Chem. Int. Ed. Engl. 2001, 40, 222.
31. Isozaki, S.; Nishiwaki, Y.; Sakaguchi, S.; Ishii, Y. Chem. Commun. 2001, 1352.
32. Ishii, Y.; Matsunaka, K.; Sakaguchi, S. J. Am. Chem. Soc. 2000, 122, 7390.
33. (a) Sakaguchi, S; Eikawa, M.; Ishii, Y. Tetrahedron Lett. 1997, 38, 7075. (b) Eikawa, M.; Sakaguchi, S.; Ishii, Y. J. Org. Chem. 1999, 64, 4676.
34. Bill, J. C.; Tarbell, D. S. Organic Syntheses, Collect. Vol. IV; Wiley, 1963; p 807.
35. Sakaguchi, S.; Hirabayashi, T.; Ishii, Y. Chem. Commun. 2002, 516.
36. Tsujimoto, S.; Iwahama, T.; Sakaguchi, S.; Ishii, Y. Chem. Commun. 2001, 2352.
37. Hara, T.; Iwahama, T.; Sakaguchi, S.; Ishii, Y. J. Org. Chem. 2001, 66, 6425.
38. Hirano, K.; Iwahama, T.; Sakaguchi, S.; Ishii, Y. Chem. Commun. 2000, 2457.
39. Iwahama, T.; Sakaguchi, S.; Ishii, Y. Chem. Commun. 2000, 613.
注:本文為提供者翻譯的,由于知識所限,其中錯誤在所難免,敬請原諒。如有問題可以查找原文。
統計數據
共收錄化學品數據
147579 條



 滬公網安備 31010602001115號
滬公網安備 31010602001115號