綠色化學(xué)之離子液體-有用的反應(yīng)溶劑
- 2012-03-31
- 專題
近年來,從綠色化學(xué)的角度出發(fā),更多研發(fā)人員投入到環(huán)境友好反應(yīng)的過程研究中。例如,空氣中的氧化反應(yīng),水、超臨界流體和氟溶劑中的反應(yīng)。最近,離子液體作為有機合成的綠色反應(yīng)溶劑引起很多關(guān)注。
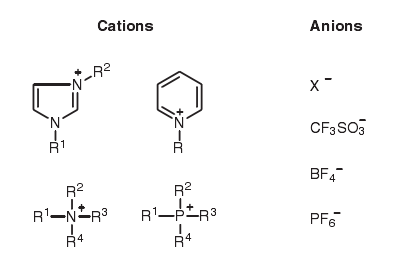
如上圖所示,離子液體是鹽類,由陽離子和陰離子構(gòu)成,陽離子如咪唑鎓、吡啶鎓、季銨基和季磷基,陰離子如鹵素離子、三氟甲磺酸根、四氟硼酸根和六氟磷酸根,在相對低溫下離子液體以液體狀態(tài)存在。他們的顯著特征包括幾乎無蒸氣壓、不易燃、不可燃、高熱穩(wěn)定性、相對低的粘度、作為液體較寬的可操作溫度范圍和高離子導(dǎo)電性。當離子液體用作反應(yīng)溶劑時,溶質(zhì)僅僅被離子溶解,這樣與以水或普通有機溶劑相比,反應(yīng)在完全不同的情況下進行。因此,離子液體被期望呈現(xiàn)非傳統(tǒng)的反應(yīng)性,而且在各種有機反應(yīng)中的應(yīng)用不斷被發(fā)掘。
包含氯鋁酸根陰離子的離子液體已經(jīng)被研究多年。這些離子液體不僅僅用作反應(yīng)溶劑,當陰陽離子的比例改變時,它們還表現(xiàn)出路易斯酸或路易斯堿的性質(zhì)。然而,因為對濕度的高靈敏性,他們只能在惰性氣體或者真空中反應(yīng)。另一方面,研究人員發(fā)現(xiàn)含有如六氟磷酸根陰離子的離子液體能在空氣中形成穩(wěn)定的鹽類,這樣引導(dǎo)了今天大量穩(wěn)定的離子液體的合成。而且,一些離子液體在水和極性有機溶劑中溶解度很小,利用這個特性,離子液體可以在有機溶劑萃取產(chǎn)物后回收利用。傳統(tǒng)溶劑很少被重復(fù)利用,這樣可以減少傳統(tǒng)溶劑的浪費。另外,離子液體作為安全溶劑,由于其低揮發(fā)性得到很多關(guān)注。
下面是一些離子液體的應(yīng)用示例:
1. Diels-Alder反應(yīng)
環(huán)戊二稀和丙烯酸甲醋的Diels-Alder反應(yīng)已見報道。在該反應(yīng)中使用1-乙基-3-甲基咪唑氯化物/氯鋁酸鹽[emimCl/(AICI3)x],內(nèi)/外型產(chǎn)物比隨著emimCl/(AICI3)x比率的變化而變化很大。相比堿性emimCl/(AICI3)x,使用酸性emimCl/(AICI3)x時內(nèi)型數(shù)量增加4倍。1a)當1-丁基-3-甲基甲基咪唑鎓四氟硼酸鹽(bmimBF4)進行相同反應(yīng)時,它表現(xiàn)了與路易斯堿emimCl/(AICI3)x相似的反應(yīng)性。1b)
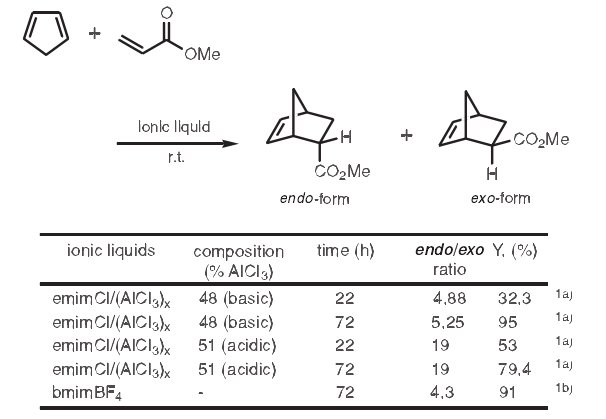
2. Heck反應(yīng)
Heck反應(yīng)中用到鈀類催化劑,極性溶劑如DMF和乙睛,基質(zhì)通常為芳基碘化物。如果使用價格較便宜但反應(yīng)性較低的芳基溴化物或氯化物,必須使用更多的活性催化劑或者添加磷配體來保持催化劑的活性。用1-丁基-3-甲基咪唑鎓溴化物(bmimBr)作溶劑,在不添加磷配體的情況下,芳基溴化物和苯乙烯反應(yīng)得到高產(chǎn)量的芪類化合物。2a)

具有給電子基團的烯醇醚與芳基鹵化物反應(yīng),在正常Heck反應(yīng)條件下,生成α-取代和β取代的混和物。然而,當使用bmimBF4作溶劑,乙烯醚和芳基鹵化物反應(yīng)只特定生成α-取代物。2b)另外,已經(jīng)有報道使用季銨鹽四丁基溴化按(Bu4NBr)的Heck反應(yīng)。2c)
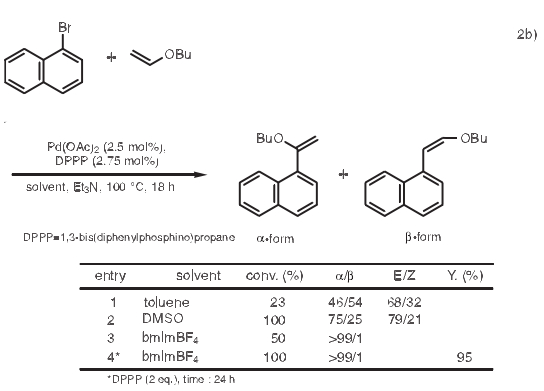
3.羥醛縮合反應(yīng)
使用離子液體的羥醛縮合反應(yīng)已見報道。在反應(yīng)中,為了從丙醛通過兩個羥醛縮合反應(yīng)得到2.4-二甲基-2-庚烯醛3,在羥醛縮合反應(yīng)Ⅰ中,離子液體相中的轉(zhuǎn)化率和水介質(zhì)中的相當。然而,如下表數(shù)值所示,產(chǎn)物的選擇性降低了。這要歸咎于產(chǎn)物1在離子液體中溶解度高而引發(fā)了副反應(yīng)。相反,與水中反應(yīng)相比,在羥醛縮合反應(yīng)Ⅱ中,離子液體相中產(chǎn)物的選擇性增強了。這是因為1的氫化產(chǎn)物在水中難溶而在離子液體中易溶。3)
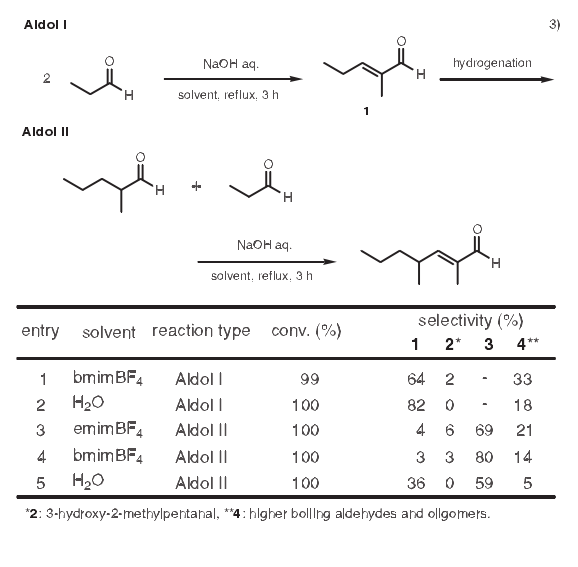
4. Suzuki-Miyaura偶聯(lián)反應(yīng)
Suzuki-Miyaura偶聯(lián)反應(yīng)中,在鈀催化劑和堿存在的條件下,芳基鹵化物和芳基硼酸生成聯(lián)芳基化合物,然而催化劑的去除一直是個難題。在利用離子液體作溶劑的體系中,反應(yīng)完成后產(chǎn)物可以用醚萃取得到,而催化劑仍留在離子液體中,然后離子液體和催化劑可以被重復(fù)利用。4)
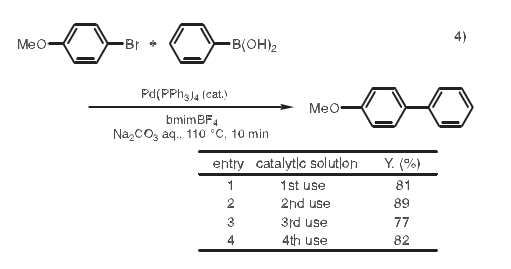
5. Wittig反應(yīng)
Wittig反應(yīng)是一個形成碳碳雙鍵的有用方法。然而,產(chǎn)物和副產(chǎn)物三苯基氧化膦的分離是個經(jīng)典難題。通常利用結(jié)晶或色譜進行分離純化。當利用離子液體作溶劑,反應(yīng)完成后,結(jié)合醚萃取和甲苯萃取,產(chǎn)物和氧化膦很容易被分離。另外,離子液體有可能被有效的重復(fù)利用。5)
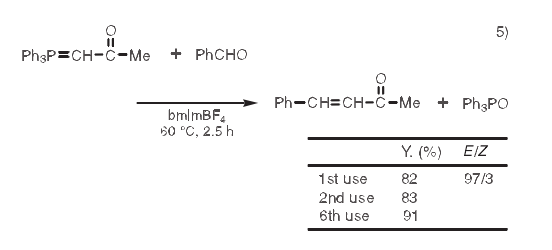
6. Stille反應(yīng)
Stille反應(yīng)是很有用的反應(yīng),在鈀催化劑存在條件下,有機錫化合物和親電試劑反應(yīng),在溫和條件下生成C-C鍵。在離子液體中,乙烯基三丁基錫和碘代環(huán)己烯酮反應(yīng),產(chǎn)物可以用醚萃取,而催化劑留在離子液體中。離子液體和催化劑可以被重復(fù)利用。該離子液體/催化劑相對空氣和潮濕穩(wěn)定,因此可以在長時間儲存后使用而不損失活性。6)
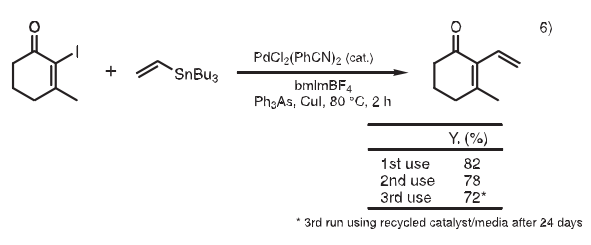
7. Friedel-Crafts反應(yīng)
下面是Friedel-Crafts反應(yīng)的一個例子。在bmimBF4中,三氟甲磺酸銅催化苯甲醚的苯甲酰化反應(yīng),甲氧基二苯甲酮在1h內(nèi)能夠定量得到,其中對位/鄰位產(chǎn)物的比率為96/4。7a)在乙睛中進行同樣的反應(yīng),1h內(nèi)轉(zhuǎn)化率較低,為64%,其中對位/鄰位產(chǎn)物的比率為93/7。另外,利用emimCl/(AICI3)x,吲哚類的區(qū)域選擇性酰化也已見報道。
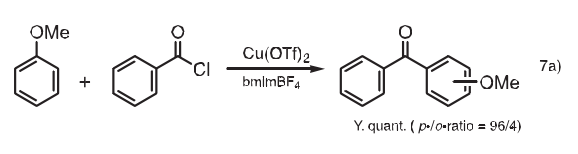
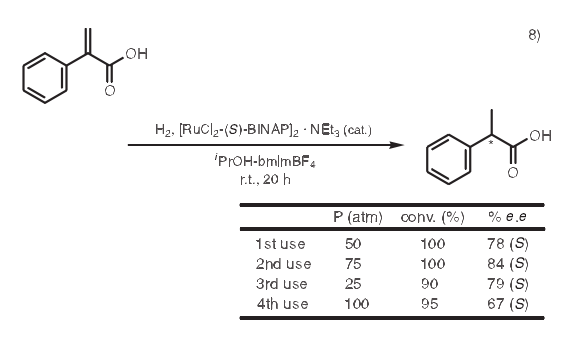
8.加氫作用
在使用均相手性過渡金屬絡(luò)合物的碳碳雙鍵不對稱加氫作用中,催化劑的回收率和產(chǎn)物的分離經(jīng)常讓人困擾。8) Dupont等曾經(jīng)報道過一個例子,其中試劑可以在離子液體和醇的兩相體系中反應(yīng)。反應(yīng)進行完全后,產(chǎn)物留在醇相,而催化劑留在離子液體相中。因此產(chǎn)物和催化劑可以很容易通過傾析分離。另外,留在離子液體中的催化劑可以被重復(fù)利用而不損失活性。
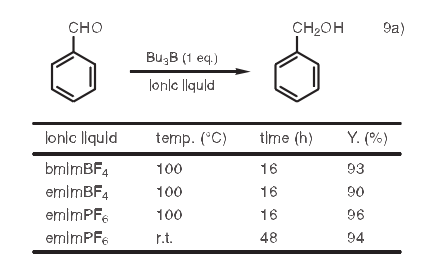
9.還原反應(yīng)
利用三烷基硼烷的醛還原反應(yīng)是一個重要的有機轉(zhuǎn)化反應(yīng)。然而,使用簡單的三烷基硼烷的還原反應(yīng)一般需要150℃以上的反應(yīng)溫度。Kaballa等曾經(jīng)報道了這種還原反應(yīng),利用bmimBF4, emimBF4、和1-乙基-3-甲基咪唑鎓六氟磷酸鹽(emimPF6)作溶劑。9a)例如,當苯甲醛在emimPF6中被三丁基硼烷還原時,反應(yīng)在100℃時進行很快,并且產(chǎn)量很高。產(chǎn)物在室溫下也可以得到,盡管相對而言需要較長的反應(yīng)時間。另外,利用離子液體的光致還原反應(yīng)也已見報道。9b)
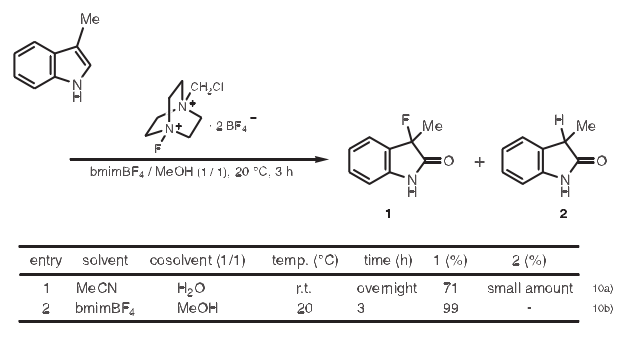
10.氟化反應(yīng)
在雜環(huán)化合物中引進氟在生物活性化合物的合成中很重要。利用N-氟-N'-(氯甲基)三乙烯二胺雙(四氟硼酸鹽)作氟化試劑,bmimBF4作溶劑,發(fā)生吲哚類的親電氟化反應(yīng),與傳統(tǒng)方法(下表行1)相比,在較短時間內(nèi)可以得到高產(chǎn)量的3-氟-2氧代吲哚類化合物。
11.開環(huán)反應(yīng)
β-氨基醇可以用作生物活性化合物的合成中的有用砌塊。有一種合成方法是利用胺類使環(huán)氧化物開環(huán)。然而,這些反應(yīng)在較高溫度下需要用到大量過量的胺類。高溫反應(yīng)條件不僅會破壞某些功能團,而且還不利于控制區(qū)域選擇性。隨后發(fā)展了多種催化劑或助催化劑如金屬氨基化合物、金屬三氟甲磺酸鹽和過渡金屬鹵化物。然而,因為它們大部分價格昂貴或者需要化學(xué)計量的量,從而限制了它們的實用性。在利用離子液體的體系中,反應(yīng)在室溫下進行,可以高產(chǎn)量的得到β-氨基醇。11)
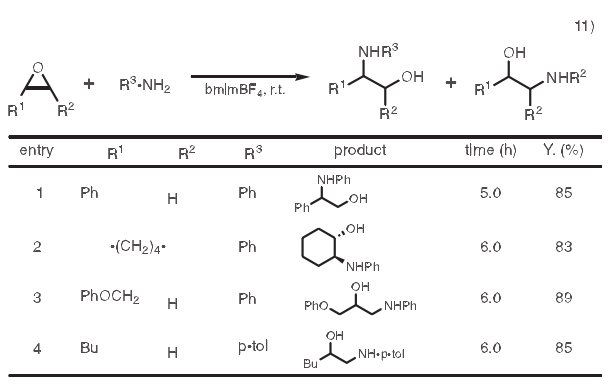
上表行3,4中縮水甘油醚或烷基環(huán)氧乙烷為例,胺類攻擊環(huán)氧化物上空間位阻較小的位點。反應(yīng)后,產(chǎn)物用醚萃取,接著在80℃下減壓干燥。離子液體可以被重復(fù)利用五次而不損失活性。
12.酶反應(yīng)
利用離子液體的酶反應(yīng)已見報道。12)眾所周知,脂肪酶可以在非天然的反應(yīng)條件下保持活性,在有機溶劑中的反應(yīng)已被大量使用。例如,有機溶劑中的醋基交換反應(yīng)是一種制備光學(xué)活性化合物的很有用的合成方法。在利用離子液體的烯丙醇的不對稱醋基交換反應(yīng)中,目標產(chǎn)物的產(chǎn)率和在有機溶劑體系中得到的相近。12a)

如上所述,多種利用離子液體的反應(yīng)已被使用,提高產(chǎn)率和回收率的改進方法和溶劑的循環(huán)利用已見報道。此外,他們也被報道在烴化13)、烯丙基化14)、環(huán)氧化15)、環(huán)加成16)、氫化醋化17)和使用超臨界CO2的反應(yīng)18)中有效。
13.其他應(yīng)用
離子液體在電化學(xué)中的應(yīng)用也引發(fā)了關(guān)注,因為它們僅僅由離子構(gòu)成,而且具有高的離子導(dǎo)電性。例如,它們作為二次電池電解質(zhì)得到廣泛研究。這些電解質(zhì)需要具有如下特性:高離子導(dǎo)電性,不易揮發(fā)性,熱穩(wěn)定性,不燃性以及無腐蝕性。離子液體正好滿足這些要求。此外,1-烷基-3-甲基咪唑鎓碘化物近期被研究作為染色敏化太陽能電池的一種電解質(zhì)。19)
最近,Hamaguchi等在報告中指出1-丁基-3-甲基-咪唑鎓四氯高鐵酸鹽是具有磁性的離子液體。20)傳統(tǒng)的磁性液體在揮發(fā)性和相分離問題上是個難題。這種新的磁性離子液體正好解決了這些問題,被期望用在多種領(lǐng)域,包括用作電機軸的密封劑。
References
1) a) C. W. Lee, Tetrahedron Lett. 1999, 40, 2461; b) T. Fischer, A. Sethi,T. Welton, J. Woolf, Tetrahedron Lett. 1999, 40, 793.
2) a) L. Xu, W. Chen, J. Xiao, Organometallics 2000, 19, 1123; b) L. Xu,W.Chen, J. Ross, J. Xiao, Org. Lett. 2001, 3, 295; c) V. P.W.Bohm,W.A. Herrmann, Chem. Eur. J. 2000, 6, 1017.
3) C. P. Mehnert, N. C. Dispenziere, R. A. Cook, Chem. Commun. 2002,1610.
4) C. J. Mathews, P. J. 5m ith, T. Welton, Chem. Commun. 2000, 1249.
S) V. L. Boulaire, R. Gree, Chem. Commun. 2000, 2195.
6) S. T. Handy, X. Zhang, Org. Lett. 2001, 3, 233.
7) a) J. Ross, J. Xiao, Green Chem. 2002, 4, 129; b) K.-S. Yeung, M. E.Farkas, Z. Qiu, Z. Yang, Tetrahedron Lett. 2002, 43, 5793; c) A. Stark,B. L. MacLean, R. D. Singer,J. Chem. Soc., Dalton Trans. 1999, 63; d)C. J. Adams, M. J. Earle, G. Roberts, K. R. Seddon, Chem. Commun.1998, 2097.
8) A. L. Monteiro, F. K. Zinn, R. F. de Souza, J. Dupont, Tetrahedron:Asymmetry 1997, 8, 177.
9) G. W. Kabalka, R. R. Malladi, Chem. Commun. 2000, 2191; b) J. L. Reynolds, K. R. Erdner, P. B. Jones, Org. Lett. 2002, 4, 917.
10) a) Y. Takeuch i, T. Taru i, N. Shibata, Org. Lett. 2000, 2, 639; b) J.Baudoux, A.-F. Salit, D. Cahard, J.-C. Plaquevent, Tetrahedron Lett.2002, 43, 6573.
11) J. S. Yadav, B. V. S. Reddy, A. K. Basak, A. V. Narsaiah, TetrahedronLett. 2003, 44, 1047.
12) a) T. Itoh, E. Akasaki, K. Kudo, S. Shirakami, Chem. Lett. 2001, 262;b) R. M. Lau, F. van Rantwijk, K. R. Seddon, R. A. Sheldon, Org. Lett.2000, 2, 4189; c) S. Park, R. J. Kazlauskas, J. Org. Chem. 2001, 668395; d) T. Itoh, S.-h. Han, Y. Matsushita, S. Hayase, Green Chem.2004, 6, 437; e)T.Ito, Vuki Gosei Kagaku Kyokaishi (J. Synth. Org.Chem. Jpn.) 2009, 67, 143.
13) M. Badri, J.-J. Brunet, Tetrahedron Lett. 1992, 33, 4435.
14) C. M. Gordon, A. McCluskey, Chem. Commun. 1999, 1431.
15) G. S. Owens, M. M. Abu-Omar, Chem. Commun. 2000, 1165.
16) a) J. Peng, Y. Deng, New J. Chem. 2001, 25, 639; b) J. F. Dubreuil, J.P. Bazureau, Tetrahedron Lett. 2000, 41, 7351.
17) a) K. Qiao, Y. Deng, New J. Chem. 2002, 26, 667; b) D. Zim, R. F. deSouza, J. Dupont, A. L. Monteiro,Tetrahedron Lett. 1998, 39, 7071.
18) S. V. Dryuba, R. A. Bartsch, Angew. Chem. Int. Ed. 2003, 42, 148.
19) a) P. Bonhote, A.-P. Dias, N. Papageorgiou, K. Kalyanasundaram, M.Gratzel, Inorg. Chem. 1996, 35, 1 168.
20) a) S. Hayashi, H. Hamaguchi, Chem. Lett. 2004, 33, 1590; b)H.Hamaguch i, Expected Materials for the Future (Mirai Zairyo) 2005, 5,29
Reviews
21) a) T. Welton, Chem. Rev. 1999, 99, 2071; b) J. D. Holbrey, K. R. Seddon, Clean Prod. Proc. 1999, 1, 223; c) P. Wasserscheid, W. Keim, Angew. Chem. Int. Ed. 2000, 39, 3772;
d) R. Sheldon, Chem. Commun. 2001, 2399; e) D. Zhao, M. Wu, Y. Kou, E. Min, Catal. Today 2002,74, 157.
注:本文為提供者翻譯的,由于知識所限,其中錯誤在所難免,敬請原諒。如有問題可以查找原文
統(tǒng)計數(shù)據(jù)
共收錄化學(xué)品數(shù)據(jù)
147579 條



 滬公網(wǎng)安備 31010602001115號
滬公網(wǎng)安備 31010602001115號