從不對稱催化劑到不對稱自催化劑
- 2012-03-14
- 專題
1、介紹:
眾所周知,多數生理活性物質都是由不對稱碳原子組成的手性分子。隨著不對稱合成工藝的發展,如何進行預期的絕對構型對映體的選擇性合成是有機合成專家面對的一個重要課題。特別是,以不對稱催化劑的催化作用為基礎的不對稱合成更是一個活躍的研究領域。包括作者在內的多數研究小組的研究表明,在二烷基鋅與醛的不對稱烷 基化的過程中,利用手性氨基醇作為不對稱催化劑,已成為光學活性仲醇領域中的主流反應 1) 。利用脯氨酸衍生的手性氨基醇、N,N-雙烷基去甲麻黃堿的衍生物或手性哌嗪作為不對稱催化劑,作者開發了一種具有高對映體選擇性的醛的不對稱烷基化工藝。在這個反應中,還可以得到高收率的通用底物和許多有用的中間體。
通過精確的分子結構設計形成一個新功能的物質也是十分有趣的。此前,還沒有已知的手性分子可做為具有自我復制能力的不對稱自催化劑。我們發現手性嘧啶和喹啉醇是具有高對映體選擇性的不對稱自催化劑,不但有自我增值的能力,而且有很好的光學純度2)。
本文我們將介紹我們在醛類的不對稱催化劑和不對稱自催化劑方面的研究結果。
2、利用手性氨基醇進行醛的不對稱烷基化
1)、利用二苯基(1-甲基-吡咯-2-基)甲醇(1,DPMPM)進行醛的不對稱烷基化。
我們已經研究了利用脯氨酸及其衍生物制備的手性氨基醇(DPMPM)對二烷基鋅進行的不對稱烷基化3)4) 。結果在芳香醛的不對稱加成反應中,相應的光學活性仲醇具有極高的光學純度。利用DPMPM的鋰醇提供的高對映體選擇性進行的不對稱乙基化,得到了幾乎完全光學純度的1-苯基-1-丙醇。通過對不對稱催化劑絕對構型的選擇,產品的S-和R-構型能夠被分別制備出來。也就是說,利用(S)-(+)-DPMPM和(R)-(-)-DPMPM可以分別得到S-和R-構型的醇類。
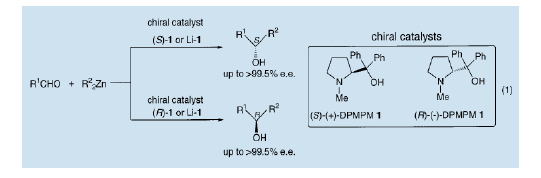
2)、利用N,N--雙烷基去甲麻黃堿進行醛的不對稱烷基化。
手性氨基醇,N,N-雙烷基去甲麻黃堿,對醛的不對稱烷基化也是一個有用的不對稱催化劑5) 。一般來說,與芳香醛相比,脂肪醛的不對稱烷基化很難得到高收率。我們發現N,N-雙烷基去甲麻黃堿無論對脂肪醛還是芳香醛都是一個對映體選擇性很高的催化劑。根據烷基取代基上的氮原子的結構不同,N,N-雙烷基去甲麻黃堿也表現出不同對映體選擇性。例如,在雙烷基鋅進行的脂肪醛的不對稱乙基化中,N,N-雙烷基去甲麻黃堿(2,DBNE)表現出很高的對映體選擇性(e.e值為93%)5a)。在二異丙基或二丁酯鋅進行的不對稱烷基化中使用N,N-雙烷基去甲麻黃堿也能表現出高選擇性6)。此外,1-苯基-2-吡咯烷基-1-丙醇(3)和N,N-二烯丙基去甲麻黃堿(4)也是有用的不對稱催化劑5b)。
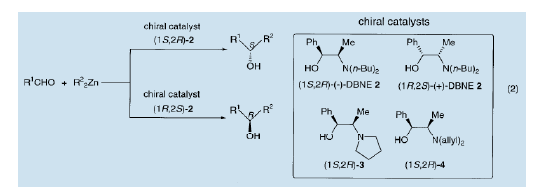
3)、二乙基鋅的對映選擇加成到一個帶官能團的醛。
利用手性氨基醇1和2可以實現各種醛的不對稱烷基化(方案1)。例如,以炔醛為基板產生一個手性丙炔醇(5)7a)。當使用氘代和含氟醛時,可以分別得到大量的具有光學活性的重氫取代(6)7b) 和含氟醇(7)7c)。通過雙烷基鋅對醛的化學和對映選擇性加成,酮醛可產生手性醇酮(8)7d)。對羰基烯酮的不對稱加成,產生大量的不對稱烯丙醇(9)4b,7e)。此外,手性羥醛(10)7f) 和雜環醇(11)7g)也可以被不對稱地制備出來。具有高對映選擇性和立體選擇性的雙醛加成工藝,產生高光學純度的二醇(12)7h) 。同時帶有酯基和醛基的化合物的烷基化會導致一個羥基酯的產生。該羥基酯可轉化為類似于手性內酯那樣的手性酯類(13)7i)。手性酞,芹菜中的一個成份,可以通過醛的不對稱烷基化,從鹵化苯甲醛得到,鹵化基轉換為酯基,并且由此產生羥基酯之后的內酯7j)。
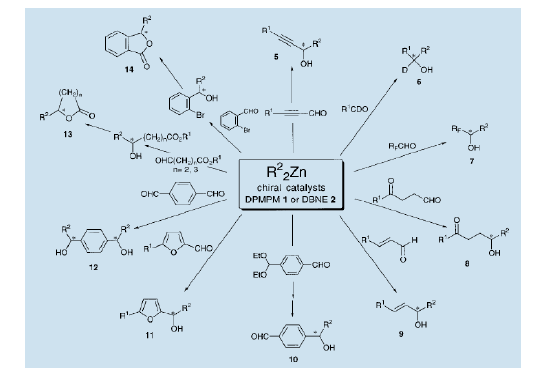
氨基醇(1R,2S)-3做為不對稱配體已成為通過酮的不對稱烷基化合成HIV逆轉錄酶抑制劑的關健一步8)。
4)、利用硫代磷酰胺進行的不對稱烷基化
在不對稱反應中利用手性硫代磷酰胺的例子是極少的。研究表明,醛的不對稱烷基化可以在四異丙基鈦存在時,以硫代磷酰胺(15,PHONE)作為催化劑來實現9)。這一反應是在低溫下(-45℃)進行的,可以得到高產率的不對稱光學活性的仲醇。這個催化劑也可以用于通過雙環丙基鋅進行的醛的不對稱環丙烷化,來生產光學純度接近97%(e.e.)的光學活性的環丙醇10)。
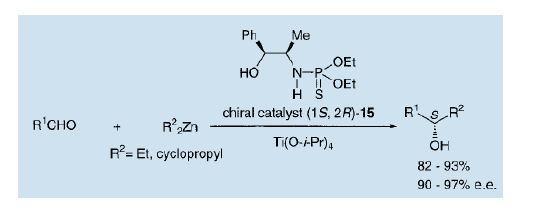
3、不對稱自催化劑
通過對吡啶-3-甲醛反應的觀察,以確定用氨基醇1和2為催化劑的不對稱烷基化一般性的規律。作者發現,反應速度要高于其他醛(反應時間:約3個小時,苯甲醛反應時間:約20小時)11) 。這表明,通過反應產生的化合物具有不對稱自催化劑的功能。
在傳統的不對稱催化中,不對稱催化劑C和產品D的結構一般是完全不同的。但在不對稱自催化中,不對稱催化劑C的結構和絕對構型與產品C完全相同。
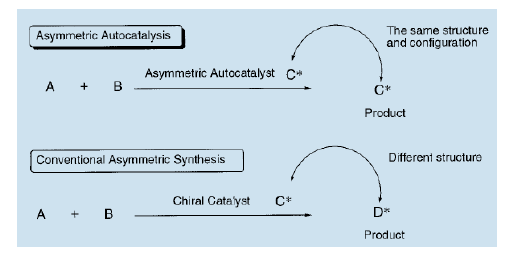
不對稱自催化擁有以下三大優勢:
i)、反應效率高。在不對稱自催化中,反應體系中的不對稱催化劑收益隨著反應的進行而增加。因此,反應效率非常高,反應能迅速完成。
ii)、反應過程簡單。傳統工藝中要求進行的不對稱催化劑與反應產物的分離,在這里是不必要的,因為它們有著相同的結構。
iii )、連續反應具備了可能性。由于產物可以充當不對稱催化劑,因此,在不對稱自催化體系中的催化劑可以反復地得到和補充。微量的催化劑就可以使大量的手性化合物反應得以進行。
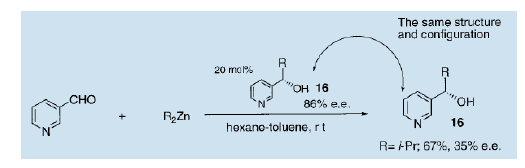
如上所述,與傳統工藝相比較的優勢而言,不對稱自催化很可能成為下一代的節能的不對稱反應。目前還沒有關于不對稱自催化相關的書面實驗報告,雖然Wynberg已經描述了反應的意義12)。1990年,我們首次報導了在3-吡啶醛的烷基化過程中使用一定量的3-吡啶醇作為自催化劑,從而得到結構和絕對構型均相同的3-吡啶醇的自催化反應13)。利用86%(e.e.)的(S)-2-甲基-1-(3-吡啶基)-1-丙醇(16)作為不對稱自催化劑,通過雙異丙醇鋅對3-吡啶甲醛進行的異丙烷化得到了結構和絕對構型與自催化劑完全相同的(S)-3-吡啶醇,收率為67% e.e值為35%。
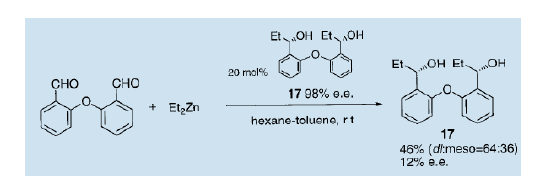
然后,我們合成了一種手性二醇并使用它作為不對稱自催化劑14)。我們發現,這個帶有二苯醚架構的手性二醇(17)在通過雙乙基鋅對相應的二醛進行的不對稱二乙烷化過程中充當不對稱自催化劑, 可以生產e.e值為17的二醇(17)。
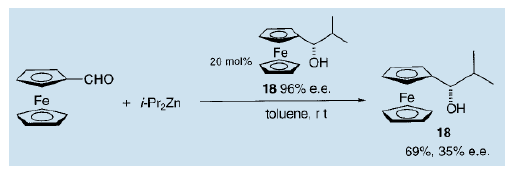
此外,我們還確定了在二茂鐵基醛與二異丙基鋅的反應中,使用手性二茂鐵基醇(18,e.e值為96%)作不對稱自催化劑,也可以得到收率為69%,不對稱量為35%的相同的醇(18)15)
1)、高對映體選擇性不對稱催化劑
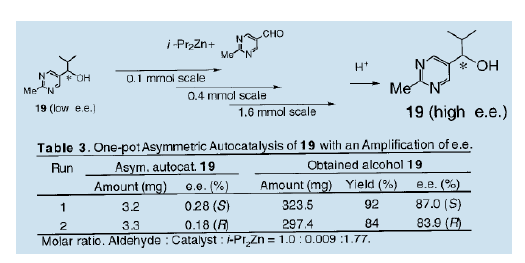
綜上所述,自從我們發表第一個關于不對稱自催化的報告后,不對稱自催化工藝過程的發展得到了關注13)。但是,事實上仍然存在著一個懸而未決的問題,即產品的光學純度還遠低于催化劑的光學純度。我們進一步研究,在考慮到分子對稱性和醛的反應的同時,制備高對映體選擇性的不對稱自催化劑。結果表明,含有兩個氮原子的5-嘧啶醇是一種優良的不對稱自催化劑。我們詳細地考察了反應并發現手性5-嘧啶醇是一種非常有效的不對稱自催化劑。二異丙基鋅與5-嘧啶醇的不對稱異丙基化過程中,可以得到高不對稱量的與自催化劑絕對構型相同的手性5-嘧啶醇(e.e值90%以上) 16)。當(S)-5-嘧啶醇(19, e.e值94%)作為不對稱自催化劑時,新的產品(S)-5-嘧啶醇(19)的光學純度是95.7% ( e.e值),這意謂著該化合物具有自我增值而不會失去其光學活性的功能。當接近完全光學純的嚓咤醇(19)使用后,新產生的化合物(19)光學純度高達98.2% ( e.e值)。
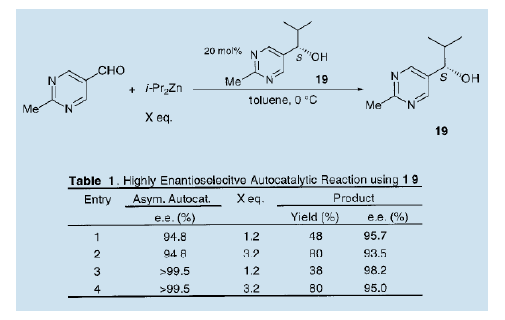
只含有一個氮原子的3-哇琳醇也被證明是非常高效的不對稱自催化劑7)。具體地說,在3-喹啉甲醛的不對稱異丙基化中使用3-喹啉醇(20, e.e值94%)作不對稱自催化劑,可得到高光學純度(e.e值為94%)的哇琳醇(20)

我們還發現,在5位帶有一個甲酞基的3-毗咤醇作為不對稱自催化劑較5位不帶任何官能團的催化效果要好得多18)。不對稱量的大小取決于甲酞基中氮原子上的烷基的性質。當R1是一個異丙基的3-吡啶醇(21)用于催化時,產品的不對稱量約為86% ( e.e值)。
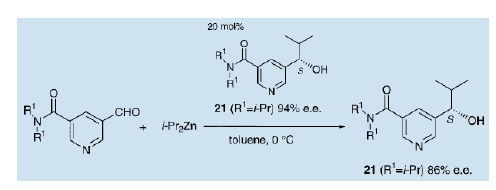
2)、不對稱自催化與光學純度的改善
Kagan等首先報導了不對稱氧化的非線性光學現象,一種產品的光學純度高于使用不對稱催化的現象19a)。Ogunil9b), Noyori等19c)還就醛的不對稱烷基化進行了進一步研究19d)。當然,所有的反應物都不是自催化劑,產品的結構也與不對稱催化劑的不同。雖然可以從e. e值為10%的催化劑中可以得到e.e值為50%的產品,但進一步改善產品的光學純度是不可能的。
另一方面,我們發現pw陡醇是有效的自催化劑。償試連續的不對稱自催化反應,以實現大部分情況下的反應是自催化反應。首先,不對稱自催化反應是利用e.e值僅有2%的(S)嘧啶醇(22)進行的。結果表明,得到的新的嘧啶醇(22)的光學純度(產品和使用的自催化劑的總和)提高至10%(e.e值)。在下一階段的反應中使用10% Ce.e值)的化合物作為不對稱自催化劑進一步提升光學純度,嘧啶醇(22)的e.e值可達到57%。在隨后的不對稱自催化反應中陸續使用獲得的醇,光學純度可進一步提升至81%(e.e值),甚至達到88% (e.e值)20)。起始時略有過量的S構型的醇陸續經過四次反應后,自身擴增了238倍,而R-構型的醇只擴增了16倍。光學純度從2% (e.e值)擴增到88%(e.e值)。
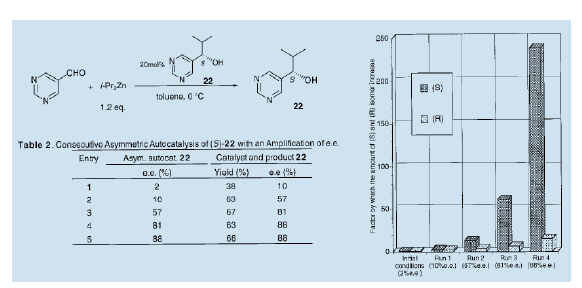
我們假設如下:嘧啶醇(22)鋅是真正的不對稱自催化劑。二異丙基鋅與醛的加成物使不對稱自催化反應得以進行,從而改善了光學純度。反應完成后,反應物酸化調整為高光學活性的嚓咤醇(22)。
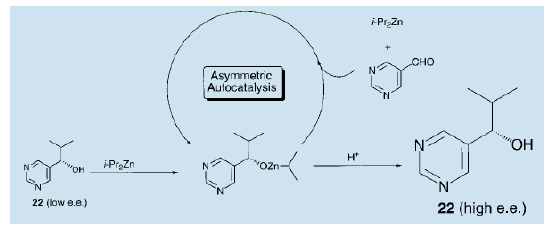
以上反應中,為了孤立嘧啶醇并用于隨后的下一階段反應中,每個反應之后,反應物都要經過酸處理。在每個循環完成之后,償試陸續在一個容器中加入二異丙基鋅和醛,以確保反應不停下來。結果表明,大大提高嘧啶醇的光學純度是切實可行的21)。例如,在二異丙基鋅和醛的反應中,使用低光學純度0.2% ( e.e值)的催化劑,生產的產品接近90% ( e.e值)。
3)、自我復制型不對稱還原
綜上所述,我們發現不對稱自催化發生在少數雙烷基鋅與醛的不對稱烷基化中。那么,這種不對稱來源和產物的構型和結構都相同的“自復制型反應”能否應用于其他反應?
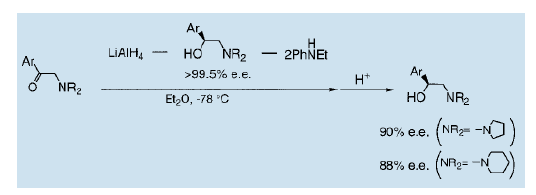
我們發現利用手性氨基醇做為配體對氨基酮進行加氫還原可以得到與那些配體結構和絕對構型完全相同的氨基醇。我們還發現利用氫化鉀鋁對α-氨基酮進行不對稱還原是可能的。非對稱β-氨基醇催化劑和非手性胺配體被用來產生一個與不對稱配體結構和絕對構型完全相同的氨基醇22)。這種反應可能被視為一個自我復制型不對稱還原。特別是在氮原子上帶有一個雜環取代基的氨基醇,甚至更有效,可以將光學純度提升至90% ( e.e值)。
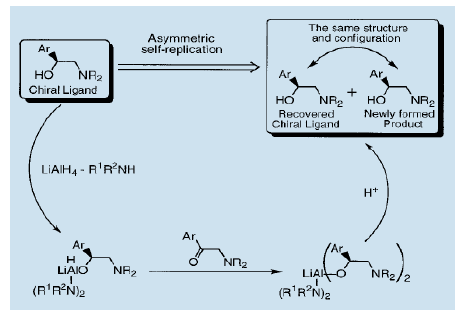
這些被重結晶的氨基醇的光學純度得以提高。圍繞重結晶的自我復制型不對稱反應物建立一個手性氨基醇自我復制的完整循環。許多手性氨基醇,如上述的化合物1和2都可以作為高對映體選擇性催化劑。其他有名的例子是具有藥理和生理活性的化合物。這使得手性氨基醇的自我復制型不對稱反應成為一個有價值的合成工藝。
4、結論
手性氨基醇,如DPMPM (1)和DBNE(2)在醛的不對稱烷基化過程中,充當不對稱催化劑井得到不對稱量很高的具有光學活性的二醇。手性嘧啶、喹啉和吡啶醇作為不對稱的自催化劑,并且是自我增值的不對稱催化。此外,嚓陡醇是微量的敏感的手性不對稱分子23)。這導致光學純度的放大。
估計將來還會有其他的有趣的功能被發現。
參考文獻
1.a)K.Soai,S.Niwa,Chem.Rev.,92,833(1992)
b)R.Noyori,M.Kitamura,Angew.Chem.Int.Ed.Engl.,30,49(1991)
c)K.Soai,T.Hayase,Yuki Gosei Kagaku Kyokaishi (J.Synth.Org.Chem.Jpn.),53,138(1995)
d)Aminoalcohols promote the ethylation of benzaldehyde by diethyl zinc.
T.Mukaiyama,K.Soai,T.Sato,H.Shimizu,K.Suzuki,J.Am.Chem.Soc.,101,1455(1979)
2.K.Soai,T.Shibata,Yuki Gosei Kagaku Kyokaishi(J.Synth.Org.Chem.Jpn.),55,994(1997)
3.a)K.Soai,A.Ookawa,J.Chem.Soc.,Chem.Commun.,1986,412
b)A.Ookawa,K.Soai,J.Chem.Soc.,Perkin Trans.1,1987,1465
4.a)K.Soai,A.Ookawa,K.Ogawa,T.Kaba,J.Chem.Soc.,Chem.Commun.,1987,467
b)K.Soai,A.Ookawa,T.Kaba,K.Ogawa,J.Am.Chem.Soc.,109,7111(1987)
5.a)K.Soai,S.Yokoyama,K.Ebihara,T.Hayasaka,J.Chem.Soc.,Chem.Commun.,1987,1690
b)K.Soai,S.Yokoyama,T.Hayasaka,J.Org.Chem.,56,4264(1991)
6.K.Soai,T.Hayase,K.Takai,T.Sugiyama,J.Org.Chem.,59,7908(1994)
7.a)S.Niwa,K.Soai,J.Chem.Soc.,Perkin Trans.1,1990,937
K.Soai,S.Niwa,Chem.Lett.,1989,481
b)K.Soai,Y.Hirose,S.Sakata,Bull.Chem.Soc.Jpn.,65,1734(1992)
c)K.Soai,Y.Hirose,S.Niwa,J.Fluorine Chem.,59,5(1992)
T.Hayase,T.Sugiyama,M.Suzuki,T.Shibata,K.Soai,J.Fluorine Chem.,84,1(1997)
d)K.Soai,M.Watanabe,M.Koyano,Bull.Chem.Soc.Jpn.,62,2124(1989)
K.Soai,M.Watanabe,M.Koyano,J.Chem.Soc.,Chem.Commun.,1989,534
M.Watanabe,K.Soai,J.Chem.Soc.,Perkin Trans.1,1994,3125
e)K.Soai,Y.Kawase,A.Oshio,J.Chem.Soc.,Perkin Trans.1,1991,1613
f)K.Soai,H.Hori,M.Kawahara,Tetrahedron:Asymmetry,1,769(1990)
g)K.Soai,Y.Kawase,S.Niwa,Heterocycles,29,2219(1989)
h)K.Soai,H.Hori,M.Kawahara,J.Chem.Soc.,Chem.Commun.,1992,106
i)K.Soai,S.Yokoyama,T.Hayasaka,Chem.Lett.,1988,843
j)K.Soai,H.Hori,M.Kawahara,Tetrahedron:Asymmetry,2,253(1991)
8.A.S.Thompson,E.G.Corley,M.F.Huntington,E.J.J.Grabowski,Tetrahedron Lett.,36,8937(1995)
A.S.Thompson,E.G.Corley,M.F.Huntington,E.J.J.Grabowski,J.F.Remenar,D.B.Collum,J.Am.Chem.Soc.,120,2028(1998)
9.K.Soai,Y.Hirose,Y.Ohno,Tetrahedron:Asymmetry,4,1473(1993)
K.Soai,Y.Ohno,Y.Inoue,T.Tsuruoka,Y.Hirose,Rec.Trav.Chim.Pays-Bas,114,145(1995)
10.T.Shibata.H.Tabira.K.Soai.J.Chem.Soc.,Perkin Trans.1,1998,177
11.K.Soai,S.Hori,S.Niwa,Heterocycles,29,2965(1989)
12.H.Wynberg,J.Macromol.Sci.Chem.,Sect.A,26,1033(1989)
13.K.Soai.S.Niwa.H.Hori. J.Chem.Soc.,Chem.Commun.,1990.982
14.K.Soai T.Hayase,C.Shimada,K.Isobe,Tetrahedron:Asymmetry,5,789(1994)
15.K.Soai T.Hayase,K.Takai,Tetrahedron:Asymmetry,6,637(1995)
16.T.Shibata H.Morioka,T.Hayase,K.Choji,K.Soai,J.Am.Chem.Soc.,118,471(1996)
17.T.Shibata K.Choji,H.Morioka,T.Hayase,K.Soai.Chem.Commun.,1996.751
18.T.Shibata H.Morioka,S.Tanji,T.Hayase,Y.Kodaka,K.Soai,Tetrahedron Lett.,37,8783(1996)
19.a)C.Puchot,O.Samuel,E.Dunach,S.Zhao,C.Agami,H.B Kagan,J.Am.Chem.Soc.,108,2353 (1986)
b)N.Oguni,Y.Matsuda,T.Kaneko,J.Am.Chem.Soc.,110,7877(1988)
c)M.Kitamura,S.Okada,S.Suga,R.Noyori,J.Am.Chem.Soc.,111,4028(1989)
d)C.Girard,H.B.Kagan,Angew.Chem.Int.Ed.,37,2922(1998)
20.K.Soai,T.Shibata,H.Morioka,K.Choji,Nature (London),378,767(1995)
注:本文為提供者翻譯的,由于知識所限,其中錯誤在所難免,敬請原諒。如有問題可以查找原文
統計數據
共收錄化學品數據
147579 條



 滬公網安備 31010602001115號
滬公網安備 31010602001115號