近年來基于主鏈骨架等級基礎上的通過誘導和維護螺旋結構的人造螺旋聚合高分子實用性分子設計方法論的研究
- 2013-02-18
- 專題
 1.簡介
1.簡介
1-1.螺旋聚合物的短暫歷史1a,b
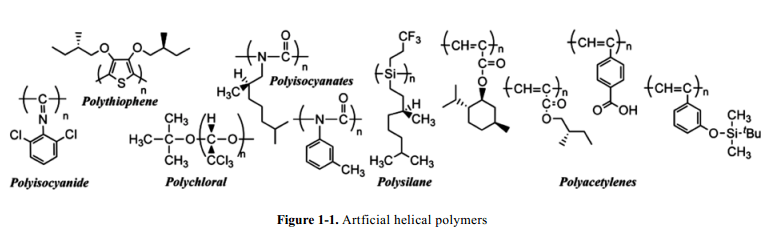
螺旋結構高分子化合物的研究幾乎與聚合物的獨立類型研究,即蛋白質螺旋結構(Pauling, 1951)、DNA雙螺旋結構(Watson, Crick, 1953)以及等規聚丙烯1/3-螺旋結的構澄清開始于同一時間。尤其是,Natta發現了等規聚丙烯具有一個先進的技術,意味著聚合物螺旋結構可以通過良好的合成反應對在聚合物結構設計中立體規則性以及相應的單體的微控人工構造出來。隨后,合成具有龐大的取代基的螺旋聚合物構型被研究出來,從而可以生成了這種聚合物的各種類型例如聚異氰酸酯,2a,b聚異氰化合物,3 聚醛,4聚(烷基異丁烯酸酯),5 聚硅烷,6 聚乙烯,7a-d 聚噻吩8(Fig. 1-1)。這些剛性與半剛性聚合物主鏈可以用來解釋維護聚合物的螺旋構象。
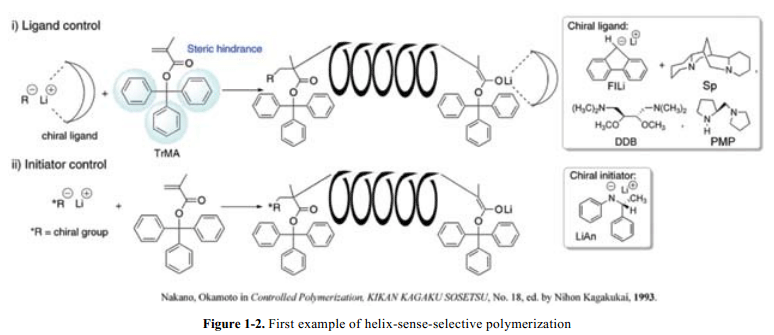
合成螺旋聚合物作為一個顯著的工作,Okamoto和他的伙伴報道了丙烯酸酯的不對稱聚合。5在這個聚合系統里面,螺旋構象的螺旋性質通過由加成聚合物引發劑組成的手性不對稱配合基控制。通常,具有靈活主鏈骨架的聚合物在溶液里面不能夠維持其螺旋構象,因為聚合物主鏈旋轉沒有強大的約束。因此,為了維護聚合物螺旋構象,精確的使用它們的空間位阻現象引入巨大的側鏈可以制作高分子聚合物主鏈。例如,聚(甲基丙烯酸三苯甲酯) 顯示穩定的螺旋構象(Fig. 1-2), 與聚(甲基丙烯酸甲酯)在溶解態中的無規則的卷曲狀形成鮮明的對比。在一個自然的結果中,聚合物主鏈繞線方向的測定意味著聚合物螺旋構象螺旋意義的確定。由乙烯基單體制得的合成高分子具有sp3-碳循環序列組成的聚合物主鏈。因此這種類型的螺旋聚合物,他們沒有有效的需要足夠的范德華力的互相間作用的官能團來維持螺旋構象。相反的,生物聚合物例如多肽就通過氫鍵和范德華力共同引導和維持其螺旋構象。尤其是,分子內和分子間的氫鍵促成了聚合物二級結構的形成。然而,在合成聚合物中合適的氫鍵序列很難構建。因此,除了合成DNA 或者多肽,其他的鮮有報道。
1-2. 近期研究的綜述
光學活性聚合物研究在合成方面可以大致分為兩種類型:重復單元有手性中心的和沒有手性中心的。前者一個例子,聚合物主鏈上引入單體分子不對稱中心式最常用的方法,比如光學活性單體聚合通過聯萘為代表 (Habaue–Okamoto9,Tsubaki10)。除此之外,綜合方法目前承擔著對于主鏈上重復單元手性控制,即手性單體不對稱聚合螺旋狀選擇性類型(Okamoto11, Nozaki12)和 外消旋單體聚合不對稱單體選擇性類型(Kakuchi13)。另一方面,后者方法的處理,原子群各向異性排列感應現象,也就是,借助于單體內部或者外部不對稱源半剛性主鏈所產生的螺旋構象的手性和穩定性都會試圖以聚乙炔和聚異氰酸酯螺旋狀選擇性聚合作用為代表。根據聚合物主鏈基本結構,這些具有軸向手性誘導(沒有手性原子)光學活性聚合物在聚合物主鏈上粗略分為sp3–sp3型和sp2–sp2型。此外,sp2–sp2類型聚合主鏈光學活性聚合物更進一步的分為共軛和交叉共軛主鏈聚合物(Fig. 1-3)。
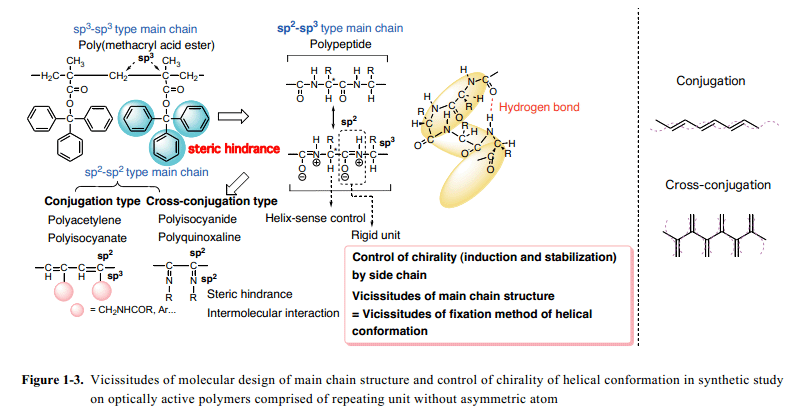
上面所述的早期的螺旋高分子聚丙烯酸酯歸類為一種具有sp3–sp3主鏈的螺旋聚合物,其構象的穩定性很大程度上取決于酯部分中的烷基基團。烷基取代導致了螺旋結構穩定性上很大程度的差異。盡管多肽本質上歸類為sp3–sp2型主鏈聚合物,120?鍵角肽鍵的平面性質歸因于共振酰胺部分提供部分剛性聚合物結構的聚合特征。α–螺旋構象的螺旋性質由α-碳和強力穩定構象的分子內氫鍵而決定的。后來光學活性聚合物的發展趨勢已經轉移到處理具有sp2–spa(a=2,3)類型主鏈重復單元的聚合物上面。聚乙炔和聚異氰酸酯都是具有共軛sp2–sp2 類型主鏈特征的聚合物,其中側鏈鍵通過sp2–sp3 鍵合誘導,穩固手性特征。另一方面,聚異氰化物是具有交叉共軛sp2–sp2 型主鏈結構的聚合物,其中側鏈鍵通過sp2–sp2 鍵合控制手性特征。對于這種類型的聚合物的合成,各種共軛與非共軛立體控制技術被研究出來。這種類型的光學活性聚合物獲得很大的收益,并且各種控制技術被提出和研究,尤其是從人造聚合物螺旋構象的設計和合成為出發點。
2. 螺旋結構的誘導和穩定性
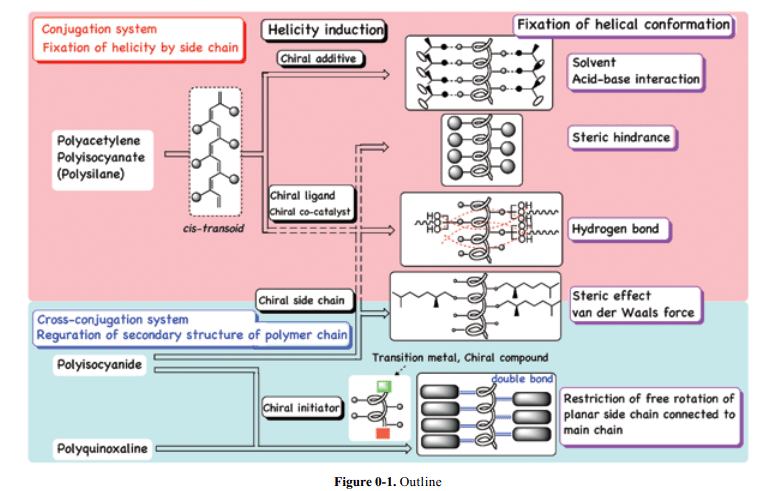
本文介紹了近期合成人造螺旋聚合物的研究工作,聚焦這些在重復單元出既無對稱中心業務對稱軸心的螺旋聚合物,根據合成方法可以分為三種類別:1)固定或者穩定的螺旋結構;2)分子外圍分子不對稱因素誘導的高分子主鏈構象;3)分子內不對稱因素不對稱誘導的高分子主鏈構象。
2-1. 用于聚合物螺旋構象的固定方法
本節討論用于維持聚合物螺旋結構與螺旋選擇性高分子螺旋構象的實用方法。這個目標的合成方法如下:1)分子間主-客體相互作用;2)金屬離子的配位或螯合;3)范德華力(相互作用);4)酸堿相互作用;5)氫鍵結合;6)龐大的側基立體效應等。
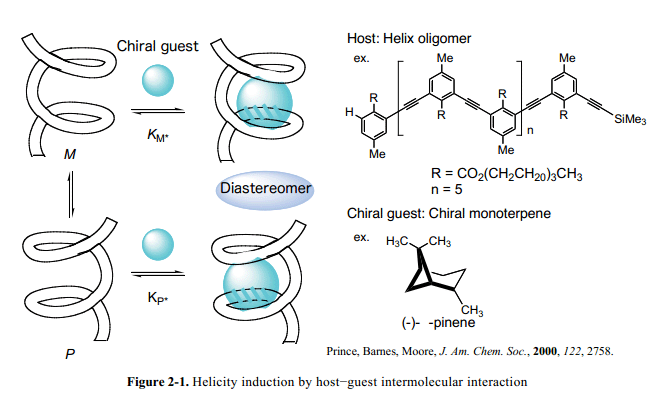
Moore 和他的伙伴們報道了m-苯乙炔撐低聚物的固定的螺旋構象(作為主體)通過手性單萜(作為客體)在乙腈溶液中以1:1混合比例而形成(Fig. 2-1)。14Inouye和他的同事已經揭示了聚(m-乙炔基吡啶)(作為主體)螺旋構象的電磁感應通過氫鍵和糖模板實現。15在這個系統里面,螺旋構象通過分子間氫鍵和剛性主鏈結構來固定。
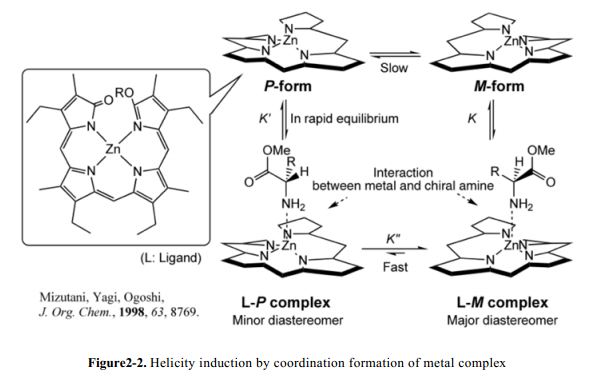
Ogoshi和同事16,Shinkai和其同事17 已經實現了感應芳香烴化合物螺旋構象,通過Zn或者Cu的螯合和手性添加劑分子分子間相互作用固定螺旋意義上的螺旋構象的(Fig. 2-2)。螺旋意義上的螺旋取決于更多的手性分子的結構。此外,Ishimaru和其同事保留了卟啉二聚體螺旋意義的螺旋構象誘導如下:外消旋卟啉二聚體與Zn(II)配合,借助手性胺-Zn相互作用由手性胺處理誘導螺旋構象,隨后移除手性胺,Ba2+離子與冠醚配合。18
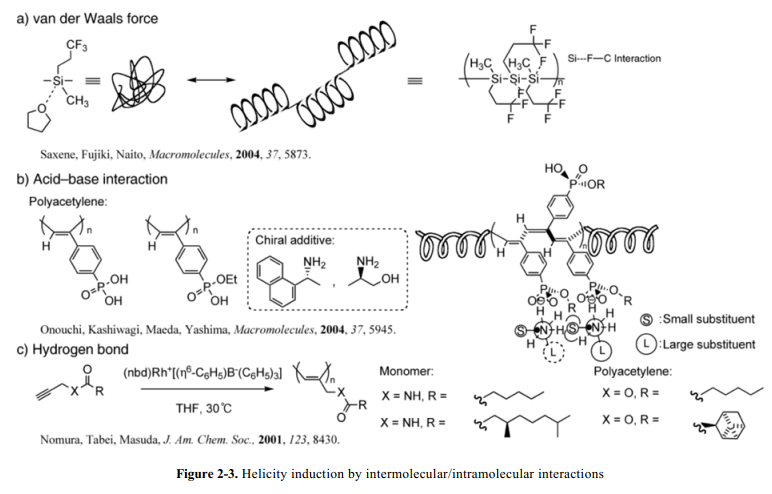
Fujiki 和其同事借助于Wurtz coupling 成功的合成了二甲硅同系物。這個聚硅烷具有長的烷基鏈,末端連接三氟甲基,通過微弱的Si---F–C間作用誘導和維護其螺旋構象。他們打算開發利用這種微弱的分子間范德華力的功能性材料。這個工作后來在Topic 1詳細描述:手性研究轉移和擴增。19
Yashima、Okamoto和他們的同事已經實現了聚乙炔衍生物(含有羧酸基側鏈或者磷酸部分的)的螺旋主鏈構象的誘導和維護。他們利用高分子主鏈上酸性側基和手性胺添加劑之間的酸堿作用誘導螺旋構象的感應現象,并且證明了手性醇替換手性胺之后其構象螺旋感應現象仍然保留。這項工作被后面的Topic 2詳細描述:手性記憶。
Masuda和他的同事通過借助于側鏈之間的氫鍵報道了poly(N-propargylamide)(具有笨重的手性側鏈和螺旋構象的順反結構的螺旋構象的)的誘導作用(Fig. 2-3c)。21
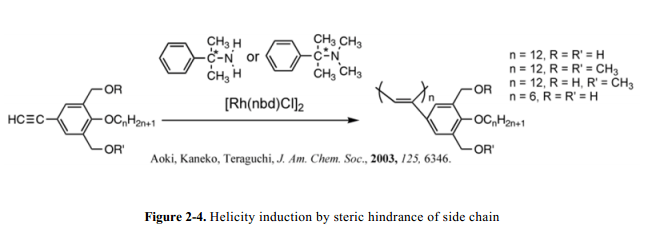
Aoki 和他的同事們清楚的演示了對比上述研究所不同的方法。由Yashima’s團隊和Masuda’s團隊報道了具有螺旋結構的聚合物的合成,其中手性醇和手性側鏈的存在是維護螺旋構象不可或缺的。相反,Aoki和他的同事證明了高分子聚合物(不使用不對稱源除了手性助催化劑(R)-/(S)-phenylethylamine)螺旋構象感應現象的維護(Fig. 2-4)。22,23這歸因于單分子結構隊列合適的設計,其中相應單元的氫鍵作用和大體積側基大致功能最為有效。
2-2.利用分子外不對稱源的不對稱誘導作用
在本節中,在重復單元主鏈或者側鏈部分沒有不對稱因素的高分子聚合物螺旋構象的不對稱誘導現象被具體描述。這種感應通過借助于單體或者聚合物分子外在的不對稱因素來進行完成。
Green 和他的同事們報道了poly(hexylisocyanate)由于其螺旋構象的原因在手性氯烷烴溶劑中顯示出一種Cotton效應。Yamashita和他的同事們報道了螺旋構象借助于手性添加劑和聚合物極性側鏈間的分子間相互作用的一個成功的誘導。例如,polyisocyanide的螺旋構象的誘導作用通過手性胺和hydroxycarbonyl側鏈間的酸堿作用來完成25,poly(phenylacetylene)的手性添加劑 分子通過冠醚側鏈實現虜獲。26基于這種方法的一個應用,他們展示了制備高分子電解質螺旋構象的方法。27
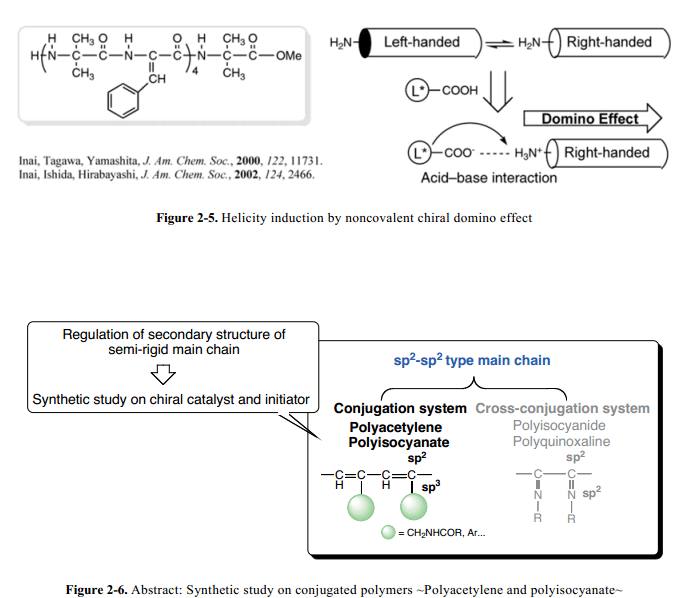
Fujiki和他的同事們報道了polysilane 通過添加手性醇的螺旋構象誘導效應的進行。28 此外,Masuda和他的同事們報道了手性N-propargylamide 通過酰胺側基和手性醇或者胺分子添加物之間的氫鍵作用的螺旋構象的誘導效應。1bInai和他的同事們發現整個多肽鏈的螺旋感應簡單的通過多肽的N-末端和依賴手性羧酸絕對構象的手性羧酸添加物之間的酸堿作用誘導(多米諾效應) (Fig. 2–5)。29
另一方面,有幾個不使用手性添加劑或者手性溶劑觀測到螺旋誘導現象的例子。Okamoto和他的同事們報道了聚噻吩借助于甲醇或者Cu(II)離子添加物實現了其不對稱誘導, 在良好的溶劑比如CHCl3中顯示無誘導CD。30
這個延伸到開發具有切換功能的手性超分子的研究中。為了實現開閉作用,發現了聚噻吩,在氯仿-乙腈混合溶液中,參雜Cu(II)–聯吡啶絡合物被利用。
在開發新型手性催化劑和引發劑的基礎上,有大量的工作從事于催化劑或引發劑的選擇上面,他們根據產物聚合物主鏈組合的靈活調整和單體龐大的側鏈來進行選擇。聚乙炔和聚異氰酸酯的手性特征的控制通過側基單鍵以sp2–sp3形式鏈接在共軛聚合物主鏈上(Fig. 2–6)。因此,已經有研究將用來開發手性催化劑控制聚合物主鏈構象。
由Rh或Mo組成的過渡金屬絡合物催化劑被用于控制聚乙炔主鏈構象。尤其是,[(nbd)RhCl]2和MoOCl4–nBu4Sn已經被認為是用于cis-transoid構象感應的有效催化劑。Noyori和其同事已經發現,Rh+(diene)[(η6-C6H5)B-(C6H5)3]類兩極離子Rh(I)絡合物的二烯配體很大程度上影響高分子聚合作用反應性。32此外,他們已經借助于Rh+(nbd)[(η6-C6H5)B-(C6H5)3]引發劑從含有長的烷基側鏈的單體中成功的合成了具有螺旋構象感應的聚乙炔(Fig.2-7,left)。這個含有自由的鹵素原子引發劑,溫和的反應條件下可以擔負高分子量的聚合物使得反應溫度低于室溫。另一方面,Okamoto和其同事報道了陰離子引發劑比如(-)-薄荷醇鋰鹽或 (S)-(+)-2-(1-吡咯烷甲基)吡咯烷能夠負擔芳香聚異氰酸酯的螺旋構象螺旋screw-sense(Fig. 2-7, right)。2b
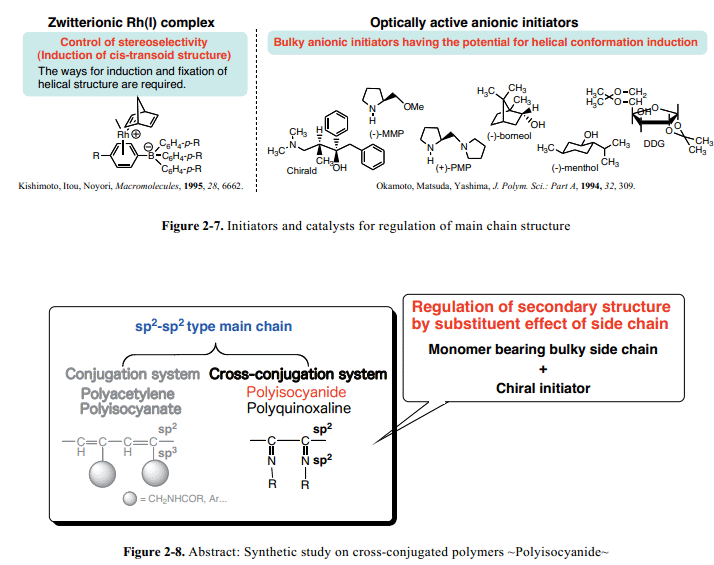
聚異氰化物和聚喹喔啉被列為交叉共軛主鏈聚合物。聚異氰化物螺旋構象screw-sense的控制與調節本質上取決于側基通過雙鍵形式(sp2–sp2)鏈接到主鏈上。單體取代基效應在手性引發劑研究過程中喚起了人們極大的興趣(Fig. 2-8)。
Nolte和其同事通過處理含有(R)-(+)-/(S)-(-)-(1-苯乙基)甲胺和鎳(II)四(叔丁基異腈)組成的引發劑大取代基的非手性異氰化物,成功的選擇性合成了聚異氰化物螺旋構象screw-sense。3
另一方面,Takahashi 和其同事借助于鉑–鈀雙核絡合物催化劑和低聚物引發劑實現了聚異腈(從手性和非手性異氰化物而來的)的screw-sense螺旋構象(Fig. 2-9)。33 這個高分子共聚物具有同樣的螺旋結構screw sense鏈接手性單體同聚物。著這個系統里面, 存在的無規共聚物按低聚物順序排好是必不可少的,在這里,手性單體通過類似Sergeants和Soldiers rule的熱力學控制來管理螺旋screw-sense。在本質上類型相同,Drenth和其同事完成了聚異腈的合成以及通過非手性異腈和具有大的側鏈的手性異氰化物的共聚作用聚合物的螺旋構象screw-sense感應。34然而,其螺旋screw-sense與單獨自含有手性側鏈單體合成而來的均聚物正好相反(Fig. 2-10, left)。這個出乎意料的結果被理解如下:非手性異氰化物聚合得到大量的右旋和左旋screw-sense螺旋聚合物,導致螺旋聚合物外消旋混合物(聚合物)的形成。另一方面,光學活性(手性)異氰化物單體的聚合作用僅僅擔負兩個螺旋構象screw-sense的一個。
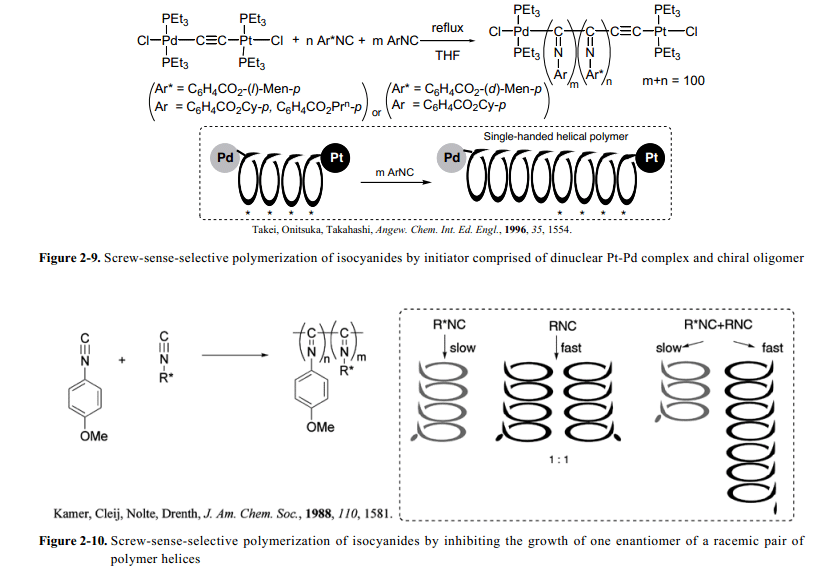
此外,光學活性異氰化物單體的聚合作用慢于非手性氰化物。其中聚合蔓延的速度非常慢的手性單體能夠影響到由非手性異氰化物單體而來的螺旋聚合物末端蔓延。然而,手性異腈單體在由非手性異腈單體衍生得到的兩種螺旋聚合物中反應速率的差異是很重要的,它只允許非手性異腈單體螺旋聚合物末端的反應,手性異腈單體所承擔的與螺旋方向一致。此外,高分子鏈末端鏈接的手性異腈單體很容易抵制下面的反應。與這種情況是一致的,螺旋高分子的兩種screw-sense中的一個收到很強大的控制可以允許螺旋高分子另外一個screw-sense的高分子聚合終端反應優先形成螺旋聚合物的screw-sense(Fig. 2-10, right)。
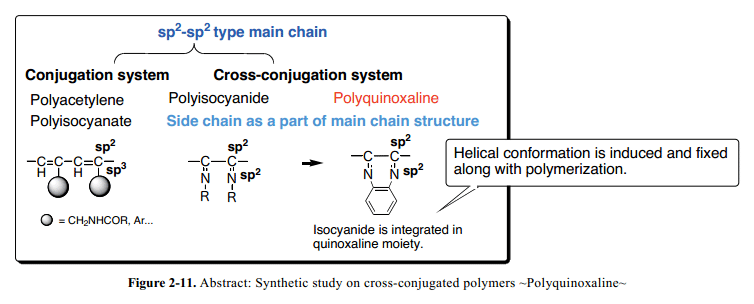
與螺旋聚異氰化物聚合物支柱screw-sense通過側鏈“獨立”控制和管理相反, C=N鍵對并入喹喔啉雜芳環形式延伸的側鏈可以有效的修復聚合物鏈。一個自然的結果中,利用喹喔啉單元的如此的特點已經開發了一系列的螺旋聚合物, 并入聚合物主鏈然后沿著螺旋構象感應進行主鏈的延伸(Fig. 2-11)。
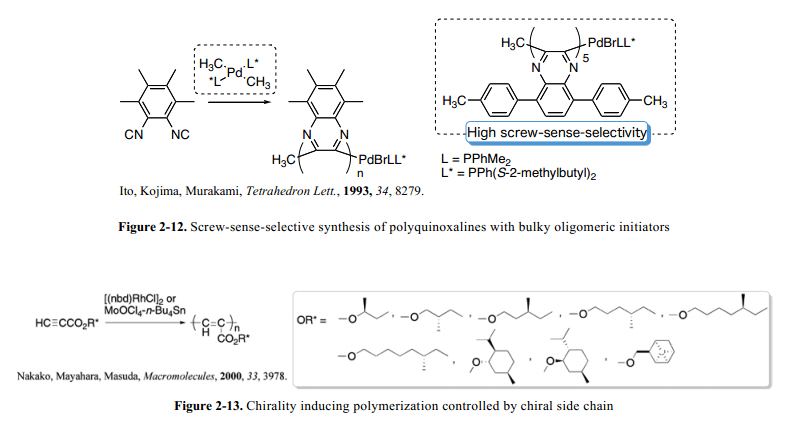
Ito和其同事報道了1,2-diisocyanoarenes借助于Pd(II)復合物的高分子聚合。35 他們報道在具有相對低選擇性手性膦配體的Pd(II) 復合物幫助下用于螺旋結構screw-sense的產生,相對于獲得的聚喹喔36,借助于光學喹喔啉pentamer-Pd(II) 復合物可以高選擇性的實現螺旋screw-sense(Fig. 2-12)。37 此外,基于分離檢查的基礎上,我們發現screw-sense-selectivity的實現并不取決于膦配體的取代基類型。36這就意味著,Pd(II)復合物螺旋screw-sense的選擇性不是決定于膦配體的手性特征,而是決定于聚合物的二級結構。這樣的考慮基礎上,Suginome和其同事借助于含有簡單不對稱源1,1'-聯萘的Pd(II)復合物成功的完成了1,2-diisocyano-3,6-di-p-toluoylbenzene的螺旋screw-sense-selective聚合作用。38 這個screw-sense-selective螺旋結構成功的感應現象歸因于先前形成的引發劑螺旋構象本身具有很高的screw-sense-selectivity。因此,聯萘核心取代基的選擇決定了聚合作用中螺旋構象的screw-sense-selectivity。
2-3. 利用分子內部不對稱源的螺旋Screw-Sense 感應現象
在本節中,將會介紹一些借助于單體內不對稱源的螺旋screw-sense感應。關于這一類的方法,具有手性側鏈的單體的簡單聚合作用和由手性側基控制的特定環境下的聚合作用比如分子間相互租用或者側基間空間排斥都有報道。Masuda 和其同事合成了一系列具有不同長度手性側鏈或者大小的聚乙炔
參考文獻
1) (a) R. Nomura, J. Tabei, T. Masuda, Macromolecules 2002, 35 , 2955-2961. (b) J. Tabei, R. Nomura, F. Sanda, T. Masuda, Macromolecules 2003, 36, 8603-8608.
2) (a) M. Green, C. Andrea, M. Reidy, J. Am. Chem. Soc. 1988, 110, 4063-4065. (b) Y. Okamoto, M. Matsuda, E. Yashima, J. Polymer Science: Part A 1994, 32 , 309-315.
3) P. Kamer, R. Nolte, W. Drenth, J. Am. Chem. Soc. 1988, 110, 6818-6825.
4) K. Ute, K. Hirose, K. Hatada, J. Am. Chem. Soc. 1991, 113, 6305-6306.
5) T. Nakano, Y. Okamoto, KIKAN KAGAKU SOSETSU 1993,18,129.
6) M. Fujiki, High POLYMERS 2004, 53 , 938-941.
7) (a) H. Nakako, R. Nomura, T. Masuda, Macromolecule, 1999, 32, 2861-2864. (b) H. Nakako, Y. Mayahara, T. Masuda, Macromolecules 2000, 33, 3978-3982.(c)E. Yashima,T.Matsushima,Y.Okamoto, J.Am. Chem. Soc. 1997, 119, 6345-6359. (d) E. Yashima, S. Huang, Y. Okamoto, Macromolecules 1995, 28 , 4184-4193.
8) B. Langeveld-Voss, E. Meijer, J. Am. Chem. Soc. 1996, 118, 4908-4909.
9) S. Habaue, T. Seko, Y. Okamoto, Macromolecules 2003, 36,2604-2608.
10) K. Tsubaki, M.Miura,H.Morikawa,J.Am. Chem. Soc. 2003, 125, 16200-16201.
11) (a)T. Nakano, K. Tsunematsu, Y. Okamoto, Chem. Lett. 2002, 31 , 42-43. (b) N. Hoshikawa, Y. Hotta, Y. Okamoto, J. Am. Chem. Soc. 2003, 125, 12380-12381.
12) K. Nozaki, J. Polymer Science: Part A 2004, 42 , 215-221.
13) M. Tsuji, R. Sakai, T. Kakuchi, Macromolecules 2002, 35 , 8255-8257.
14)R. Prince, S. Barnes, J. Moore, J. Am. Chem. Soc. 2000, 122, 2758-2762.
15) M. Inouye, M. Waki, H. Abe, J. Am. Chem. Soc. 2004, 126, 2022-2027.
16)(a) T. Mizutani, S. Yagi, H. Ogoshi, J.Org. Chem. 1998, 63, 8769-8784. (b) T. Mizutani, S. Yagi, H. Ogoshi, J. Org. Chem. 1998, 63 , 8769-8784.
17)M. Yamamoto, M. Takeuchi, S. Shinkai, J. Chem. Soc. Perkin Trans. 2 2000, 9-16.
18)Y.Kudo, T. Ohno, Y. Ishimaru, J. Am. Chem. Soc. 2001, 123, 12700-12701.
19) A. Sexana, M. Fujiki, M. Naito, Macromolecules 2004, 37 , 5873-5879.
20)a) E.Yashima,K.Maeda,Y.Okamoto,Nature 1999, 399, 449-451. b) H. Onouchi,D. Kashiwagi, K. Maeda, E. Yashima, Macromolecules 2004, 37 , 5495-5503.
21) R. Nomura, J. Tabei, T. Masuda, J. Am. Chem. Soc. 2001, 123, 8430-8431.
22) T.Aoki, T. Kaneko,M.Teraguchi, J. Am. Chem. Soc. 2003, 125, 6346-6347.
23) Y. Umeda, T. Kaneko, M. Teraguchi, T. Aoki, Chem. Lett. 2005, 34 , 854-855.
24) M. Green, C. Khanti, C. Peterson, J. Am. Chem. Soc. 1993, 115, 4941-4942.
25) M. Ishikawa, K. Maeda, E. Yashima, J. Am. Chem. Soc. 2002, 124, 7448-7458.
26) R. Nonokawa, E. Yashima, J. Am. Chem. Soc. 2003, 125, 1278-1283.
27) H. Onouchi, K. Maeda, E. Yashima, J. Am. Chem. Soc. 2001, 123, 7441-7442.
28)H.Nakashima,J.Koe, K.Torimitsu,M.Fujiki, J.Am.Chem.Soc.2001,123, 4847-4848.
29) (a)Y. Inai, K. Tagawa, M.Yamashita, J. Am.Chem. Soc. 2000, 122, 11731-11732. (b)Y. Inai, Y. Ishida, T. Hirabayashi, J. Am. Chem. Soc. 2002, 124, 2466-2473.
30) E. Yashima, H. Goto, Y. Okamoto, Macromolecules 1999, 32, 7942-7945.
31) H. Goto, E. Yashima, J. Am. Chem. Soc. 2002, 124, 7943-7949.
32)Y. Kishimoto, M. Itou, R. Noyori, Macromolecules 1995, 28, 6662-6666.
33) (a) F. Takei, K. Onitsuka, S. Takahashi, Angew. Chem. Int. Ed. Engl. 1996 , 35, 1554-1556. (b) F. Takei, K. Onitsuka, S. Takahashi, Polymer J. 2000, 32 , 524-526.
34)P. Kamer, M.Cleij, R.Nolte,W. Drenth, J. Am. Chem. Soc. 1988, 110, 1581-1587.
35) Y. Ito, E. Ihara, M. Murakami, J. Am. Chem. Soc. 1990, 112, 6446-6447.
36) Y. Ito, Y. Kojima, M. Murakami, Tetrahedron Lett. 1993, 34, 8279-8282.
37)Y. Ito, Y.Kojima,M.Murakami,Angew.Chem. Int. Ed. Engl. 1992, 31 , 1509-11510.
38) (a) Y. Ito, T. Ohara, M. Suginome, J. Am. Chem. Soc. 1996, 118, 9188-9189. (b) Y. Ito, T. Ohara, M. Suginome, J. Am. Chem. Soc. 1998, 120, 11880-11893. (c) Y. Ito, T. Ohara, M. Suginome, Macromolecules 1998, 31 , 1697- 1699.
注:本文為提供者整理翻譯的,由于知識所限,錯誤在所難免,敬請原諒。如有問題可以查找原文。
統計數據
共收錄化學品數據
147579 條



 滬公網安備 31010602001115號
滬公網安備 31010602001115號