與胺/酰胺配體合作的雙功能分子催化
- 2013-01-21
- 專題
1. 介紹
過渡金屬類分子催化劑伴隨著新型的催化轉換以及人們對反應機制的了解有了進一步的發展。特別是,持續付出的大量努力開發了具有兩個或者更多個活性位點協同一致的雙功能分子催化劑,從而實現了有機合成高效分子變換。最近,我們開發了金屬配體雙功能催化劑(協奏催化劑),其中non-innocent ligands直接參與基質的激活和鍵的形成。雙功能分子催化是一個有吸引力和總體策略的概念可以實現有效地分子改造。1)
1995年, Noyori 和他的同事們報道了二胺配體在簡單的芳香酮和BINAP-Ru(II) [BINAP=2,2’-雙(二苯基膦基-1,1’-聯萘)]系統對映選擇性加氫方面一個嶄新的影響。2) RuCl2[(S)-binap](dmf)n,手性1,2-二胺和KOH組合在酮加氫反應中比經典的BINAP–Ru催化劑顯示出更為高級的活性。隨后,一個新的膦釕催化劑概念的雛形,以N-磺化1,2-二胺為手性試劑得到了進一步的發展,用于酮類的高效不對稱轉移氫化反應。3)這個真正的催化劑的詳細的實驗內容和理論分析表明,如Figure 1中所描述的,在循環催化過程中,具有正方形平面幾何狀的氨釕絡合物和配位飽和的氫化(胺)釕絡合物都有涉及。酰胺絡合物具有足夠的Br?nsted堿度,很容易氫化得到含有2-丙醇基的仲醇用以生產氫化(胺)配合物。NH單元被綁定到胺配合物金屬中心,具有足夠的酸性可以用來激活酮基質。在氨基和胺絡合物的相互轉換中,金屬/NH部分協同合作通過一個環狀過渡態傳遞氫,其中,H–和H+ 被通過一個方式等量轉移,從氫(胺)絡合物到C=O鍵,或者從2-丙醇到胺絡合物,并且不用金屬中心的直接協調(外層機制)。雙功能過渡金屬分子催化劑這個獨特的概念使得反應具有高利率和顯著的空間立體選擇性,因為 這個反應是通過一個配置緊密的設備和手性催化劑得以完成。
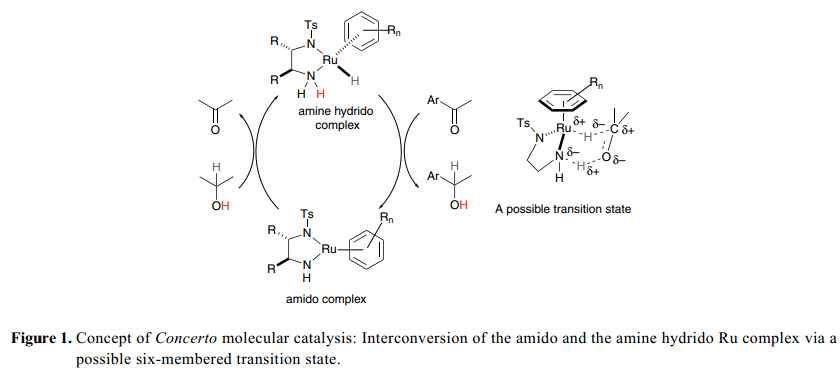
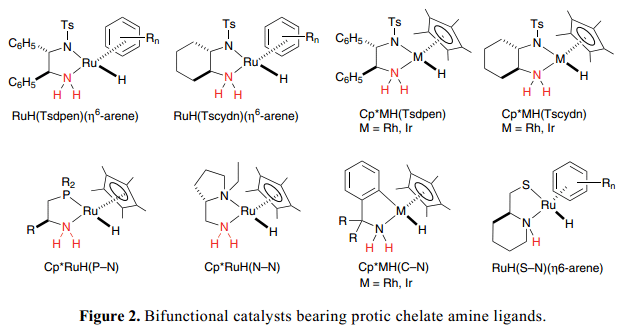
Figure 2 列舉了我們組新近開發的一些有明確定義的雙功能分子催化劑的代表性例子。手性雙功能η6-arene–Ru絡合物的概念是,RuH(Tsdpen)( η6-arene), [Tsdpen =N-(p-甲苯磺酰基)-1,2-二苯基乙二胺]已經被成功的擴展到了類似的Cp*Rh和Ir絡合物中,Cp*MH(Tsdpen)[Cp*=η5-C(CH3)5,M=Rh, Ir]。4)除了N–磺酰化二胺復合物,8 和9組的金屬絡合物與二胺(N–N),5) 氨基膦(P–N),6) 氨基乙硫醇(S–N),7)o-氨基甲苯(C–N)8) 配體已經被廣泛的開發用作完成金屬/NH效應的雙功能分子催化劑。
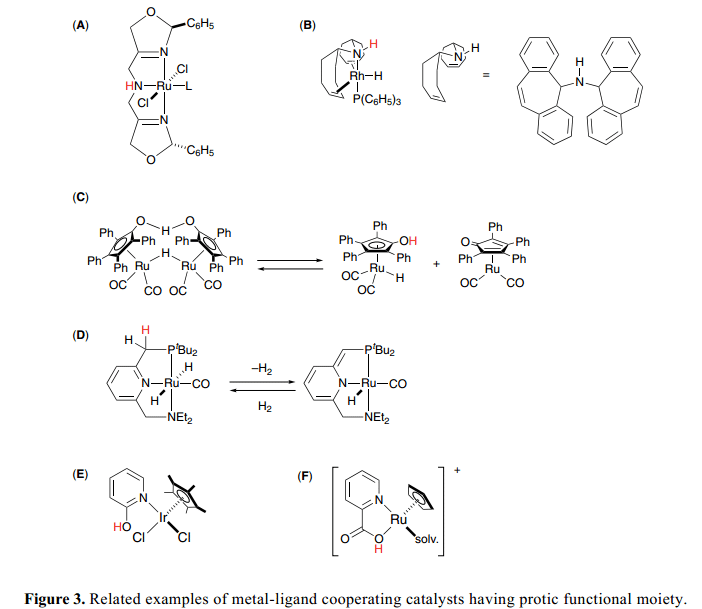
其他的研究小組研究別的相關的雙功能催化劑,Figure 3表示了幾組8 和9絡合物,其中輔助配體上的質子官能團與金屬中心協作催化氫化,氫化轉移等。Zhang(A)9)和Grützmacher催化劑(B)10) 具有三叉質子胺配體,能夠幫助H+/H–類似的方式下轉移到雙功能催化劑上面。Shvo催化劑 (C)11)可以釋放催化活性物質,環戊二烯和環戊二烯酮絡合物,OH基團作為質子媒介在促進氫轉移過程中起到了一個關鍵的作用。最近,Milstein開發了新的PNN pincer complexes (D)12) 作為高活性氧化還原催化劑,并且找到了他們獨特的通過脫芳構化作用的氫化/脫氫反應機制。Fujita和Yamaguchi設計了Cp*Ir 絡合物(E)13),具有2-羥基吡啶和pyridonate配體,可以有效地通過酸性OH 官能團促進仲醇的脫氫反應。Kitamura和Tanaka 證明了The acidic nature of CpRu fragment (F)上的2-喹啉羧酸酸性質影響到了烯丙基醇C–O鍵的活性從而得到烯丙基醚。14)
本為關注于我們最新的進展,基于金屬/NH協作的雙功能分子催化劑,它們利用不對稱還原轉換反應和相關的對映選擇性C–C和C–N鍵的生成反應。
2.使用雙功能催化劑的不對稱轉移氫化反應1c)
一般來講,2-丙醇可以用作一種安全、無毒、環境友好型氫源。盡管2-丙醇的不對稱還原得到了一個令人滿意的結果,但是,其內在的一個弊端是氫轉移是可逆的,這就導致了轉移的局限取決于系統的熱力學因素以及反應混合物和催化劑在長時間曝光下產品對映體純度的損耗。另一方面,甲酸遵循不對稱還原反應,在不可逆轉方法中轉換率100%。15)
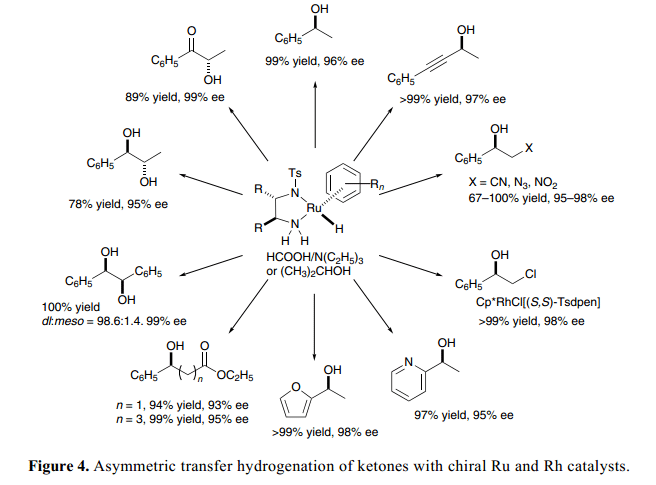
簡單的芳香酮類和含有雙功能催化劑的甲酸、三乙胺混合物的不對稱還原反應具有高效活性、選擇性、廣泛的底物范圍以及實用性等特點。雙功能氫化(胺)-Ru配合物是配體飽和,催化系統容許有氨基、酯、氰基、硝基、疊氮化和氯基團以及芳香雜環和炔鏈,1c)如Figure 4總結所示。C–N雙鍵也可以與甲酸和三乙胺含有手性Ru 或者Rh 催化劑的混合物還原得到相應的胺,具有一個很高的對映體過量百分數。16)
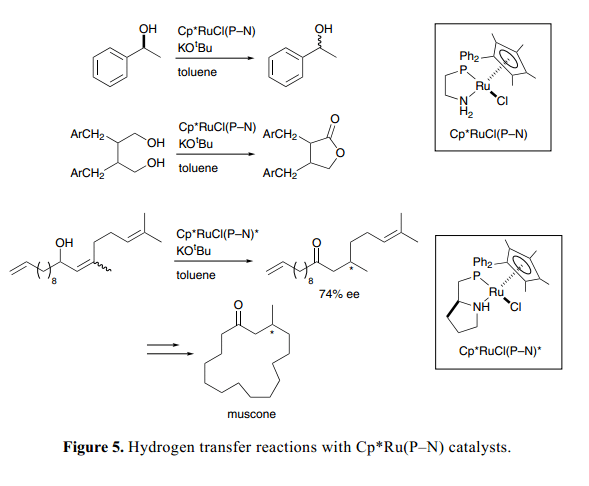
如Figure 5所示,一系列的含有質子膦胺螯合物配體的Cp*Ru(P–N)絡合物 也用作氫化轉移的高效催化劑。基于可逆氫化機制通過胺和氨絡合物兩者之間互換,氧化還原過程可以成功的用于手性醇的快速外消旋化17)以及利用丙酮將二醇特定的選擇氧化為內酯。18)手性Cp*Ru(P–N)復雜絡合物對映選擇性異構化烯丙基醇為β-取代基酮類,接下來閉環置換得到溫和的(R )-麝香酮。19)
3. 極性基質雙功能催化劑的催化加氫6)
由于我們在2001年報道了醇溶劑在綁定異裂H2鍵到16-電子[Cp*Ru{Me2 N(CH2)2 NH2}]+(Cp*Ru(N–N))片段的的影響,20)我們系統的測試了除酮以外的極性基質的催化氫化,發現具有叔膦基替換叔胺可以導致Ru/NH 雙功能范圍擴大化。例如, Cp*Ru(P–N復合物,[Cp*Ru{Ph2 P(CH2)2 NH2}]+, 在各種終端環氧化物中給不飽和C–O選擇性提供氫鍵,從而生成相應的仲醇,然而Cp*Ru(N–N) 復合物是完全消極惰性的。21)
Cp*RuCl(P–N)催化劑直接催化氫化N-acylcarbamates和carboxyimides選擇性得到N -protected amines 和alcohols。22)
值得注意的是,目前的氫化作用適用于還原轉化反應。雙功能催化條件下伯胺從N-phthalimides脫保護同樣適用于Gabriel氨基酸的合成。例如, N-鄰苯二甲酰-L-苯丙氨酸甲酯通過手性N–acyloxazolidiones處理氫解得到物光學純度損耗的L-Phe甲酯鹽酸鹽,這是由Evans 研發的合成手性醇和無光學純度損耗的original 手性助劑的非常有用的合成中間體,如Figure 6所示。23a)
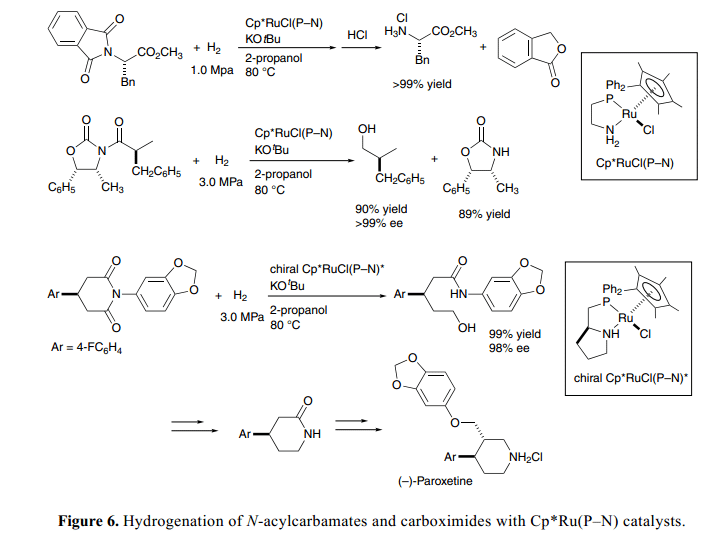
手性Cp*Ru(P–N)催化劑,具有手性P–N配合基鍵(由L-普氨酸衍生得到)促進前手性4-arylglutarimides對映選擇性氫化通過去保護得到相對應的δ-羥基酰胺,具有很好的ee值,且產率很高。進一步細化加工得到手性哌啶酮衍生物,這個可以作用合成生理學光學活性手性化合物包括抗抑郁藥物帕羅西汀等的重要合成中間體。
Cp*Ru(P–N)催化劑強壓條件下也能促進酯和酰胺類氫化得到醇或者胺。23b)這個氫化過程使用金屬氫化試劑化學計量法也將為傳統的還原方法提供一個很強大的替代方法。
4. 雙功能催化劑有氧氧化反應24)
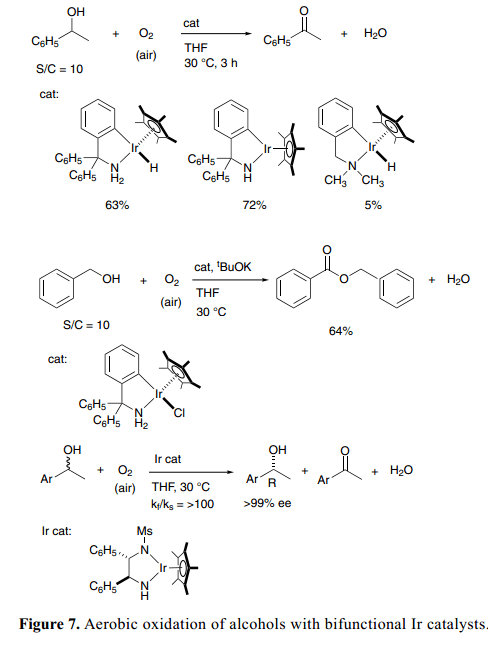
當分子氧用于雙官能團醇類脫氫氧化反應中的氫原子受體時,有氧氧化變為一個簡單且有機廢物最小化的一個過程。幸運的是,我們發現了一個新的可孤立的官能團酰胺-Ir絡合物,具有一個C–N螯合胺配體Cp*Ir[ κ2(N,C)-(NHCR2-2-C6H4)] (R=C6H5和CH3),和相應的氫(胺)絡合物Cp*IrH[κ2(N,C)-{NH2CR2-2-C6H4}],可以作為酮類轉移氫化反應的高效催化劑,促進催化醇類的有氧氧化。8a)1-苯基乙醇的催化反應在空氣大氣壓強下平穩進行,含有酰胺-Ir絡合物,Cp*Ir[κ2(N, C)-{NHC(C6H5)2-2-C6H4}] (Figure 7)。25)氫(胺)-Ir 絡合物,Cp*IrH[κ2(N,C)-{NH2C(C6H5)2-2-C6H4}], 和二元態催化劑系統(含有氯(胺)-Rh、-Ru絡合物和KOC(CH3)3), 也能得到氧化產物苯乙酮。伯醇在相同條件下反應得到二聚產品、酯類等。當含有氯絡合物組分催化劑的芐醇混合物Cp*IrCl[κ2(N,C)-{NH2C(C6H5)2-2-C6H4}], 與當量的KOC(CH3)3在THF中攪拌反應,空氣溫度為30 °C時,得到相對應的苯甲酸芐酯衍生物。
當應用到二級醇與手性酰胺催化劑的動力學拆分時,醇的有氧氧化更為引起人們的興趣(Figure 7)。有氧氧化條件下通過手性Ir 絡合物Cp*Ir[( S,S)-Msdpen](Ms=甲磺酰),有效的解決了外消旋1-苯乙醇的動力學拆分,得到48%的 (R)-1-苯基乙醇和98% ee;kf/ ks比率為100。26)同樣的,1-indanol與1-tetralol 室溫下反應得到R-enantiomers,>99% ee且46–50%產率。
5.承接金屬-N鍵的雙核雙功能催化劑的擴展27)
金屬配體雙能能效應實現了單核half-sandwich氨基絡合物的形成,有望于 有效的制備具有M–N鍵的亞氨基-橋雙核絡合物。細致的結構分析和NMR研究 表明了吸電子雙核集團使得亞氨基橋雙核絡合物穩固,28) 同時也具有一源于M–N鍵的酸堿雙功能性質。
不飽和雙(亞氨)-橋二銠(III)復合物配體,[(Cp*Rh)2(μ-NTs)2](Ts=SO2C6H4CH3-p)室溫下與H2(1atm)在CH2Cl2中反應24h得到雙(亞氨)-橋二銠(II)復合物(Cp*Rh)2(μ-NHTs)2],產率為82% 如Figure 8所示。應該注意的是,在這個反應中, H2形式上轉換為兩個氨基質子和兩個電子用于二銠在[(Cp*Rh)2(μ-NTs)2]的還原。雙(亞氨) 復合物與過量的2-丙醇反應得到雙(胺基)復合物。兩個NH質子的產生與金屬中心的兩個電子還原相結合與伯醇、仲醇通過不飽和單核氨基絡合物脫氫作用形成了鮮明的對比,這就導致了hydrido–amine復合物的形成,并且如上所述沒有形成正式的金屬的還原。
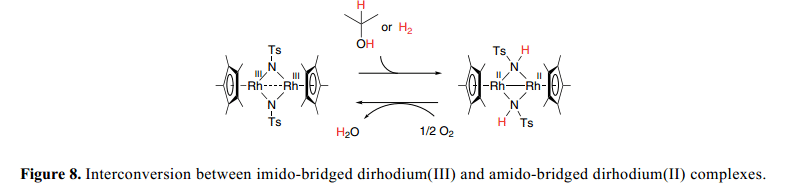
雙(氨基)-橋二銠(II)復合物與O2快速反應形成雙(亞氨)-橋二銠(III)復合物和水。29) 此外,雙核imido和amido之間的溫和的氧化還原互換可以應用到H2和醇的有氧氧化中起到催化作用。
6. 不對稱共軛加成雙功能催化劑30)
堿性氨基復合物可以與含酸性的有機化合物反應,得到含有金屬碳鍵親核試劑的胺復合物。例如,我們發現紫色Ru復合物,Ru[(R, R)-Tsdpen]( η6-三甲苯),–30°C條件下與丙二酸二甲酯在甲苯中平穩反應得到黃色結晶物,Ru[CH(CO2 CH3)2][(R,R)-Tsdpen](η6-三甲苯)。31)如果從一個氨基金屬復合物中得到的具有金屬鍵親核試劑的胺胺復合物進攻缺電子受體,催化作用的C–C 鍵形成得以實現。事實上,手性Ru催化劑,Ru[(S,S)-Tsdpen](η6-arene)有效的提高了dimethyl malonate對環enones 或者nitro olefins的對映選擇性Michael 加成反應得到具有很好的ee值的加成產物(Figure 9)。通過雙功能Ru催化劑,1,3-dicarbonyl compounds對cyclic enones的Michael addition 反應的NMR和DFT分析結果表明對映選擇性C–C鍵的形成通過螯合電子對中間物的形成, Ru金屬中心與enone分子協同為C–C鍵的形成制造出一個高組織性環境,只產生一種對映選擇性產品。31b)

手性氨基催化劑對映選擇性共軛加成可以擴展到α –cyanoacetates與dialkyl azodicarboxylates的Ir-催化反應得到直接胺化產物。2)當乙炔酯用作親電子試劑,α–cyanoacetate和雙功能手性催化劑對映選擇性和Z 選擇性共軛加成得到手性加成產物,擁有一個四元碳中心,具有很好的ee值。33)
7. 總結
本文主要關注最新進展的化學概念上的新的包括立體性、區域性和化學選擇性還原劑或者氧化轉移以及對映選擇性質C–C、C–N鍵(通過Michael-type共軛加成而產生)的協作催化劑與雙功能過渡金屬分子催化劑。配位胺試劑合理的設計使得M/NH單元中電子因素在雙功能催化劑中顯示平衡狀態,是其具有廣泛性和高實用性的催化性能的決定性因素。我們相信目前雙功能分子催化劑能夠為開啟新的選擇性分子轉移包括對映選擇性合成的層面上提供一個廣闊的機會。
參考文獻
1) a) T. Ikariya, K. Murata, R. Noyori, Org. Biomol. Chem. 2006, 4, 393. b) K. Mu?iz, Angew. Chem. Int. Ed. 2005, 44 , 6622. c) T. Ikariya, A. J. Blacker, Acc. Chem. Res. 2007, 40, 1300. d) T. Ikariya, Bull. Chem. Soc. Jpn. 2011, 84 , 1.
2) a) T. Ohkuma, H. Ooka, S. Hashiguchi, T. Ikariya, R. Noyori, J. Am. Chem. Soc. 1995, 117, 2675. b) T. Ohkuma, H. Ooka, S. Hashiguchi, T. Ikariya, R. Noyori, J. Am. Chem. Soc. 1995, 117, 10417.
3) a) S. Hashiguchi, A. Fujii, J. Takehara, T. Ikariya, R. Noyori, J. Am. Chem. Soc. 1995 , 117 , 7562. b) K.-J. Haack, S. Hashiguchi, A. Fujii, T. Ikariya, R. Noyori, Angew. Chem. Int. Ed. Engl. 1997, 36 , 285.
4)a) K. Murata, T. Ikariya, R. Noyori, J. Org. Chem. 1999, 64, 2186. b) K. Mashima, T. Abe, K. Tani, Chem. Lett. 1998, 1199. c) K. Mashima, T. Abe, K. Tani, Chem. Lett. 1998, 1201.
5) M. Ito, M.Hirakawa, K. Murata, T. Ikariya , Organometallics 2001, 20 , 379.
6) a) M. Ito, T. Ikariya, Chem. Commun. 2007, 5134. b) M. Ito, A. Osaku, C. Kobayashi, A. Shiibashi, T. Ikariya, Organometallics 2009, 28 , 390. c) M. Ito, T. Ikariya, J. Synth. Org. Chem. Jpn. 2008, 66 , 1042.
7) a) M. Ito, Y. Shibata, A. Watanabe, T. Ikariya, Synlett 2009, 1621. b) M. Ito, A. Watanabe, Y. Shibata, T. Ikariya, Synlett 2010, 29 , 4584.
8) a ) S. Arita, T. Koike, Y. Kayaki, T. Ikariya , Organometallics 2008, 27 , 2795. b) J.-B. Sortais, V. Ritleng, A. Voelklin, A. Holuigue, H. Smail, L. Barloy, C. Sirlin, G. K. M. Verzijl, J. A. F. Boogers, A. H. M. de Vries, J. G. de Vries, M. Pfeffer, Org. Lett. 2005, 7, 1247.
9) Y. Jiang, Q. Jiang, X. Zhang, J. Am. Chem. Soc. 1998, 120, 3817.
10) a) P. Maire, T. Büttner, F. Breher, P. Le Floch, H. Grützmacher, Angew. Chem. Int. Ed. 2005, 44 , 6318. b) T. Zweifel, J.-V. Naubron, T. Büttner, T. Ott, H. Grützmacher, Angew. Chem. Int. Ed. 2008, 47 , 3245. c) T. Zweifel, J.-V. Naubron, H. Grützmacher, Angew. Chem. Int. Ed. 2009 , 48 ,
559.
11) a ) Y . B l u m , D . C z a r k i e , Y . R a h a m i n , T . S h v o , Organometallics 1985, 4, 1459. b) Y. Shvo, D. Czarkie, Y. Rahamim, D. F. Chodosh, J. Am. Chem. Soc. 1986, 108, 7400.
12) a) J. Zhang, G. Leitus, Y. Ben-David, D. Milstein, J. Am. Chem. Soc. 2005, 127, 10840. b) C. Gunanathan, Y. Ben-David, D. Milstein, Science 2007, 317, 790. c) S. W. Kohl, L. Weiner, L. Schwartsburd, L. Konstantinovski, L. J. W. Shimon, Y. Ben-David, M. A. Iron, D. Milstein, Science 2009, 324, 74.
13) a) K. Fujita, N. Tanino, R. Yamaguchi, Org. Lett. 2007, 9, 109. b) R. Yamaguchi, C. Ikeda, Y. Takahashi, K. Fujita, J. Am. Chem. Soc. 2009, 131, 8410.
14) a) S. Tanaka, H. Saburi, Y. Ishibashi, M. Kitamura, Org. Lett. 2004, 6, 1873. b) S. Tanaka, H. Saburi, M. Kitamura, Angew. Chem. Int. Ed. 2005, 44 , 1730. c) S. Tanaka, T. Seki, M. Kitamura, Angew. Chem. Int. Ed. 2009, 48 , 8948.
15) A. Fujii, S. Hashiguchi, N. Uematsu, T. Ikariya, R. Noyori, J. Am. Chem. Soc. 1996, 118, 2521.
16) a) N. Uematsu, A. Fujii, S. Hashiguchi, T. Ikariya, R. Noyori, J. Am. Chem. Soc. 1996 , 118 , 4916. b) J. Mao, D. C. Baker, Org. Lett. 1999, 1, 841.
17) M. Ito, A. Osaku, S. Kitahara, M. Hirakawa, T. Ikariya, Tetrahedron Lett. 2003, 44 , 7521.
18) a) M. Ito, A. Osaku, A. Shiibashi, T. Ikariya, Org. Lett. 2007, 9, 1821. b) M. Ito, A. Shiibashi, T. Ikariya, Chem. Commun. 2011, 2134.
19) M. Ito, S. Kitahara, T. Ikariya, J. Am. Chem. Soc. 2005, 127, 6172.
20) M. Ito, M. Hirakawa, K. Murata, T. Ikariya , Organometallics 2001, 20 , 379.
21) M. Ito, M. Hirakawa, A. Osaku, T. Ikariya, Organometallics 2003, 22 , 4190.
22) a) M. Ito, A. Sakaguchi, C. Kobayashi, T. Ikariya, J. Am. Chem. Soc. 2007, 129, 290. b) M. Ito, C. Kobayashi, A. Himizu, T. Ikariya, J. Am. Chem. Soc. 2010, 132, 11414.
23) a) M. Ito, L. W. Koo, A. Himizu, C. Kobayashi, A. Sakaguchi, T. Ikariya, Angew. Chem. Int. Ed. 2009, 48 , 1324. b) M. Ito, T. Ootsuka, R. Watari, A. Shiibashi, A. Himizu, T. Ikariya, J. Am. Chem. Soc. 2011, 133, 4240.
24) T. Ikariya, S. Kuwata, Y. Kayaki, Pure Appl. Chem. 2010, 82, 1471.
25) S. Arita, T. Koike, Y. Kayaki, T. Ikariya, Chem. Asian J. 2008, 3, 1479.
26) S. Arita, T. Koike, Y. Kayaki, T. Ikariya, Angew. Chem. Int. Ed. 2008, 47 , 2447.
27) S. Kuwata, T. Ikariya, Dalton Trans. 2010, 39 , 2984.
28) a) K. Ishiwata, S. Kuwata, T. Ikariya, Organometallics 2006, 25 , 5847. b) H. Arita, K. Ishiwata, S. Kuwata, T. Ikariya, Organometallics 2008, 27 , 493.
29) K. Ishiwata, S. Kuwata, T. Ikariya, J. Am. Chem. Soc. 2009 , 113, 5001.
30) a) T. Ikariya, I. D. Gridnev, Chem. Rec. 2009, 9, 106. b) T. Ikariya, I. D. Gridnev, Top. Catal. 2010, 53 , 894.
31) a) M. Watanabe, K. Murata, T. Ikariya, J. Am. Chem. Soc. 2003, 125, 7508. b) I. D. Gridnev, M. Watanabe, H. Wang, T. Ikariya, J. Am. Chem. Soc. 2010, 132, 16637.
32) Y. Hasegawa, M. Watanabe, I. D. Gridnev, T. Ikariya, J. Am. Chem. Soc. 2008, 130, 2158.
33) Y. Hasegawa, I. D. Gridnev, T. Ikariya, Angew. Chem. Int. Ed. 2010, 49 , 8157.
注:本文為提供者整理翻譯的,由于知識所限,錯誤在所難免,敬請原諒。如有問題可以查找原文。
統計數據
共收錄化學品數據
147579 條



 滬公網安備 31010602001115號
滬公網安備 31010602001115號