利用芳香族羧酸酐的各種合成方法
- 2013-01-11
- 專題
概論
脫水縮合試劑,室溫下穩定,易處理,且反應性高,遵循這樣的結果,人們發現,芳香族羧酸酐可以用作各種功能強大的試劑。通過使用TFBA或者BTFBA與路易斯酸催化劑反應可以為碳氧鍵的形成提供一個最有效的支持,使得所需的羧酸酯和內酯的合成有很好的收益率。此外,堿性條件下,MNBA或者DMNBA與親核催化劑反應可以方便的制得酸敏感性羧酸酯、內酯和酰胺類。另外,利用PMBA或苯甲酸酐作為不對稱催化劑可以實現外消旋仲醇與外消旋2-芳疾病算的動力學拆分,從而建了一個新的合成光學活性羧酸酯、仲醇、2-芳基丙酸的方法。
1. 介紹
有效地人工合成有機物質,就要求開發用于形成(1)碳碳鍵;(2)碳氫鍵;(3) 碳氧鍵;(4)高選擇性的碳氮鍵的簡便方法。隨著有機合成二十多年來的飛速發展,多來越多的優秀的化學合成方法被開發出來。“無環立體控制合成方法”的建立,比如說形成區域選擇性和立體選擇性碳碳鍵的烯丙基化反應或者醇醛縮合反應使得近幾年來構建分子量超過1000的有機分子碳骨架成為可能。對于碳氫鍵的形成,由于不對稱氫化反應的不斷進步等,易獲得光學活性分子的絕對構型控制。
然而,與令人矚目的(1)與(2)的研究相比較, (3)和(4)新反應形成的發展目前沒有大的進展。在這種情況下,我們試圖通過使用“芳香族羧酸酐” 作為縮合試劑來開發一系列新的碳-雜元素鍵的形成反應。由于這些反應在溫和的條件下進行,并且沒有有害物質比如重金屬等的使用,因此這些方法合成有機分子對環境負擔小,并且可以高選擇性的在任何的位置形成碳雜元素鍵。在本文中,我們介紹一系列這些年中我們從開發到應用覆蓋的研究成果。
2.利用“芳香族羧酸酐”的縮合反應的發現
在研究甲硅烷基烯醇醚化學性質的同時,我們也研究了羧酸的甲硅烷基酯并關注了其作為酰化試劑的效用。首先,我們發現了一個新的反應,其中路易斯酸催化劑的存在下,羧酸甲硅酯(親電子試劑)與烷基甲硅醚(親核試劑)之間發生一個親核取代反應得到相應的羧酸酯,產率很高(Scheme 1)。1)

然而,這個反應是一個直接的將羧酸甲硅酯到羧酸酯的酯交換反應,并且需要甲硅烷氧基到烷氧基轉換進程中的熱量。
在此階段,我們決定在溫和的條件下使用不同的試劑來重新研發衣蛾制備羧酸酯的替代方法。
比如乙酰氯,苯甲酰氯常用于醇的酰化,乙酸酐也可用作適當的酰化試劑。另一方面,芳香族的羧酸酐反應性特別的差,所以他們很少用于醇的直接苯甲酰化。因此,我們假定苯甲酸酐作為酰基供體反應活性屬性較低,相應的脂肪族羧酸酯可以從羧酸硅烷酯和烷基硅烷醚中選擇性的獲得(Scheme 2)。
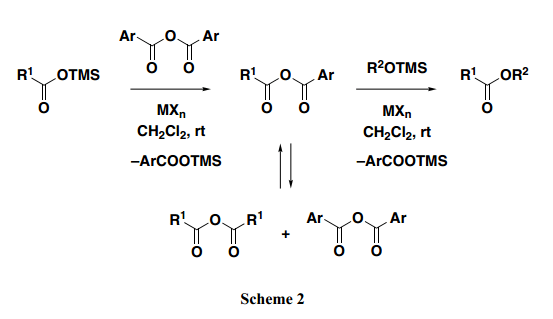
首先,酰基轉換反應在脂肪族羧酸硅烷酯和芳香族羧酸酐之間平穩進行。接著,混合酸酐部分快速的生成歧化為兩種類型的對稱酸酐,因此,這三種酸酐整體上在反應系統中必須快速的進入平衡混合狀態。由于通常情況下酸酐的反應性在對稱芳香族羧酸酐<對稱脂肪族羧酸酐<混合酸酐順序中逐漸增高,所以可以假定最活躍的酸酐與親核試劑優先反應。此外,如果混合酸酐中脂肪族酸酐部分的反應性高于芳香族酸酐部分的反應性,烷基甲硅烷基醚,必須優先攻擊的脂族酰基部分,得到相應的脂族羧酸酯,同時伴隨著芳族羧酸的甲硅烷基酯的消除。
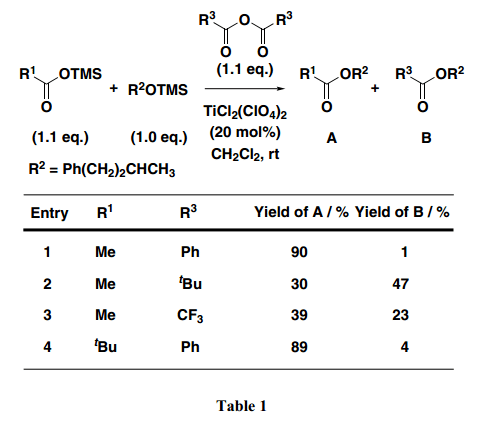
事實上,4-苯基-2-丁醇的三甲基硅烷醚加入預先準備好的混合酸酐中(使用TiCl2 (ClO4)2作為路易斯酸催化劑從乙酸三甲基硅烷酯和苯甲酸酐制得),得到所期望的酯A 90% 產率, 同時苯甲酸酐與三甲基硅烷基醚直接反應得到沒有計劃的酯B (1%產率)(Table 1, Entry 1)。結果顯示,第一階段的反應苯甲酸酐平穩進行轉換為混合酸酐,苯甲酸酯的形成速率比脂肪族酸酯慢得多。當使用其他可用酸酐時,得到同樣的實驗進程,結果如Entries 2–4所描述。盡管新戊醇或者三氟乙酸酐在合成肽中適用于制備混合酸酐的有效試劑,但是它們不適合用于縮合反應中。例如,在反應中使用酸酐,相當數量的不是預期期望的酯B(新戊酯或三氟酯)作為副產物成為意想不到的產物(Entries 2和3)。另一方面,如Entry 4所示, 新戊酸三甲基硅烷基酯使用苯甲酸酐轉換得到A,產率很好,結果顯示通常情況在這個條件下新戊酸酯會優先于苯甲酸酯形成。
3. 使用4-三氟甲基苯甲酸酐的酯化反應(TFBA)2)
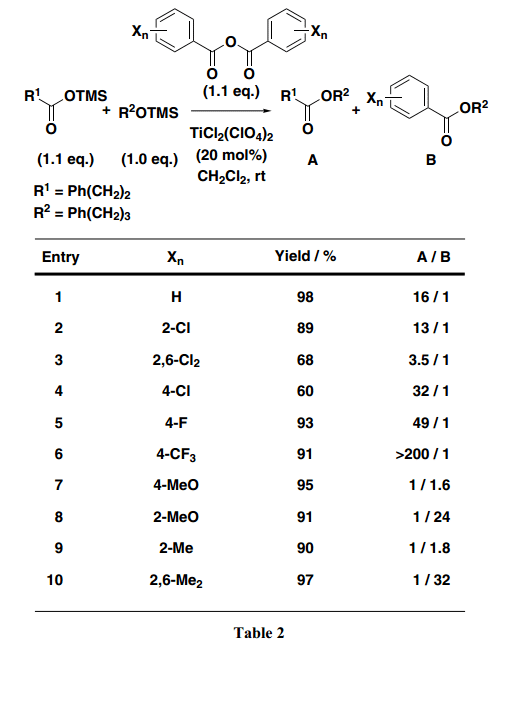
開發適合分子內縮合反應的合成方法,要求設計從幾乎等量的兩種起始原料中合成得到高產率目標產物。此外,為了提高環化產品的產率,很有必要開發一個新的合成具有完美選擇性的酯的方法。因此,我們嘗試在脫水縮合反應中在芳香環上引入多種取代基來增加其產率和選擇性(Table 2)。例如,Entry 1與Entries 4–6 相比較顯示出在芳香環4-位置處進入一個吸電子基團可以增加化學選擇性。特別是,使用4-三氟甲基酸酐(TFBA)的反應得到選擇性極好的預期產品脂肪族酸酯,并且通過NMR監測,幾乎沒有苯甲酸酯副產物生成。此外,如Entries 2和3所示,芳香環2-位置處引入氯產生相同或者略微弱些的選擇性。另一方面, 在使用具有甲氧基或者甲基基團的取代苯甲酸酐條件下,選擇性被逆轉,優先得到不需要的苯甲酸酯,而不是預期想要的脂肪羧酸酯(Entries 7–10)。從這些結果可以發現,在芳香環4-位置處引入一個強吸電子基團十分有效;特別是,具有一個三氟甲基基團的TFBA作為一個縮合試劑功能非常好。接下來,我們路易斯酸仔細研究了酯化功能的促進,比如Sn(OTf)2和TiCl2(OTf)2。結果發現,異丁酸、異戊酸、新戊酸和3-苯基丙酸三甲基硅烷酯與烷基三甲基硅烷酯快速反應得到相應并且幾乎等量的羧酸酯(Scheme 3)。此外,在TFBA存在下,酯化反應得到近90%或者更多的目標產物和不到約1 mol% 的路易斯酸。
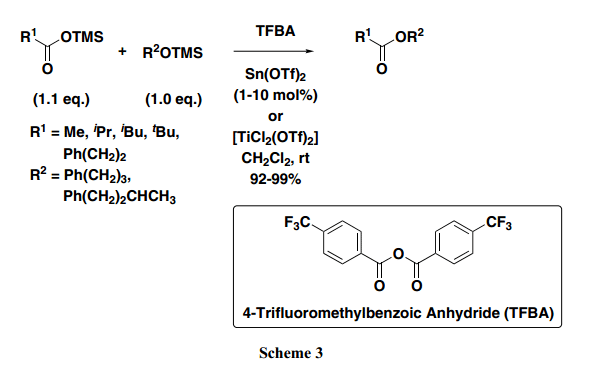
作為一個酯化方法的應用案例,合成高純度的共軛酸酯可得以實現。α,β-不飽和酯,比如巴豆酸、異戊烯酸和當硅酸酯在堿性條件下有進行異構化的可能性,這會造成產生副產物的麻煩。相反,在酯化反應中通過使用TFBA只有目標產物可以選擇性的獲得(Scheme 4)。2b)

此外,應當指出,TFBA在合成活性酯中也十分有效,比如硝基苯酚酯和苯硫酚酯2b,3)取代基酰苯胺,4)和芳香酮5)(Scheme 5)。此外,這個方法也可有效的用于將甲酰基引入吲哚環中以及傳統的方法比如Gattermann?Koch(加特曼-科赫反應)反應或者維爾斯邁爾反應中。因此,我們成功的開發了一個從甲酸直接制備3-甲酰基吲哚的有效方法(Scheme 6)。6)
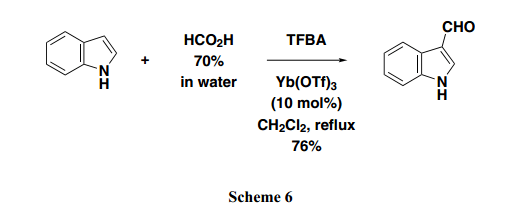
4.利用TFBA的ω-甲硅氧烷基羧酸硅酸酯內酯化反應7)
將縮合方法適用于分子內反應有意想不到的難度。事實上,雖然有越來越多新和成方法的報道,但是目前有效的內酯合成還是很少。這是因為在反應設計中低濃度條件下提高分子內反應,以及開發新的試劑可以激活酯的羥基或羧基基團的選擇性都很困難。為解決這些問題以合成天然產物的有效方法如下:(1) Mukaiyama?Corey method (S-pyridylester method);(2) Mukaiyama method (鎓鹽法);(3)正宗方法(硫醇酯活化法);(4)Yamaguchi method(2,4,6-三氯苯甲酰氯/Et3N/DMAP方法);(5)Steglich?Keck method(DCC/DMAP·HCl method)。
然而,所有的反應通常都必須在高溫該稀釋條件下進行,使得分子內反應優于分子間反應。在這樣的條件下,反應過程中使用不穩定的底物可以得到預期的環化產品,產率不好。我們嘗試通過TFBA處理內酯化ω-羥基羧酸硅烷基衍生物與期望的羧酸部分選擇性激活,從而導致所生成的混合酸酐快速的閉環。結果,化學選擇性激活得以實現,顯示最初由ω-羥基羧酸硅烷基酯和TFBA 所得的混合酸酐快速環化得到相應的大型內酯(Scheme 7)。這個方法使得制備13-元或更大型的內酯成為可能,并伴隨有一些小量的相關26-元中型或大型內酯。此外,路易斯酸催化劑活性按Sn(OTf)2< TiCl2(SbF6)2< TiCl2(OTf)2< TiCl2(ClO4)2順序依次增強。

5. 游離羧酸和醇通過使用TFBA和其類似物的縮合反應8)
在上訴反應中,要求必須預先從羧酸和醇中制備硅烷基衍生物。為了開發更為便利的方法,我們篩選了各類芳香酸酐作為有效的脫水試劑。雖然在開始時,有這樣的問題,反應過程中一些催化劑失活導致產率差勁,我們最終通過使用比TFBA具有更強吸電子基環的3,5-雙(三氟甲基)苯甲酸酐(BTFBA),得到了所需的羧酸酯,產率很好(Scheme 8)。
此外,通過使用3當量的三甲基氯硅烷,游離的羥基羧酸分子內脫水縮合得到所需的大環內酯,收益很好,類似于通過甲硅烷酯方法所得的情況。8b,9)在優化反應條件下,可使用市售TFBA代替內酯化。尤其是,12-羥基硬脂酸環化反應平穩進行,即使只有1mol%的路易斯酸條件下,得到產率為83%的13-元內酯(Scheme 9)。

此外,通過使用Group 4金屬三氟甲磺酸根, Hf(OTf)4 作為路易斯酸,在TFBA的存在下平穩的極性宏酯化反應得到相應的內酯。另外,值得注意的是,中型環恩子也可以通過該方法得到。例如,通過采用這個方法Cephalosporolide D的8-元環內酯部分的合成得以成功的實現(Scheme 10)。10)

6. 使用2-甲基-6-硝基苯甲酸酐(MNBA)的酯合成11)
上述 “取代基苯甲酸酐方法”對制備耐酸性分子非常有效,然而,這在合成多官能團天然產物方面仍然有很多的結構性限制。因此,我們更為嚴密的篩選出新型的芳香族羧酸酐,堿性條件下可以通過親核催化劑如DMAP 進行激活(Table 3)。如Entry 1所示,反應使用無取代苯甲酸酐得到目標脂肪族羧酸酯,中等產率,化學選擇性好(A/B=100/1)。此外,當甲氧基基團引入到芳香環4-位置處時,化學選擇性得到改善,然而,目標酯A 產率降低,因為反應抑制作用(Entry 2)。 此外,如Entries 3和4所示,芳香環4-位置處通過使用具有吸電子基的取代苯甲酸酐,例如TFBA,反應速率顯著提高,然而,反應中也會有2–4% 產率的副產物取代基苯甲酸酯B生成。

考慮查到這樣的結果,我們在芳香環2-位置處對取代基效果做了進一步的檢測,期望羰基周圍的位阻影響可以改進化學選擇性。在Entries 5–7,我們嘗試通過使用2-位置或者2-和6-位置具有吸電子基團甲基或者甲氧基的取代基苯甲酸酐合成羧酸酯。這些反應整體上顯示出良好的選擇性,將副產物B產率降至1%或者更少。然而,由于反應性降低,這個條件的結果對內酯化仍然不足。兩外, Entries 8和9所示,反應中使用2-和6-位置處都具有氯的芳香酸酐,混合酸酐生成,酯化反應順利進行,然而,與使用TFBA相比,化學選擇性沒有得到改善。這些結果表明方向換上有吸電子基團對于高反應速率非常重要,另一方面 芳香環2-位置處引入給電子集團會出現高的化學選擇性。基于這些現象的考慮,我們設計了2-甲基-6-硝基苯甲酸酐(MNBA),希望通過利用它改善反應性和化學選擇性來足以的應用于分子內的反應。當我們使用MNBA(由2-甲基-6-苯甲酸)時,在當前的反應模板中,人們發現,所需的縮合反應快速進行,并且沒有副產物2-甲基-6-硝基苯甲酸酯的生成(Entry 10)。
我們一直在不斷的研究天然產物的合成,使用各種基材利用MNBA 方法極性分子內和分子間的縮合反應。在很多情況下,所需產物的合成產率會高于其他很多現有的合成方法,基質的一般性驗證了我們的方法。如下圖所示,利用MNBA成功的實現antibacterial Botcinic Acid的全合成(Scheme 11)。12)

7. 使用MNBA和其類似物的內酯化反應11b,13)
自從我們發現了使用MNBA的有效分子間縮合的最佳條件,我們也采用這個方法來分子內縮合。反應過程只需要將ω –羥基羧酸溶液室溫下通過注射泵緩慢加入MNBA和DMAP溶液中(二氯甲烷或甲苯作溶劑)。在這些反應調價下,混合酸酐生成逐漸進行,并得到相應的內酯。因此,反應過程中MA的濃度始終很低,這種高稀釋條件下提高了單體選擇性。此外,MA激活可以在室溫下完成,代替回流條件,這是一個簡單的程序,通過親核試劑阻止基料的降解 。值得注意的是我們成功的合成了2-Epibotcinolide的9-元內酯部分,首先假定Botcinin E化合物是通過應用MNBA方法而得(Scheme 12)。14)
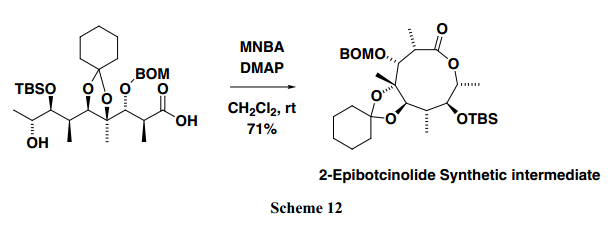
當MNBA方法被用于制備紅霉素A苷元時,定量的產率得到所需的14-元內酯。15) 根據以往的紅霉素A苷元合成的報道,知道環化效率不同源于seco acid 引入的前體保護基團。如Scheme 13所示,seco acid的內酯化,它具有一個適合閉環的結構,室溫下段時間內能夠快速的進行生成定量的紅霉素A苷元。值得注意的是,即使是20 mol%的DMAP活化劑,也足夠用來內酯化。具有類似于seco acid結構的原料的環化反應一直以來被認為得不到所需的內酯,然而,使用MNBA加熱條件下的內酯化取得了令人滿意的所需內酯。
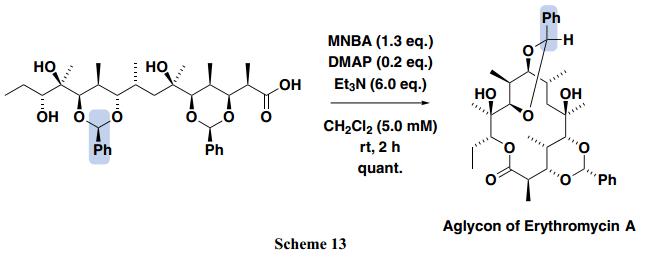
這個方法更適合用于大型內酯的合成,例如,一個seco-acid 唄成功的轉換為相應的25-元α-氧代內酯。這個中間酯最后脫保護得到2-hydroxytetracosanolide,昆蟲白蟻的防御性唾液分泌(Scheme 15)。16)

此外,篩選出具有各種吸電子基芳香酸酐之后,人們發現,通過使用2,6-二甲基-4-硝基苯甲酸酐(DMNBA),其2-和6-位置具有甲基,并且4-位置處具有一個強吸電子基,可以得到相應的羧酸酯和內酯,產率很好,并且相當于使用MNBA的量。由于使用MNBA 和DMNBA 的反應通常情況下在溫和條件下進行,具有多個羥基的達到區域選擇性seco-acid成功環化。如下圖所示,人造麝香化合物 (9E)-異黃葵內酯在三個步驟中從非保護的油桐酸中成功制得,產率為66% (Scheme 16)。17)
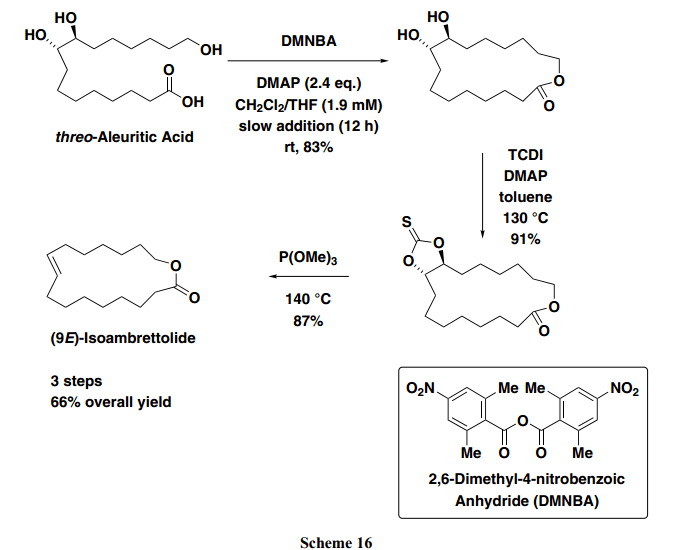
8.具有活性優于DMAP 的吡啶N-氧催化劑DMAPO的發展
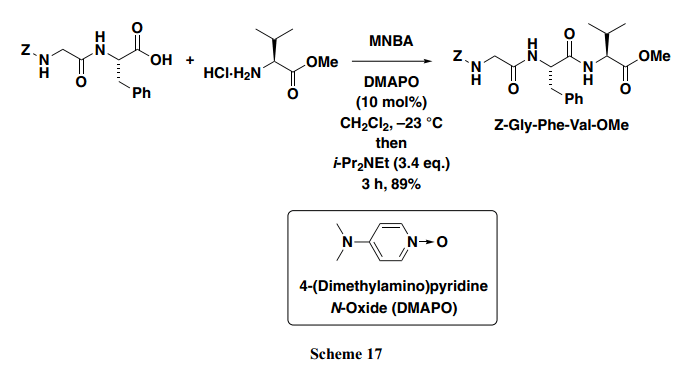
MNBA和DMAP的組合使得從羧酸和胺中合成羧酸酰胺成為可能。然而,這個方法中肽偶合的應用不合實際,由于其外消旋作用。堿性條件下篩選合適的催化劑交替DMAP后,發現4-二甲基氨基吡啶N-氧化物(DMAPO),已被用于有機磷酸酯類化合物的合成,可以有效地應用于肽偶合。例如,Z-Gly-Phe與Val-OMe 反應得到相應的肽,并沒有外消旋作用(Scheme 17)。18)
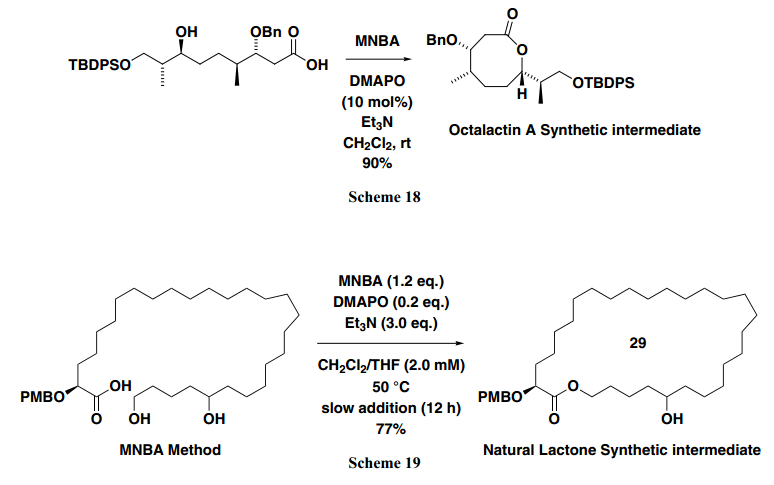
有這些結果人們發現,通過使用芳香族羧酸酐作為縮合試劑,DMAPO是一個極好的內酯化催化劑。如下所示為Octalactin A,一個抗腫瘤海洋內酯的全合成, DMAPO(2–10 mol%)的催化量有效地使得8-元環部分形成,得到所需的中間體,產率高達90%(Scheme 18)。19)
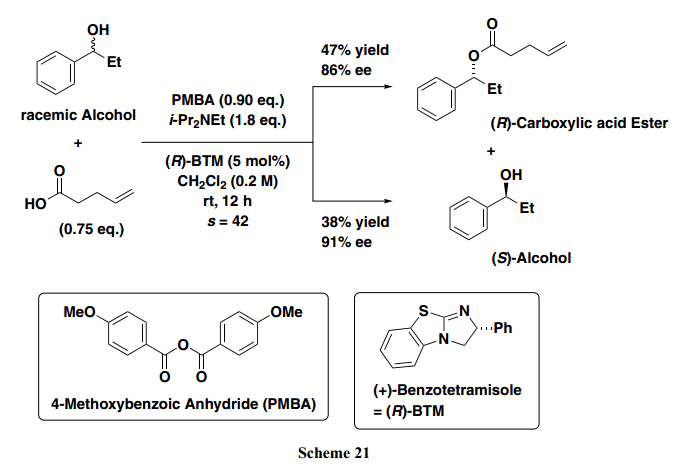
MNBA/DMAPO方法也可成功的引入大型宏內酯的形成(Scheme 19)。13b,16,20)如下所示,通過MNBA和DMAPO的結合成功的實現白蟻防御性唾液分泌的合成, 得到相應的單羥基內酯,產率高,區域選擇性好。通常,seco acid,具有較少取代基長,趨于穩定的線性結構防止內酯形成。因此,通過我們的方法可以成功的獲得所需的大環內酯,產率極好(77%)。另一方面,當我們與Yamaguchi method 作比較時,后者產率僅為29% (Scheme 20)。

9.使用芳香族酸酐作為縮合劑的不對稱酯化反應的發展21-23)
前面的章節中,非手性親核試劑用作促進劑。考慮到在不對稱合成中進一步的應用,我們決定篩選出手性親核試劑代替DMAP。由Birman等人推廣的(+)-苯并四咪唑 [(R)-BTM]24) 是一個很好的不對稱催化劑可以滿足我們的目的需求。通過和我們的脫水耦合方法相結合,對應選擇性酯化可以實現。事實上,在4-甲氧基苯甲酸酐(PMBA)或苯甲酸酐的存在下, 外消旋二級芐醇與非手性羧酸反應得到過量的相應的(R)-羧酸酯和(S)-仲醇對映體(Scheme 21)。21)
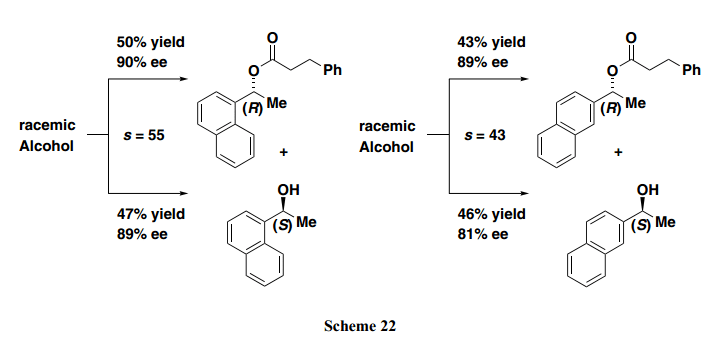
1-(α-萘基)-1-乙醇和1-(β-萘基)-1-乙醇與(R)-BTM和 苯甲酸酐的動力學拆分可以成功的完成,具有良好的s –值,分別為55和43(Scheme 22)。這里的s 值是表示兩種對映體之間反應速率比的一個因素。通常,如果s值超過20,動力學拆分實際上是有用的。例如,在外消旋1-(α-萘基)-1-乙醇的反應中,(R)-酯成功獲得,產率為50%(90% ee)。此外,剩余的(S)-醇也可以47%產率回收(89% ee)。
通過這種新穎的不對稱催化,很有可能建立一個外消旋羧酸動力學拆分的新的方法。篩選適合這個目標的非手性醇之后,發現雙(α-萘基)甲醇是一個非常好的親核試劑。事實上,PMBA或苯甲酸的催在下,當外消旋2-芳基丙醇與雙(α-萘基)甲醇反應進行時,不對稱脫水反應順利進行,得到高產率高對映體的目標產物 (R)-羧酸酯,以及剩余的具有中等對映選擇性的(S)-2-苯基丙酸(Scheme 23)。22)

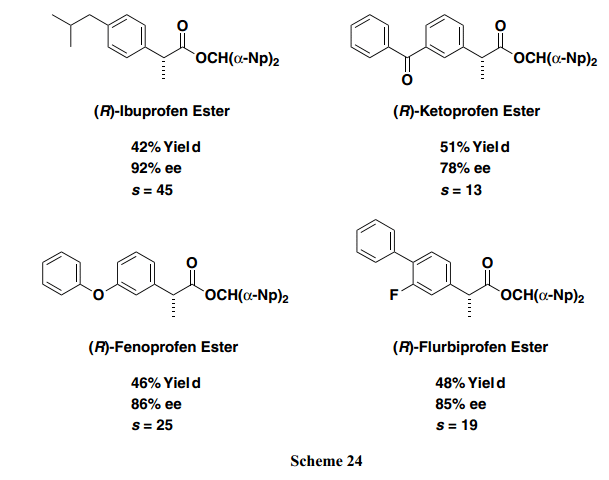
具有2-芳基丙酸部分作為基礎結構的化合物被廣泛的用作非甾體類抗炎藥 (NSAIDs)。我們還成功的建立了一個新的合成方法,該方法提供光學活性NSAIDs和高選擇性的酯衍生物(Scheme 24)。22)此外,所得雙(α-萘基)甲基酯常規條件下很容易氫化裂解,光學純度沒有任何損失。因此,所得的手性羧酸酯可以被認為是游離羧酸的前體。
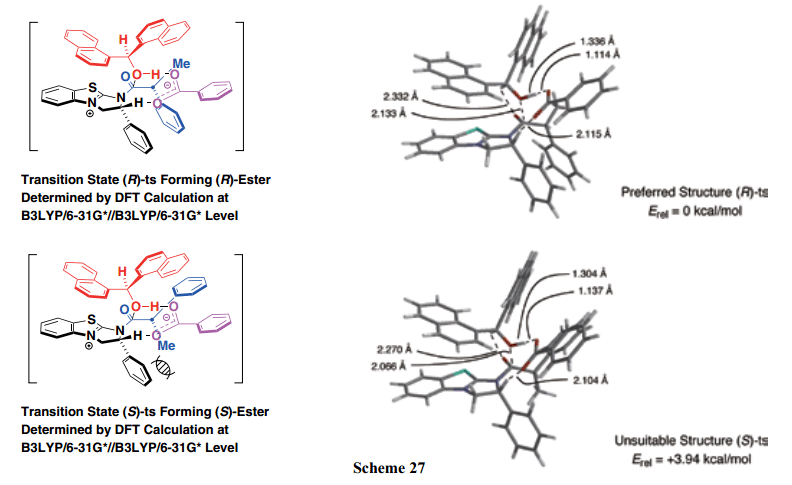
此外,我們成功的研發了(S)-β -Np-BTM, 一個新型親核催化劑,優化了外消旋α –芳基丙酸的動力學拆分。(S)-β-Np-BTM的使用時的外消旋萘普生有效地動力學拆分,其中最終得到(S)-萘普生,一個高光學純度抗炎物質(Scheme 25)。22)T外消旋羧酸動力學拆分的可能途徑如下所示(Scheme 26):親核催化劑存在下,苯甲酸酐和外消旋羧酸堿性條件下快速進行反式酰基化反應得到外消旋混合酸酐(MA),暫時形成一個關鍵的中間體。在這兩個對映異構體中,混合酸酐通過(R)-BTM 優先激活從(R)-羧酸中生成[(R)-MA],然后,與雙(α–萘基)甲醇反應選擇性得到相應的(R)-羧酸酯。另一方面,由(S)-羧酸得來的混合酸酐[(S)-MA]仍舊沒有反應。為了支持上述預測的機制,我們確定的優選的兩個過渡態(R)-ts和(S)-ts((R)-和(S)-羧酸中衍生得來)分別通過使用密度泛函理論(DFT)在B3LYP/6-31G*//B3LYP/6-31G*水平計算。這些過渡態的能量比較表明(R)-ts的能量低于(S)-ts。如Scheme 27所示,由于(S)-ts的α –位置處的甲基取代部分和BTM C-2位置處的苯基基團之間的空間排斥,(S)-ts穩定性降低,并且所需的(R)-羧酸選擇性獲得。因此,我們通過使用計算化學方法已經公開了不對稱縮合反應中enantio-discrimination的反應機制和起源。


10. 結論
總之,我們簡要概述了我們實驗室中所研究的脫水縮合反應的發展。闡明了芳香族羧酸酐(室溫下穩定易處理的花歌舞)的功能,與足夠的催化劑結合使用可以用作高反應性能的偶合試劑。TFBA 或BTFBA與酸性催化劑組合,或者MNBA 或DMNBA與親核催化劑結合,堿性條件下適用于羧酸酯和內酯的合成。TFBA 和MNBA都有市售,建議您嘗試一下。另一方面,DMAPO, 這個新型的催化劑也發揮了有效地作用。DMAPO水合物形式也有市售,可以用于比如升華的脫水過程。DMAPO催化能力高于DMAP,值得注意的是,通過使用DMAPO,各種肽類可以得到制備,并且可以沒有明顯的外消旋環化。因此,游離羧酸和醇不對稱偶合中,PMBA或苯甲酸酐功能可以用作一個有效地脫水縮合試劑。23) 使用這些組合與不對稱催化劑(R)-BTM或(S)-β-Np-BTM很容易的獲得各種光學活性酯,羧酸和醇。
最后,我們將不勝感激更多的研究人員使用并評估該方法,我們希望我們的研究結果將有助于有機化學合成的發展。
References
1) I. Shiina, T. Mukaiyama, Chem. Lett. 1992, 2319-2320.
2) (a) T. Mukaiyama, I. Shiina, M. Miyashita, Chem. Lett. 1992, 625-628. (b) M. Miyashita, I. Shiina, S. Miyoshi, T. Mukaiyama, Bull. Chem. Soc. Jpn. 1993, 66 , 1516-1527.
3) T. Mukaiyama, M. Miyashita, I. Shiina, Chem. Lett. 1992, 1747-1750.
4) (a) M. Miyashita, I. Shiina, T. Mukaiyama, Chem. Lett. 1993, 1053-1054. (b) M. Miyashita, I. Shiina, T. Mukaiyama, Bull. Chem. Soc. Jpn. 1994, 67, 210-215.
5) (a) T. Mukaiyama, K. Suzuki, Chem. Lett. 1992, 1751-1754. (b) K.Suzuki,H. Kitagawa, T. Mukaiyama,Bull. Chem. Soc. Jpn. 1993, 66 , 3729-3734.
6) I. Shiina, M. Miyashita, M. Nagai, T. Mukaiyama, Heterocycles 1995, 40 , 141-148.
7) T. Mukaiyama, J. Izumi, M. Miyashita, I. Shiina, Chem. Lett. 1993, 907-910.
8) (a) I. Shiina, S. Miyoshi, M. Miyashita, T. Mukaiyama, Chem. Lett. 1994 , 515-518. (b) I. Shiina, Tetrahedron 2004 , 59, 1587-1599.
9) I. Shiina, T. Mukaiyama, Chem. Lett. 1994, 677-680.
10) (a) I. Shiina, Y. Fukuda, T. Ishii, H. Fujisawa, T. Mukaiyama, Chem. Lett. 1998, 831-832. (b) I. Shiina, H. Fujisawa, T. Ishii, Y. Fukuda, Heterocycles 2000 , 52 , 1105-1123.
11) (a) I. Shiina, R. Ibuka, M. Kubota, Chem. Lett. 2002, 286-287. (b) I. Shiina, M. Kubota, H. Oshiumi, M.Hashizume, J. Org. Chem. 2004, 69 , 1822-1830. See also, (c) I. Shiina, Yuki Gosei Kagaku Kyokaishi (J. Synth. Org. Chem. Jpn.), 2005, 63 , 2-17.
12) (a) H. Fukui, S. Hitomi, R. Suzuki, T. Ikeda, Y. Umezaki, K. Tsuji, I. Shiina, Tetrahedron Lett. 2008, 49 , 6514-6517. [Cover Feature Article] See also, (b) H. Fukui, I. Shiina, Org. Lett. 2008, 10, 3153-3156. (c) H. Fukui, I. Shiina, Yuki Gosei Kagaku Kyokaishi (J. Synth. Org. Chem. Jpn.), 2009, 67 , 628-642.
13) (a) I. Shiina, M. Kubota, R. Ibuka, Tetrahedron Lett. 2002, 43, 7535-7539. See also, (b) I. Shiina, H. Fukui, A. Sasaki, Nat. Protoc. 2007, 2, 2312-2317. (c) I. Shiina, Chem. Rev. 2007, 107, 239-273 .
14) (a) I. Shiina, Y. Takasuna, R. Suzuki, H. Oshiumi, Y. Komiyama, S. Hitomi, H. Fukui, Org. Lett. 2006, 8, 5279-5282. (b) I. Shiina, H. Fukui, Chem. Commun. 2009, 385-400. [Feature Article]
15) I. Shiina, T. Katoh, S. Nagai, M. Hashizume, Chem. Rec. 2009, 9, 305-320.
16) I. Shiina, A. Sasaki, T. Kikuchi, H. Fukui, Chem. Asian J. 2008, 3, 462-472.
17) (a) I. Shiina, R. Miyao, Heterocycles 2008, 76 , 1313-1328. See also, (b) I. Shiina, M. Hashizume, Tetrahedron 2006, 62, 7934-7939.
18) (a)I. Shiina, H. Ushiyama, Y. Yamada,Y.Kawakita,K. Nakata,Chem. Asian J. 2008, 3, 454-461. See also, (b) I. Shiina, Y. Kawakita, Tetrahedron 2004,60 , 4729-4733.
19) (a) I. Shiina, H. Oshiumi, M. Hashizume, Y. Yamai, R. Ibuka, Tetrahedron Lett. 2004, 45 , 543-547. (b) I. Shiina, M. Hashizume, Y. Yamai, H. Oshiumi, T. Shimazaki, Y. Takasuna, R. Ibuka, Chem. Eur. J. 2005, 11 , 6601-6608.
20) I. Shiina, T. Kikuchi, A. Sasaki, Org. Lett. 2006, 8, 4955-4958.
21) I. Shiina, K. Nakata, Tetrahedron Lett. 2007, 48 , 8314-8317. [Cover Feature Article]
22) (a) I. Shiina, K. Nakata,Y.Onda, Eur.J.Org.Chem. 2008, 5887-5890. (b) I. Shiina, K. Nakata, K.Ono, Y. Onda,M.Itagaki, J. Am. Chem. Soc. 2010, 132, 11629-11641.
23) For the asymmetric esterification, bulky fatty-chain carboxylic anhydrides, such as pivalic anhydride, are also effective as dehydrating reagents. See: (a) I. Shiina, K. Nakata, M. Sugimoto, Y. Onda, T. Iizumi, K. Ono, Heterocycles 2009 , 77 , 801-810. (b) I. Shiina, K. Nakata, K. Ono, M. Sugimoto, A. Sekiguchi, Chem. Eur. J. 2010, 16 , 167-172.
24) (a) V. B. Birman, X. Li, Org. Lett. 2006, 8, 1351. (b) V. B. Birman, L. Guo, Org. Lett. 2006, 8, 4859.
注:本文為提供者整理翻譯的,由于知識所限,錯誤在所難免,敬請原諒。如有問題可以查找原文。
統計數據
共收錄化學品數據
147579 條



 滬公網安備 31010602001115號
滬公網安備 31010602001115號