二苯乙炔 Diphenylacetylene

結(jié)構(gòu)式
| 物競編號 | 057P |
|---|---|
| 分子式 | C14H10 |
| 分子量 | 178.23 |
| 標(biāo)簽 | 二苯基乙炔, 二苯乙炔 |
編號系統(tǒng)
CAS號:501-65-5
MDL號:MFCD00004786
EINECS號:207-926-6
RTECS號:暫無
BRN號:606478
PubChem號:24866731
物性數(shù)據(jù)
1. 性狀:無色固體
2. 密度:0.990 g/cm3
3. 晶相標(biāo)準(zhǔn)熱熔(J·mol-1·K-1):226
4. 熔點(oC):62.5
5. 沸點(oC,0.3 mmHg):90~97
6. 晶相相標(biāo)準(zhǔn)燃燒熱(焓)(kJ·mol-1):-7250.7
7. 晶相標(biāo)準(zhǔn)聲稱熱(焓)( kJ·mol-1):312.4
8. 閃點(oC):170
9. 比旋光度(o):未確定
10. 自燃點或引燃溫度(oC):未確定
11. 蒸氣壓(kPa,25oC):未確定
12. 飽和蒸氣壓(kPa,60oC):未確定
13. 燃燒熱(KJ/mol):未確定
14. 臨界溫度(oC):未確定
15. 臨界壓力(KPa):未確定
16. 油水(辛醇/水)分配系數(shù)的對數(shù)值:未確定
17. 爆炸上限(%,V/V):未確定
18. 爆炸下限(%,V/V):未確定
19. 溶解性:溶于乙醚、熱的乙醇。
毒理學(xué)數(shù)據(jù)
生態(tài)學(xué)數(shù)據(jù)
該物質(zhì)對環(huán)境可能有危害,對水體應(yīng)給予特別注意。
分子結(jié)構(gòu)數(shù)據(jù)
1、 摩爾折射率:58.73
2、 摩爾體積(cm3/mol):166.6
3、 等張比容(90.2K):434.8
4、 表面張力(dyne/cm):46.3
5、 極化率(10-24cm3):23.28
計算化學(xué)數(shù)據(jù)
1.疏水參數(shù)計算參考值(XlogP):無
2.氫鍵供體數(shù)量:0
3.氫鍵受體數(shù)量:0
4.可旋轉(zhuǎn)化學(xué)鍵數(shù)量:2
5.互變異構(gòu)體數(shù)量:無
6.拓?fù)浞肿訕O性表面積0
7.重原子數(shù)量:14
8.表面電荷:0
9.復(fù)雜度:193
10.同位素原子數(shù)量:0
11.確定原子立構(gòu)中心數(shù)量:0
12.不確定原子立構(gòu)中心數(shù)量:0
13.確定化學(xué)鍵立構(gòu)中心數(shù)量:0
14.不確定化學(xué)鍵立構(gòu)中心數(shù)量:0
15.共價鍵單元數(shù)量:1
性質(zhì)與穩(wěn)定性
1.按規(guī)格使用和貯存,不會發(fā)生分解,避免與氧化物接觸。
2.低毒,可通過皮膚吸收。
貯存方法
密封保存,放置在通風(fēng),干燥的環(huán)境中。
合成方法
1.制法:

苯偶酰腙(3):于裝有攪拌器、回流冷凝器的反應(yīng)瓶中,加入二苯乙二酮(2)105.1g(0.5mol),正丙醇325mL,85%的水合肼76g(1.3mol),加熱回流60h。冷后抽濾,用冷的無水乙醇洗滌,干燥,得苯偶酰腙(3)99~106g,mp150~151.5℃,收率83%~89%。二苯乙炔(1):于裝有攪拌器、回流冷凝器的反應(yīng)瓶中,加入上述化合物(3),480mL苯,攪拌下加入黃色氧化汞2~4g,微微加熱,有氮氣放出,反應(yīng)物變灰色。加熱至微沸,不斷加入氧化汞2~4g,總共加入氧化汞240g(1.1mol)。加完后繼續(xù)攪拌1h。放置過夜。抽濾,濾餅用100mL苯洗滌。合并苯溶液,水洗,無水硫酸鈉干燥,減壓回收苯后高真空蒸餾,收集95~105℃/27~40Pa的餾分,得二苯乙炔①(1)60~65g,收率67%~73%。產(chǎn)品可用100mL(95%)的乙醇重結(jié)晶提純。注:①利用類似方法可以制備二對甲苯基乙炔(C16H14)、a-萘基苯基乙炔(C18H12)。[1]
用途
二苯乙炔是取代茋和偶苯酰的合成前體[1],可以進行環(huán)加成反應(yīng)。由于對稱性和高度的平面性,二苯乙炔是非常好的Lewis酸,在金屬有機化學(xué)中也是很好的配體。
氧化及還原 二苯乙炔可以被鉬(VI)和鎢(VI)的多氧金屬、[二(三氟乙酸)碘代]五氟苯氧化生成安息香酸。鉻族絡(luò)合物、鋅-鉻、錳酸鋇以及其它試劑可使二苯乙炔氧化成偶苯酰[2]。
二苯乙炔的有效還原方法如下:可用NiCl2·4PPh3酸制備反式茋,在釕催化劑作用下發(fā)生氫化反應(yīng)生成順式茋,也可用CoCl2·4PPh3、SmI2、AcOH或用鋅與Pd/C結(jié)合來完成[3],利用氫和蒙脫石-(二苯基膦化氫)鈀(II)絡(luò)合物或用鋅與Pd/C結(jié)合可將炔鍵還原成烷烴。
炔烴π鍵與X-Y的加成 很多試劑可對炔鍵加成。例如,RS-Cl (式1)[4]、PhSe-F、Me3Sn-PPh2、PhS-F、PhS-SPh和ClHg-OAc可與二苯乙炔發(fā)生反式加成,而Bu3Sn-H (式2)[5]、RNH-H和HO2C-H則會生成順式芪衍生物。H-CN、TMS-CN、X2 (X=鹵素)、Et-AlEt2等也可與二苯乙炔加成。
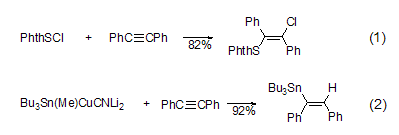
卡賓加成 二苯乙炔可與鉻、鎢和卡賓鈷等發(fā)生加成反應(yīng)。Fischer類型卡賓鉻與二苯乙炔反應(yīng)生成環(huán)戊酮。而卡賓鉻中含氮時可以得到吡咯啉酮 (式3)[6]。Fischer類型的卡賓鎢可直接反應(yīng),因為可以形成七元環(huán) (式4)[7]。
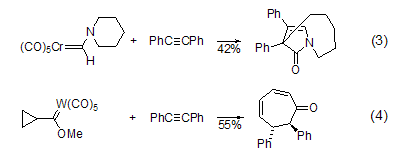
與不同金屬的相互作用 二苯乙炔可用于鈀催化偶合反應(yīng)和環(huán)化反應(yīng)中 (式5)[8],而鎳則可以形成螺環(huán)化合物 (式6)[9],鋅絡(luò)合物的插入則可生成許多不飽和分子。二苯乙炔有和有機金屬絡(luò)合物及有機金屬簇結(jié)合的傾向,并能進行金屬化反應(yīng)。

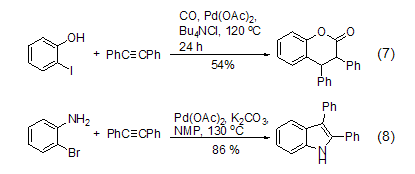
環(huán)的形成及環(huán)加成 二苯乙炔可通過環(huán)加成反應(yīng)來制備酯(式7)[10]、唑、苯并噻吩、吲哚(式8)[11]、吡咯和呋喃-2(5H)-酮等化合物及其衍生物。
安全信息
危險運輸編碼:暫無
危險品標(biāo)志:暫無
安全標(biāo)識:暫無
危險標(biāo)識:暫無
文獻
[1]參考文獻:1、Cope A C,Smith D S,Cotter R J.Org Synth,1963,Coll Vol 4:377. 2、林原斌,劉展鵬,陳紅飆.有機中間體的制備與合成.北京:科學(xué)出版社,2006:108. 參考書:有機化合物合成手冊/孫昌俊,王秀菊,孫風(fēng)云主編. 北京:化學(xué)工業(yè)出版社,2011.8 ISBN 978-122-11519-53. Shosenji, H.; Nakano, Y.; Yamada, K. Chem. Lett., 1988, 1033. 4. Capozzi, G.; Gori, L.; Menichetti, S.; Nativi, C. J. Chem. Soc., Perkin Trans.1, 1992, 1923. 5. Barbero, A.; Cuadrado, P.; Fleming, I.; Gonzalez, A.; Pulido, F. Chem. Commun., 1992, 351. 6. Parlier, A.; Rudler, H.; Yefsah, R.; Alvarez, C. J. Organomet. Chem., 1987, 328, C21. 7. Herndon, J.; Chatterjee, G.; Patel, P.; Matasi, J.; Tumer, S.; Harp, J.; Reid, M. J. Am. Chem. Soc., 1991, 113, 7808. 8. (a) Silverberg, L.; Wu, G.; Rheingold, A.; Heck, R. J. Organomet. Chem., 1991, 409, 411. (b) Wu, G.; Rheingold, A.; Geib, S.; Heck, R. Organometallics, 1987, 6, 1941. 9. Kong, K.; Cheng, C. Organometallics, 1992, 11, 1972. 10. Dmitry, V. K.; Richard, C. L. J. Org. Chem., 2003, 68, 9423. 11. Shen, M.; Li, G. S.; Lu, B. Z.; Hossain, A.; Roschangar, F.; Farina, V.; Senanayake, C. H. Org. Lett., 2004, 6, 4129. 12.參考書:現(xiàn)代有機合成試劑<性質(zhì)、制備和反應(yīng)>;胡躍飛 付華 編著;化學(xué)工業(yè)出版社;ISBN 7-5025-8542-7
備注
暫無
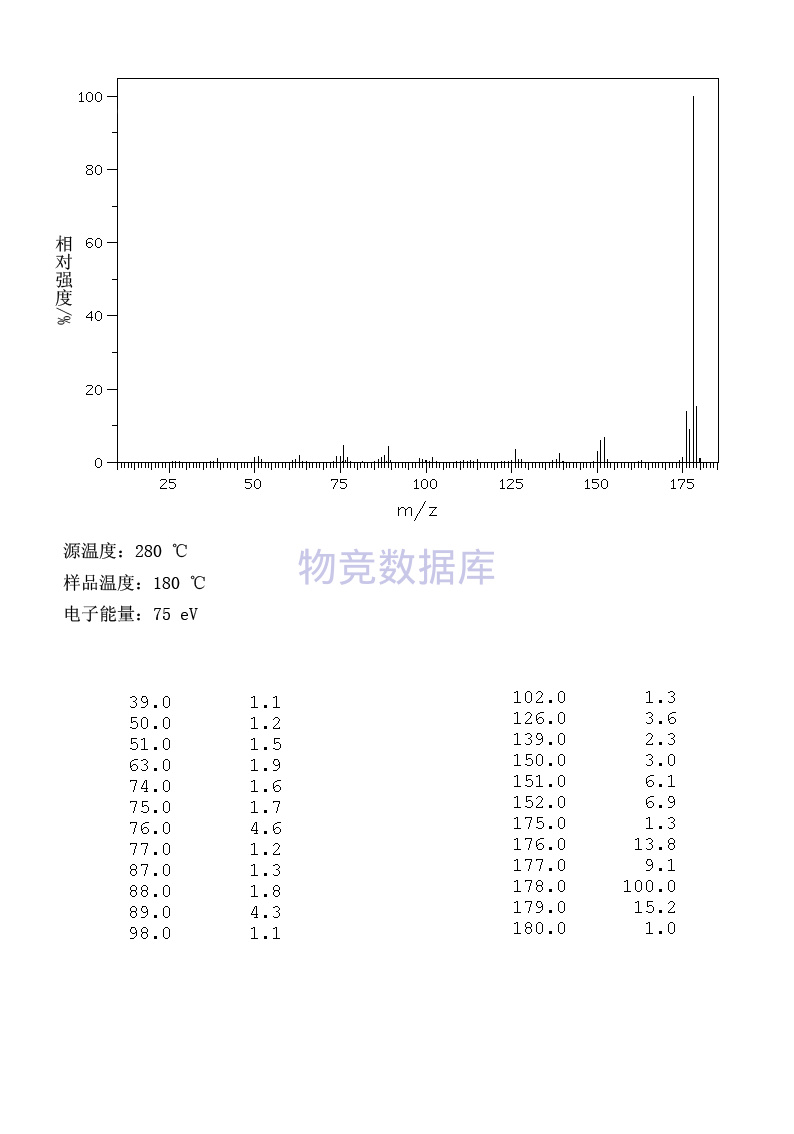
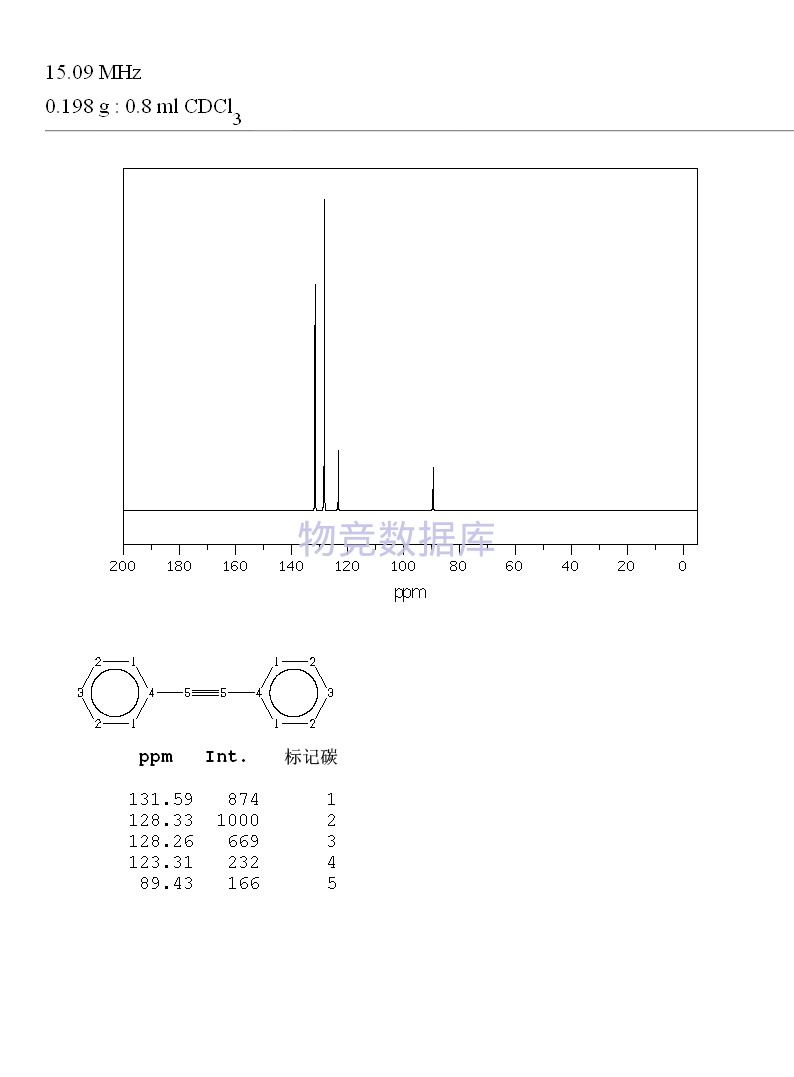
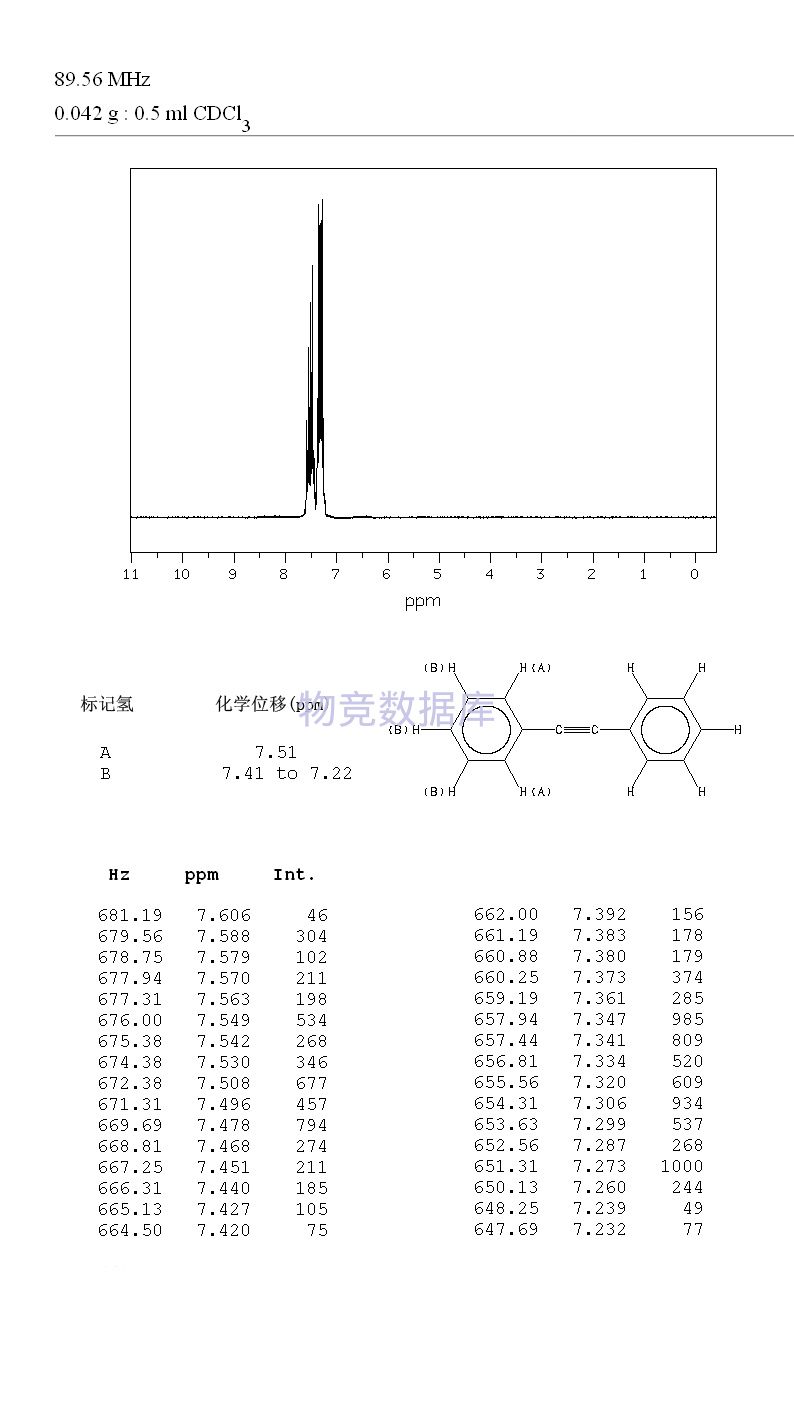
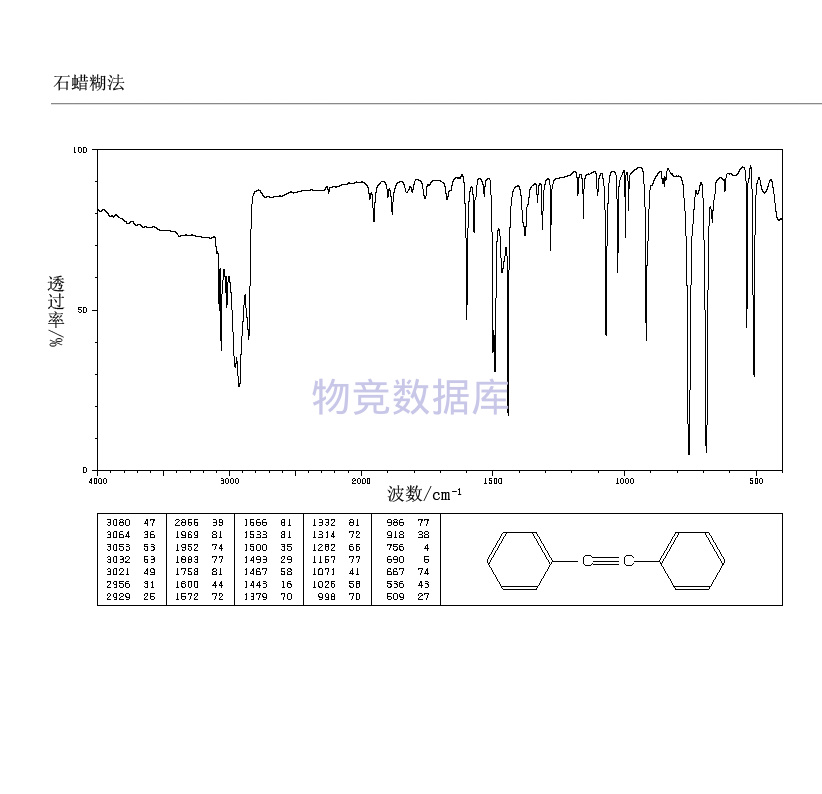
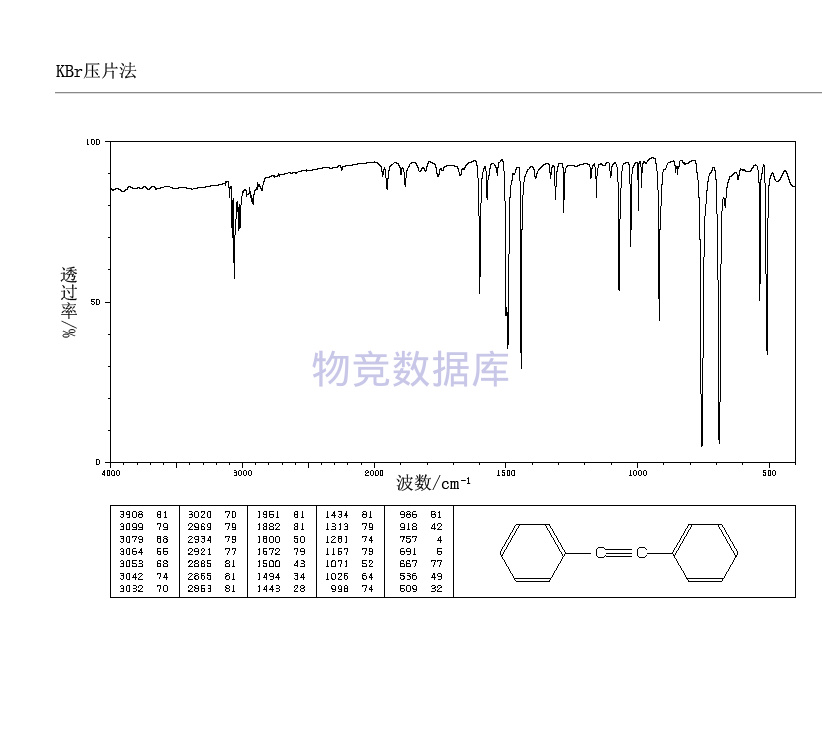
表征圖譜
統(tǒng)計數(shù)據(jù)
共收錄化學(xué)品數(shù)據(jù)
147579 條




 滬公網(wǎng)安備 31010602001115號
滬公網(wǎng)安備 31010602001115號