四氟化鈾 Uranium tetrafluoride
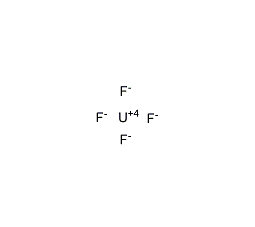
結(jié)構(gòu)式
| 物競(jìng)編號(hào) | 011F |
|---|---|
| 分子式 | UF4 |
| 分子量 | 314.02 |
| 標(biāo)簽 | 鈧族元素 |
編號(hào)系統(tǒng)
CAS號(hào):10049-14-6
MDL號(hào):暫無
EINECS號(hào):233-170-1
RTECS號(hào):暫無
BRN號(hào):暫無
PubChem號(hào):暫無
物性數(shù)據(jù)
暫無
毒理學(xué)數(shù)據(jù)
暫無
生態(tài)學(xué)數(shù)據(jù)
暫無
分子結(jié)構(gòu)數(shù)據(jù)
暫無
計(jì)算化學(xué)數(shù)據(jù)
1.疏水參數(shù)計(jì)算參考值(XlogP):無
2.氫鍵供體數(shù)量:0
3.氫鍵受體數(shù)量:4
4.可旋轉(zhuǎn)化學(xué)鍵數(shù)量:0
5.互變異構(gòu)體數(shù)量:無
6.拓?fù)浞肿訕O性表面積0
7.重原子數(shù)量:5
8.表面電荷:0
9.復(fù)雜度:19.1
10.同位素原子數(shù)量:0
11.確定原子立構(gòu)中心數(shù)量:0
12.不確定原子立構(gòu)中心數(shù)量:0
13.確定化學(xué)鍵立構(gòu)中心數(shù)量:0
14.不確定化學(xué)鍵立構(gòu)中心數(shù)量:0
15.共價(jià)鍵單元數(shù)量:1
性質(zhì)與穩(wěn)定性
綠色針狀晶體,單斜晶系,晶格常數(shù)a0=(12.73±0.01)A(1A=0.1nm,下同),b0=(10.753±0.007)A,c0=(8.404±0.008)A,β=(126.33±0.05)°。熔點(diǎn)(960±5)℃,沸點(diǎn)1415℃,密度為(6.70±0.10)g/cm3。難溶于水,不溶于稀酸和稀堿,溶于濃酸和濃堿。可與堿金屬氟化物形成各種復(fù)鹽。
貯存方法
暫無
合成方法
制法1 UO2+4HF→UF4+2H2O【250~270℃反應(yīng)溫度】
二氧化鈾與氟化氫反應(yīng)可生成四氟化鈾,但同時(shí)此反應(yīng)也可以逆向進(jìn)行,所以反應(yīng)過程中要及時(shí)除去生成的水。
由于二氧化鈾易被氧化生成高氧化態(tài)化合物,而高氧化態(tài)氧化物用氟化氫進(jìn)行氟化時(shí),可生成UO2F2,則將使四氟化鈾的純度下降,所以反應(yīng)前二氧化鈾要預(yù)先在氫氣流中,于800~900℃下進(jìn)行還原處理2~3h,使之重新變成UO2。取適量的二氧化鈾放入鉑舟或鎳舟中,送入反應(yīng)管內(nèi),用高純度的氬將系統(tǒng)內(nèi)的空氣完全逐出以后,升溫至550~650℃,通入氟化氫。反應(yīng)時(shí)間依氧化鈾的粉碎程度而定。反應(yīng)完畢后,停止導(dǎo)入氟化氫,再通入氬氣將殘留的氟化氫完全逐出以后,迅速使反應(yīng)管的溫度降至常溫。如果在殘留有氟化氫的情況下降至常溫時(shí),則氟化氫將被吸附在氟化鈾上。應(yīng)注意,如果在氟化氫中或用作逐出氣的氬氣中含有水及氧氣時(shí),會(huì)使四氟化鈾中的雙氧鈾及氧化物雜質(zhì)含量增加。
制法2
2UO2+5NH4F·HF→2UF4·NH4F+3NH3+4H2O【150℃反應(yīng)溫度】
UF4·NH4F4→UF4+NH4F【50℃反應(yīng)溫度】
氟氫化銨(在常溫下為穩(wěn)定的白色粉末,容易處理。)與二氧化鈾反應(yīng)可制得四氟化鈾。
往二氧化鈾粉末中加入比所需量過量20%的氟氫化銨粉末,在惰性氣氛中充分混合,壓成疏松的片,放進(jìn)聚四氟乙烯反應(yīng)器中,導(dǎo)入惰性氣體,同時(shí)在150℃下加熱8h,就可制得綠色的UF4·NH4F。將UF4·NH4F移至鉑舟中,并放入鎳制反應(yīng)管或不銹鋼反應(yīng)管內(nèi),如果在惰性氣流中加熱至450℃,隨著反應(yīng)的進(jìn)行,NH4F逐漸揮發(fā)而分離出去,即可得到四氟化鈾。
用途
暫無
安全信息
危險(xiǎn)運(yùn)輸編碼:暫無
危險(xiǎn)品標(biāo)志:暫無
安全標(biāo)識(shí):暫無
危險(xiǎn)標(biāo)識(shí):暫無
文獻(xiàn)
None
備注
None
表征圖譜
統(tǒng)計(jì)數(shù)據(jù)
共收錄化學(xué)品數(shù)據(jù)
147579 條




 滬公網(wǎng)安備 31010602001115號(hào)
滬公網(wǎng)安備 31010602001115號(hào)