L-天冬氨酸 L-Aspartic acid
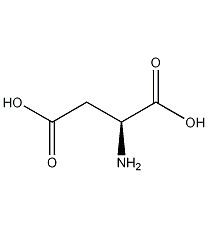
結構式
| 物競編號 | 017Y |
|---|---|
| 分子式 | C4H7NO4 |
| 分子量 | 133.1 |
| 標簽 | L(+)-氨基丁二酸, L(+)-氨基琥珀酸, L-天門冬氨酸, L-天冬酸, (S)-(+)-Aminosuccinic acid, (S)-Aspartic acid, 生化試劑, 中間體 |
編號系統(tǒng)
CAS號:56-84-8
MDL號:MFCD00002616
EINECS號:200-291-6
RTECS號:CI9098500
BRN號:1723530
PubChem號:暫無
物性數(shù)據(jù)
1. 性狀:無色斜方晶系葉片狀或棒狀晶體或結晶粉末,無臭。常為左旋光性。
2. 密度(g/mL,25/4℃): (d12.5/4)1.514
3. 相對蒸汽密度(g/mL,空氣=1):未確定
4. 熔點(oC):270-271
5. 沸點(oC,常壓):未確定
6. 沸點(oC,5.2kPa):未確定
7. 折射率:未確定
8. 閃點(oC):未確定
9. 比旋光度(o):[a]20/D+25°(c=1.97,6mol/L鹽酸中)。
10. 自燃點或引燃溫度(oC):未確定
11. 蒸氣壓(kPa,25oC):未確定
12. 飽和蒸氣壓(kPa,60oC):未確定
13. 燃燒熱(KJ/mol):未確定
14. 臨界溫度(oC):未確定
15. 臨界壓力(KPa):未確定
16. 油水(辛醇/水)分配系數(shù)的對數(shù)值:未確定
17. 爆炸上限(%,V/V):未確定
18. 爆炸下限(%,V/V):未確定
19. 溶解性:溶于熱水、酸、堿及鹽溶液,不溶于乙醇和乙醚。
毒理學數(shù)據(jù)
1、急性毒性:小鼠腹腔LC50:6mg/kg
2、其它多劑量毒性:大鼠經(jīng)口TDLo:25079mg/kg/7D-C
3、致突變性:姐妹染色單體exchangeTEST系統(tǒng):人類淋巴細胞:10mg/L
生態(tài)學數(shù)據(jù)
暫無
分子結構數(shù)據(jù)
1、 摩爾折射率:27.20
2、 摩爾體積(cm3/mol):87.8
3、 等張比容(90.2K):261.3
4、 表面張力(dyne/cm):78.2
5、 極化率(10-24cm3):10.78
計算化學數(shù)據(jù)
1.疏水參數(shù)計算參考值(XlogP):無
2.氫鍵供體數(shù)量:3
3.氫鍵受體數(shù)量:5
4.可旋轉化學鍵數(shù)量:3
5.互變異構體數(shù)量:無
6.拓撲分子極性表面積101
7.重原子數(shù)量:9
8.表面電荷:0
9.復雜度:133
10.同位素原子數(shù)量:0
11.確定原子立構中心數(shù)量:1
12.不確定原子立構中心數(shù)量:0
13.確定化學鍵立構中心數(shù)量:0
14.不確定化學鍵立構中心數(shù)量:0
15.共價鍵單元數(shù)量:1
性質與穩(wěn)定性
1.常溫常壓下性質穩(wěn)定。
2.為天然產(chǎn)物,無毒。
3.存在于煙葉、煙氣中。
貯存方法
密封干燥保存。
合成方法
1.左旋天冬氨酸的制法有合成法和發(fā)酵法。1.合成法主要是以馬來酸或富馬酸或它們的酯為原料,在加壓下用氨處理,然后水解。較容易合成得到外消旋天冬氨酸,但至今還沒有理想的拆分外消旋體的方法。2.發(fā)酵法在酶作用下,將富馬酸與氨加成,可高收率地得到產(chǎn)品。采用這種方法只生成左旋體,收率高,因此是工業(yè)生產(chǎn)的主要方法。
2.由反丁烯二酸、氨在三葉草假單胞菌或產(chǎn)氨短桿菌的天冬氨酸酶作用下得到。
3.以馬來酸、富馬酸或它們的酯為原料,在酶的作用下與氨加成。反應如下:
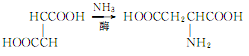
4.煙草:BU,22;FC,21。
用途
1.生化及醫(yī)學臨床研究。可作氨解毒劑,肝機能促進劑,疲勞恢復劑等醫(yī)藥品,可制L-天冬酸鈉食品添加劑和各種清涼飲料的添加劑,還可作生化試劑、培養(yǎng)基和有機合成中間體。
2.可作為生化試劑、培養(yǎng)基和有機合成中間體。在醫(yī)藥上作為心臟病類藥物、肝功能促進劑、氨解毒劑、疲勞消除劑和氨基酸輸液的成分。也用于食品工業(yè)的保鮮劑等。
3.營養(yǎng)增補劑。添加于各種清涼飲料。醫(yī)藥上用作氨解毒劑、肝功能促進劑。化妝品中用作營養(yǎng)添加劑。
4.L-天冬氨酸常用作非對映烷基化反應的手性底物,并且可作為手性源合成其它手性化合物等。
非對映選擇性烷基化 L-天冬氨酸酯能夠在α-和β-位發(fā)生烷基化 (式1)[2],其中β-烷基化反應的應用最為廣泛。在β-烷基化反應進程中,氨基酸部分對該反應的非對映選擇性有著重要的影響。同時,也可通過L-天冬氨酸的環(huán)狀衍生物發(fā)生β-烷基化而制備β-二羰基化合物[3]。
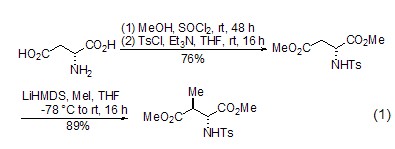
手性化合物的合成 以L-天冬氨酸為手性源,可以合成一系列手性化合物,如使用碘化亞銅、硼氫化鈉等作用后,可以得到多官能團的氧氮雜環(huán)類化合物 (式2)[4],該化合物可進一步生成喹啉類化合物[4]。
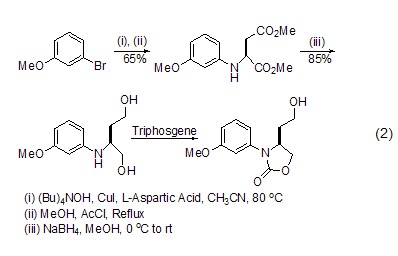
酰胺鍵的形成 L-天冬氨酸作為氨基酸,與其它氨基酸一樣也可生成酰胺類化合物 (式3)[5]。
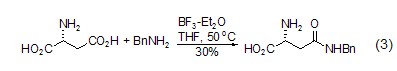
同時,還可以以L-天冬氨酸為母體,實現(xiàn)環(huán)內(nèi)酰胺的合成。如合成六元環(huán)內(nèi)酰胺 (式4)[6]。產(chǎn)物中還存在烷氧基,因此可作為另外一個反應位點進一步發(fā)生衍生化。
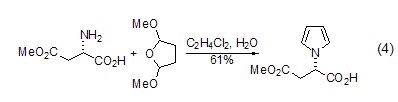
β-氨基酸(或氨基酸酯)的合成 L-天冬氨酸經(jīng)過氨基保護、烷基化等步驟后,可生成β-氨基酸或氨基酸酯 (式5)[10],該反應實現(xiàn)了從天然氨基酸到非天然氨基酸的轉化。
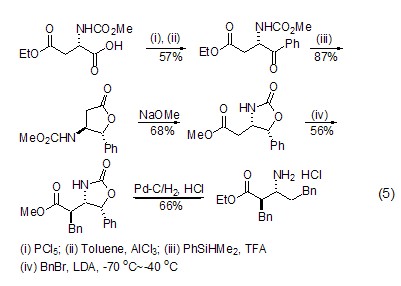
此外,L-天冬氨酸分子中含有兩個羧基和一個氨基,因此可作為多齒配體與金屬離子配位[7~9]或者自身形成內(nèi)酯化合物[10,11]。
安全信息
危險運輸編碼:暫無
危險品標志: 易燃
易燃  有害
有害  刺激
刺激
文獻
1. Marshall, J. A.; Andersen, N. H.; Schlicher, J. W. J. Org. Chem., 1970, 35, 858. 2. Goodenough, K. M.; Moran, W. J.; Raubo, P.; Harrity, J. P. A. J. Org. Chem., 2005, 70, 207. 3. Luppi, G.; Tomasini, C. Synlett, 2003, 6, 797. 4. Ding, K.; Flippen-Anderson, J.; Deschamps, J. R.; Wang, S. Tetrahedron Lett., 2004, 45, 1027. 5. van Leeuwen, S. H.; Quaedflieg, P. J. L. M.; Broxterman, Q. B.; Milhajlovic, Y.; Liskamp, R. M. J. Tetrahedron Lett., 2004, 45, 653. 6. Patel, J.; Pelloux-Leon, N.; Minassian, F.; Vallee, Y. J. Org. Chem., 2005, 70, 9081. 7. Anokhina, E. V.; Jacobson, A. J. J. Am. Chem. Soc., 2004, 126, 3044. 8. Rattat, D.; Eraets, K.; Cleynhens, B.; Knight, H.; Fonge, H.; Verbruggen, A. Tetrahedron Lett., 2004, 45, 2531. 9. Kobayashi, S.; Matsubara, R.; Nakamura, Y.; Kitagawa, H.; Sugiura, M. J. Am. Chem. Soc., 2003, 125, 2507. 10. Seki, M.; Shimizu, T.; Matsumoto, K. J. Org. Chem., 2000, 65, 1298. 11. Calvisi, G.; Dell'Uomo, N.; De Angelis, F.; Dejas, R.; Giannessi, F.; Tinti, M. O. Eur. J. Org. Chem., 2003, 4501. 12.參考書:現(xiàn)代有機合成試劑<性質、制備和反應>;胡躍飛 付華 編著;化學工業(yè)出版社;ISBN 7-5025-8542-7 13. Sason M, Matsuyama S. Nippon Sembai Kosha Chuo Kenkyusho Kenkyu Hokoku, 1978, 120: 1-6.
備注
暫無
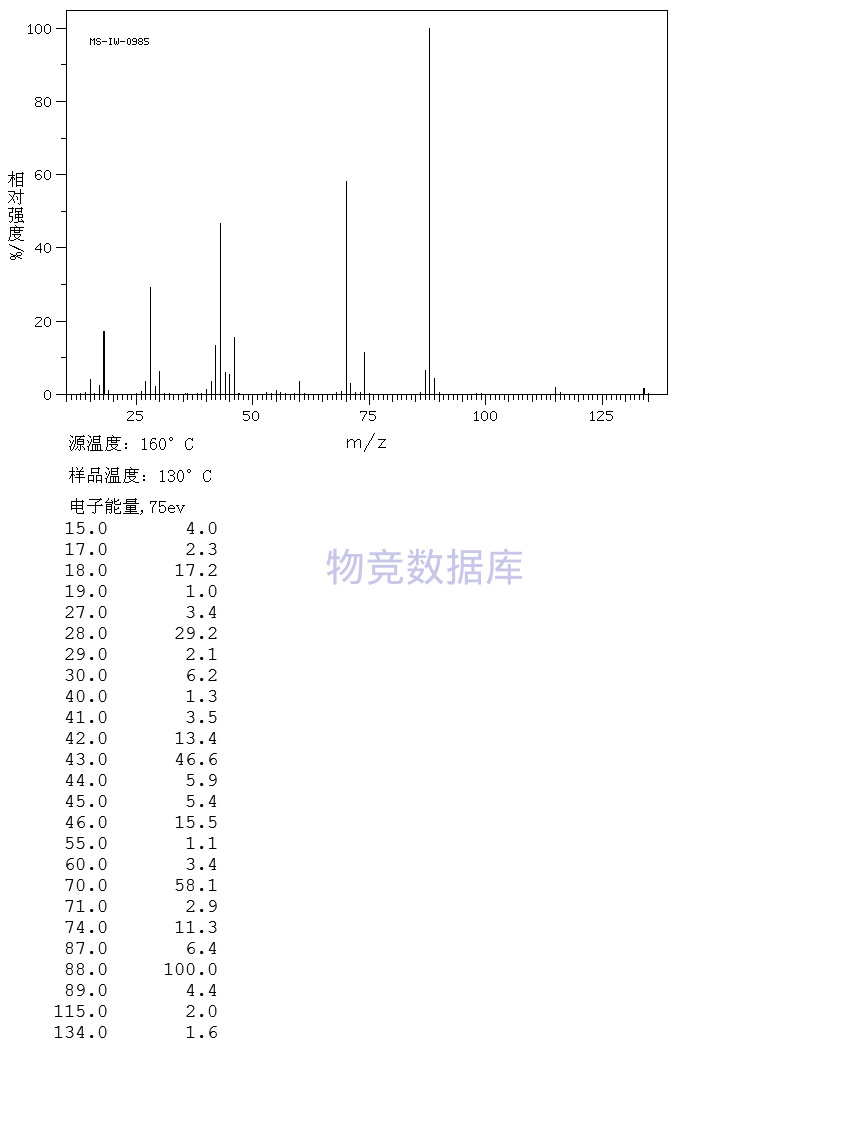
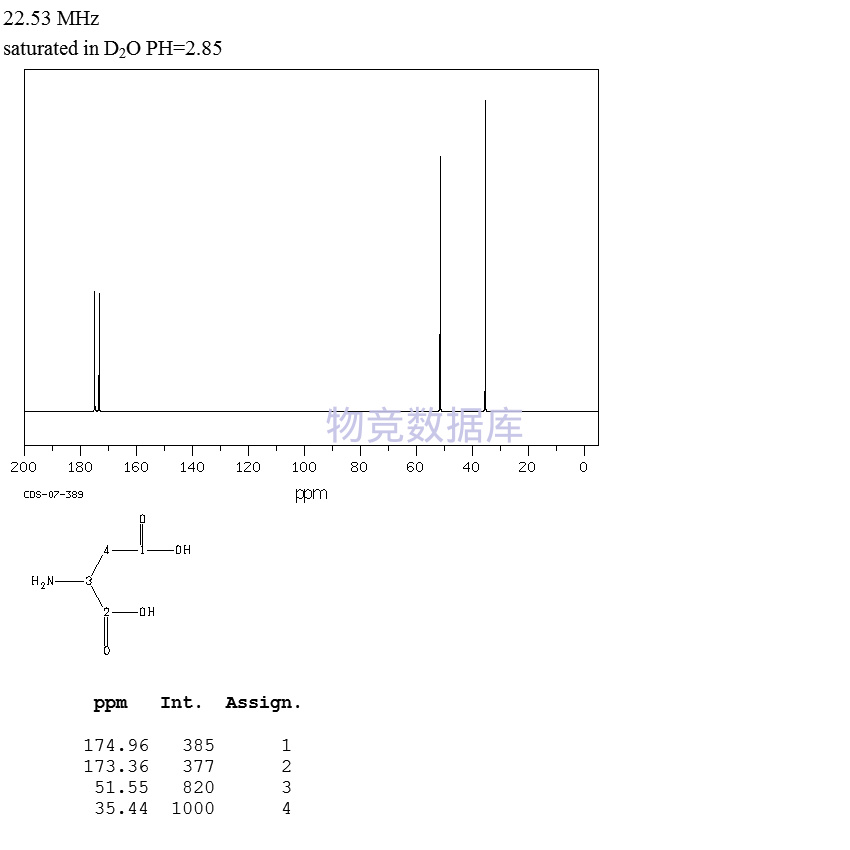
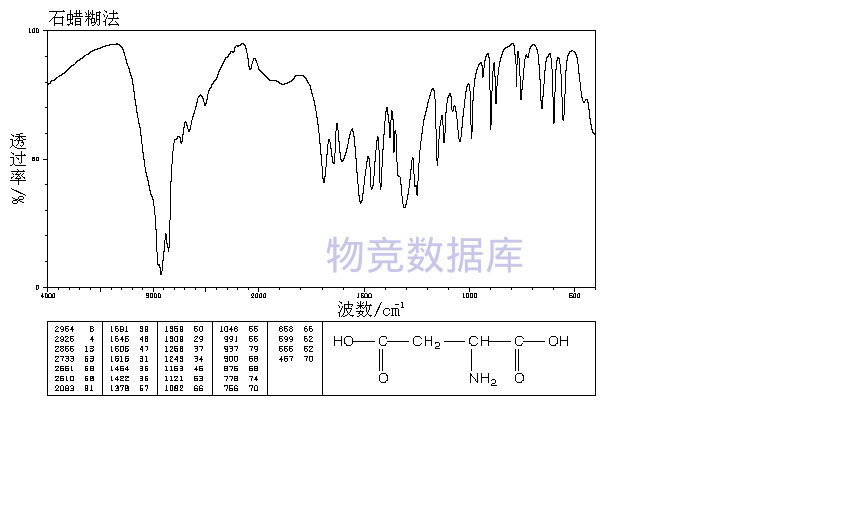
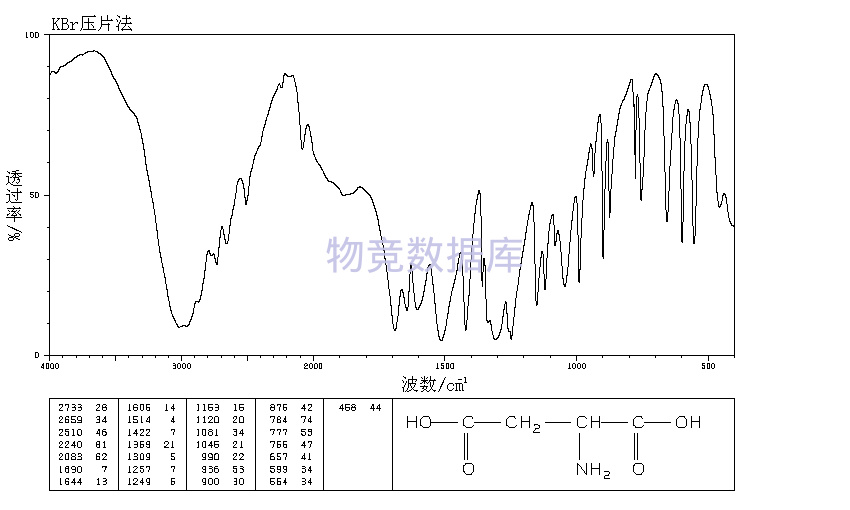
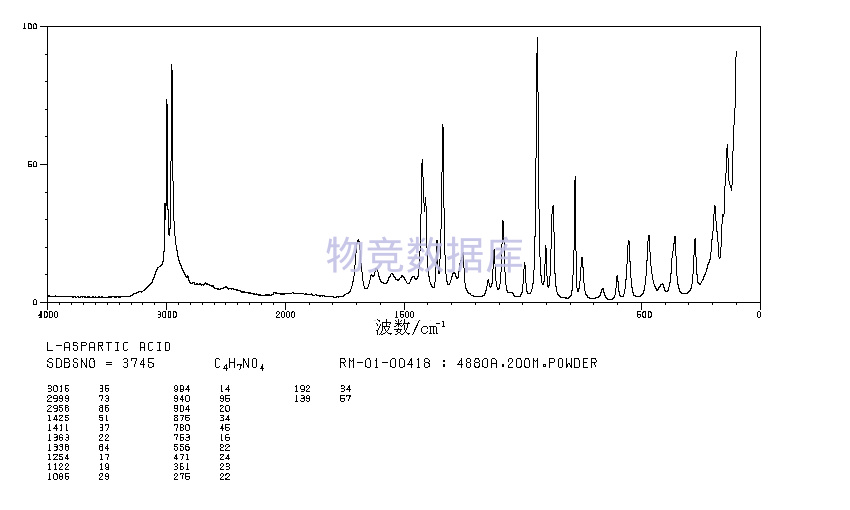
表征圖譜
統(tǒng)計數(shù)據(jù)
共收錄化學品數(shù)據(jù)
147579 條



 滬公網(wǎng)安備 31010602001115號
滬公網(wǎng)安備 31010602001115號