二氧化硫 Sulfur dioxide
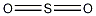
結構式
| 物競編號 | 172M |
|---|---|
| 分子式 | SO2 |
| 分子量 | 64.06 |
| 標簽 | 亞硫酸酐, 無水亞硫酸, 純亞硫酸酐, Sulfurous anhydride, Sulfurous oxide, Sulfurous anhydride, 還原性漂白劑, 冷凍劑, 防腐劑, 熏蒸劑, 殺蟲劑, 殺菌劑, 電子特種氣體原料及中間體 |
編號系統
CAS號:7446-09-5
MDL號:MFCD00011450
EINECS號:231-195-2
RTECS號:WS4550000
BRN號:3535237
PubChem號:暫無
物性數據
1.性狀:無色氣體,有刺激性氣味。[1]
2.熔點(℃):-75.5[2]
3.沸點(℃):-10[3]
4.相對密度(水=1):1.4(-10℃)[4]
5.相對蒸氣密度(空氣=1):2.25[5]
6.飽和蒸氣壓(kPa):330(20℃)[6]
7.臨界溫度(℃):157.8[7]
8.臨界壓力(MPa):7.87[8]
9.辛醇/水分配系數:-2.20[9]
10.溶解性:溶于水、乙醇、乙醚。[10]
11.黏度(mPa·s,0oC):0.3936
12.黏度(mPa·s,-10.5oC):0.4285
13.黏度(mPa·s,-15oC):0.4521
14.黏度(mPa·s,-33.5oC):0.5508
15.蒸氣壓(kPa,-268C):338.42
16.蒸氣壓(mmHg,21oC):1779
17.蒸發熱(KJ/mol,-10.08oC):24.95
18.熔化熱(KJ/mol):7.41
19.生成熱(KJ/mol,25oC):297.01
20.沸點上升常數:1.48
21.電導率(S/m):3×10-8
毒理學數據
1、大鼠吸入(1h)LC50:6600mg/m3。ADI 0~70mg/kg(以SO2計,包括SO2和亞硫酸鹽的總ADI;FAO/WHO,2001)。對眼及呼吸道黏膜有強烈的刺激作用。SO2在空氣中濃度達0.04%~0.05%時,人就會中毒。
2、屬中等毒類,易被濕潤的黏膜表面吸收而生成亞硫酸,其中部分氧化為硫酸,故對呼吸道和眼有強烈的刺激作用。輕度中毒時發生流淚、畏光、咳嗽、鼻、咽、喉部灼燒樣痛、聲音嘶啞,甚至呼吸短促、胸悶、胸痛。有時還會出現惡心、嘔吐、上腹痛、頭痛、頭昏、全身無力等癥狀。嚴重中毒時于數小時內發生肺水腫、呼吸困難、紫紺、支氣管痙攣而引起急性肺氣腫。空氣中的濃度為7.86~13.1mg/m3時人可感覺到,52.4mg/m3時刺激眼黏膜,1048~1310mg/m3時短時間即有生命危險。最高容許濃度為20mg/m3。
3.急性毒性[11] LC50:6600mg/m3;2520ppm(大鼠吸入,1h)
4.刺激性[12] 家兔經眼:6ppm(4h),共32d,輕度刺激。
5.亞急性與慢性毒性[13] 小鼠吸入本品5.24mg/m3,半年,出現免疫反應受抑制。
6.致突變性[14] DNA損傷:人淋巴細胞5700ppb。DNA抑制:人淋巴細胞5700ppb。細胞遺傳學分析和姐妹染色單體交換:人多種接觸途徑42mg/m3。
7.致畸性[15] 兔孕后6~18d吸入最低中毒劑量(TCLo)70ppm(7h),致肌肉骨骼系統發育畸形。
8.其他[16] 大鼠吸入最低中毒濃度(TCLo):4mg/m3,(24h)(交配前72d),引起發情周期改變或失調,對分娩有影響,對雌性生育指數有影響。小鼠吸入最低中毒濃度(TCLo):25ppm(7h)(孕6~15d),引起胚胎毒性。
人吸入LCLo:1000ppm(10min);TCLo:3ppm(5d);400~500ppm,立即危及生命。
生態學數據
1.生態毒性 暫無資料
2.生物降解性 暫無資料
3.非生物降解性 暫無資料
4.其他有害作用[17] 該物質可嚴重污染大氣,由其形成的酸與對植物的危害尤為嚴重。
分子結構數據
1、摩爾折射率:12.05
2、摩爾體積(cm3/mol):40.2
3、等張比容(90.2K):115.1
4、表面張力(dyne/cm):66.8
5、極化率(10-24cm3):4.77
計算化學數據
1、疏水參數計算參考值(XlogP):
2、氫鍵供體數量:0
3、氫鍵受體數量:2
4、可旋轉化學鍵數量:1
5、互變異構體數量:
6、拓撲分子極性表面積(TPSA):40.1
7、重原子數量:6
8、表面電荷:0
9、復雜度:59.8
10、同位素原子數量:0
11、確定原子立構中心數量:0
12、不確定原子立構中心數量:0
13、確定化學鍵立構中心數量:0
14、不確定化學鍵立構中心數量:0
15、共價鍵單元數量:2
性質與穩定性
1.在常溫下,潮濕的二氧化硫與硫化氫起反應析出硫。在高溫及催化劑存在的條件下,可被氫還原成為硫化氫,被一氧化碳還原成硫。強氧化劑可將二氧化硫氧化成三氧化硫,僅在催化劑存在時,氧才能使二氧化硫氧化為三氧化硫。具有自燃性,無助燃性。液態二氧化硫能溶解如胺、醚、醇、苯酚、有機酸、芳香烴等有機化合物,多數飽和烴不溶解。有一定的水溶性,與水及水蒸氣作用生成有毒及腐蝕性蒸氣。無機化合物如溴、三氯化硼、二硫化碳、三氯化磷、磷酰氯、氯化碘以及各種亞硫酰氯化物都可以任何比例與液態二氧化硫混合。堿金屬鹵化物在液態二氧化硫中的溶解度按I->Br->Cl-的次序減小。金屬氧化物、硫化物、硫酸鹽等多數不溶于液態二氧化硫。
2.化學性質:液態二氧化硫比較穩定,不活潑。氣態二氧化硫加熱到2000℃不分解。不燃燒,與空氣也不組成爆炸性混合物。化學性質極其復雜,不同的溫度可表現出非質子溶劑、路易氏酸、還原劑、氧化劑、氧化還原試劑等各種作用。液態二氧化硫還可作自由基接受體。如在偶氮二異丁腈自由基引發劑存在下與乙烯化合物反應得到聚砜。液態二氧化硫在光照下,可與氯和烷烴進行氯磺化反應,在氧存在下生成磺酸。液態二氧化硫在低溫表現出還原作用,但在300℃以上表現出氧化作用。
3.穩定性[18] 穩定
4.禁配物[19] 強還原劑、強氧化劑、易燃或可燃物
5.避免接觸的條件[20] 潮濕空氣
6.聚合危害[21] 不聚合
貯存方法
儲存注意事項[22] 儲存于陰涼、通風的有毒氣體專用庫房。遠離火種、熱源。庫溫不宜超過30℃。應與易(可)燃物、氧化劑、還原劑、食用化學品分開存放,切忌混儲。儲區應備有泄漏應急處理設備。
合成方法
1.用氨水吸收硫酸廠尾氣,吸收液含亞硫酸銨和亞硫酸氫銨,用硫酸分解可放出高濃度SO2氣體,經干燥、壓縮、分離和冷卻即成液體產品。也可用硫黃與純氧在焚硫爐內燃燒,生成高濃度的SO2氣體,經干燥、壓縮和冷凝成液體SO2。
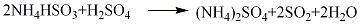
精制方法:液態二氧化硫中的雜質含有微量SO3、水、不揮發物質及空氣成分(O2、N2、CO2等)。一般可直接作合成反應的溶劑使用。精制時可將液態二氧化硫氣化,通入濃硫酸中以除去SO3,通入裝有五氧化二磷的玻璃管或在盛有五氧化二磷的容器中進行蒸餾以除去水分。
2.氨酸法 用硫酸分解硫酸廠尾氣吸收工序所得的亞硫酸銨亞硫酸氫銨母液,產生的約100%二氧化硫氣體,經壓縮法和冷凍法,可制得二氧化硫。
3.壓縮法 用硫酸分解亞硫酸銨亞硫酸氫銨母液,分解產生的二氧化硫氣體,經冷凝、干燥、過濾,再經壓縮液化,制得液體二氧化硫成品。其反應式如下。
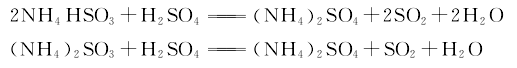
4.冷凍法 用硫酸分解亞硫酸銨亞硫酸氫銨母液,分解產生的二氧化硫氣體經干燥后送至低溫冷凝器,在常壓下進行冷凝,用氨冷凍維持溫度在液化點-10℃以下。制得液體二氧化硫成品。其反應式如下。
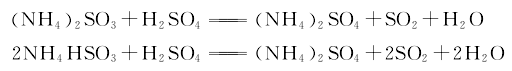
5.純氧燃燒法 將硫磺與純氧在焚硫爐內燃燒,生成的高濃度二氧化硫氣體,經凈化、干燥、壓縮液化、冷凝,制得二氧化硫成品。其反應式如下。

6.檸檬酸鈉法 經過凈化的二氧化硫氣體用檸檬酸鈉溶液吸收,再用低壓蒸汽脫出二氧化硫,經冷卻、分離冷凝水,用濃硫酸進行干燥,然后經壓縮液化、冷凝,制得液體二氧化硫成品。
用途
1.二氧化硫是我國允許使用的還原性漂白劑。對食品有漂白和對植物性食品內的氧化酶有強烈的抑制作用。我國規定可用于葡萄酒和果酒,最大使用量0.25g/kg,殘留量不得超過0.05g/kg。主要用于生產三氧化硫、硫酸、亞硫酸鹽、硫代硫酸鹽,也用作熏蒸劑、漂白劑、防腐劑、消毒劑、還原劑等。
2.主要用作硫酸的制造原料,也用作多種有機化學反應的溶劑。在液態二氧化硫中陽離子或陽碳離子與液態二氧化硫分子都能獨立存在,而對陰離子的溶劑化作用強。因此液態二氧化硫作溶劑有利于陽離子作為反應中間體的化學反應,可加快反應速度。例如Beckmann重排反應,Wager Meerwein重排反應,酯化反應等。液態二氧化硫作溶劑也有利于陽離子聚合反應和順反異構的異構化反應。此外液態二氧化硫還可用于熏蒸劑、殺蟲劑、水果蔬菜防腐劑、殺菌劑、纖維漂白劑以及礦物油的精制、各種亞硫酸鹽的制造、鎂的冶煉等。
3.在工業中是多種化合物的良好溶劑。可用作冷凍劑、防腐劑、漂白劑及其他有機產品的原料。也用于制造保險粉和亞硫酸鹽等。還用于農藥、醫藥、人造纖維及染料等工業部門。
4.用于制造硫酸和保險粉等。[23]
安全信息
危險運輸編碼:UN 2037 2.3
危險品標志: 有毒
有毒
安全標識:S9 S26 S45 S36/S37/S39
文獻
[1~23]參考書:危險化學品安全技術全書.第一卷/張海峰主編.—2版.北京;化學工業出版社,2007.6 ISBN 978-7-122-00165-8
備注
暫無
表征圖譜
統計數據
共收錄化學品數據
147579 條




 滬公網安備 31010602001115號
滬公網安備 31010602001115號