氮化硅 Silicon(Ⅳ) Nitride
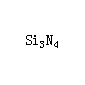
結構式
| 物競編號 | 0L8T |
|---|---|
| 分子式 | Si3N4 |
| 分子量 | 140.28 |
| 標簽 | 四氮化三硅, Trisilicon tetranitride, 穩定劑, 精細陶瓷 |
編號系統
CAS號:12033-89-5
MDL號:MFCD00011230
EINECS號:234-796-8
RTECS號:暫無
BRN號:暫無
PubChem號:24859489
物性數據
1. 性狀:灰色無定形粉末或晶體。
2. 密度(g/mL,25℃):3.18
3. 熔點(oC):1900
毒理學數據
主要的刺激性影響:
在皮膚上面:可能引起發炎;
在眼睛上面:可能引起發炎;
致敏作用:沒有已知的敏化現象。
生態學數據
通常對水是不危害的,若無政府許可,勿將材料排入周圍環境。
分子結構數據
暫無
計算化學數據
1.疏水參數計算參考值(XlogP):無
2.氫鍵供體數量:0
3.氫鍵受體數量:4
4.可旋轉化學鍵數量:0
5.互變異構體數量:無
6.拓撲分子極性表面積13
7.重原子數量:7
8.表面電荷:0
9.復雜度:154
10.同位素原子數量:0
11.確定原子立構中心數量:0
12.不確定原子立構中心數量:0
13.確定化學鍵立構中心數量:0
14.不確定化學鍵立構中心數量:0
15.共價鍵單元數量:1
性質與穩定性
氮化硅有α、β兩種晶型。α-Si3N4為顆粒結晶,β-Si3N4為針狀結晶體,兩者均屬六方晶系,相對密度3.18,莫氏硬度9,熱膨脹系數小、化學穩定性好,并具有優良的抗氧化性。在1900℃分解為氮和硅。氮化硅的強度很高且耐高溫,即使1200℃的高溫,其強度也不會改變,受熱后不會熔成融體,一直到1900℃才會分解,耐化學腐蝕性能,能耐幾乎所有的無機酸以及多種有機酸的腐蝕;氮化硅堅硬、熱膨脹系數小,熱震穩定性極好,絕緣性好,化學性質穩定,機械強度很高。難氧化,可做成熔融Al,Pb,Mg,Sn的坩堝。
貯存方法
常溫密閉,陰涼通風干燥處。
合成方法
1.主要有硅粉直接氮化法、二氧化硅還原法和氯化硅法。在大規模工業生產中,二氧化硅還原法更為人們所重視。
二氧化硅還原法二氧化硅粉末100份(重量份,下同),混入炭黑35份,尿素樹脂100份,然后加入800份水、0.1份氧化鋁(作反應核用)、1份草酸銨和0.3份非離子表面活性劑(作分散劑),進行強攪拌,并在攪拌中加入氨水調整Ph值為9.0。將此混合好的料漿噴霧干燥,所得干燥物在電爐中,在氮氣氛中,在1480℃進行3 h氮化還原反應。再將還原反應產物于。720℃,在空氣中進行脫炭處理,制得氮化硅粉末成品。
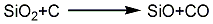
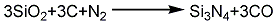
2.一般是用鐵礬土,高嶺土,黏土或其他含有Al2O3的物質添加一定量的碳,再在氮氣氣氛中加熱到1300~1500℃,即得到產物Si3N4。其中使用的氮氣一定要保證不含氧。
3.硅直接氮化法 將硅粉放在氮氣、氨氣或氫氮混合氣中,加熱至1200~1450℃直接氮化制得。在1200~1300℃反應可制得α相含量高的Si3N4原始粉末,燒結成陶瓷時強度高。
4.二氧化硅還原法 以二氧化硅、氮氣和炭為原料制備氮化硅,反應式如下。
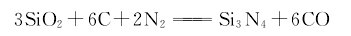
將硅石(或正硅酸乙酯水解制得的二氧化硅)與炭按一定比例充分混合,通入氮氣加熱至1400℃氮化24h。反應溫度超過1550℃會生成SiC,因此需加入少量的Fe2O3來抑制SiC的生成,反應后用鹽酸除去含鐵的化合物,該方法制得的原料粉中α相含量高,但粉末中常有少量的SiO2雜質,這是有害的。
5.氣相合成法 以四氯化硅和氨氣為原料生產氮化硅,反應式如下。
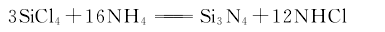
將四氯化硅與無水氨氣在0℃的己烷中反應生成亞氨基硅[Si(NH)2],氨基硅[Si(NH2)4]和氯化銨沉淀,在真空中加熱除去氯化銨之后,在惰性氣體中加熱分解生成氮化硅。
也可用硅烷(SiH4)和氨氣在1050~1350℃形成無定型Si3N4,在1450℃形成α相氮化硅。
用途
2.用于絕緣材料、機械耐磨材料、熱機材料、切削工具、高級耐火材料及抗腐蝕、耐磨損密封部件等。氮化硅陶瓷可做燃氣輪機的燃燒室、機械密封環、輸送鋁液的電磁泵的管道及閥門、永久性模具、鋼水分離環等。氮化硅摩擦系數小,用于高溫軸承,其工作溫度可達1200℃,比普通合金軸承的工作溫度提高2.5倍,而工作速度是普通軸承的10倍。利用氮化硅陶瓷很好的電絕緣性和耐急冷急熱性可以用來做電熱塞,用它進行汽車點火可使發動機起動時間大大縮短,并能在寒冷天氣迅速起動汽車。氮化硅陶瓷還有良好的透微波性能、介電性以及高溫強度,作為導彈和飛機的雷達天線罩。
3.用作精細陶瓷燒結原料,耐腐蝕、耐磨、研磨原材料。安全信息
危險運輸編碼:暫無
危險品標志: 刺激
刺激
危險標識:R37
文獻
暫無
備注
暫無
表征圖譜
統計數據
共收錄化學品數據
147579 條




 滬公網安備 31010602001115號
滬公網安備 31010602001115號