氰化鈉 Sodium cyanide
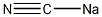
結構式
| 物競編號 | 03W3 |
|---|---|
| 分子式 | NaCN |
| 分子量 | 49.01 |
| 標簽 | 山奈鈉, : 山柰, Cianuro disodio, 媒染劑, 增白劑, 掩蔽劑, 淬火劑, 印刷線路板電鍍用原材料 |
編號系統
CAS號:143-33-9
MDL號:MFCD00003523
EINECS號:205-599-4
RTECS號:VZ7525000
BRN號:3587243
PubChem號:24886191
物性數據
1.性狀:白色或略帶顏色的塊狀或結晶狀顆粒,有微弱的苦杏仁味。[9]
2.熔點(℃):563.7[10]
3.沸點(℃):1496[11]
4.相對密度(水=1):1.596[12]
5.飽和蒸氣壓(kPa):0.13(817℃)[13]
6.辛醇/水分配系數:-1.69[14]
7.溶解性:易溶于水,溶于液氨,微溶于乙醇、乙醚、苯。[15]
毒理學數據
1、急性毒性:
大鼠經口LD50:6440 ug/kg;大鼠腹腔LD50:4300 ug/kg;小鼠腹腔LD50:4900 ug/kg;小鼠皮下LD50:3600 ug/kg;兔子經皮LD50:10400 ug/kg;兔子皮下LD50:2200 ug/kg。
2.急性毒性[16] LD50:6.4mg/kg(大鼠經口)
3.刺激性 暫無資料
4.其他[17] 倉鼠植入最低中毒劑量(TDLo):5999mg/kg(孕6~9d),引起胚胎毒性,肌肉骨骼發育異常及心血管(循環)系統發育異常。
生態學數據
1.生態毒性 暫無資料
2.生物降解性 暫無資料
3.非生物降解性 暫無資料
4.其他有害作用[18] 該物質對環境有危害,應特別注意對水體的污染。
分子結構數據
1、摩爾折射率:無可用的
2、摩爾體積(cm3/mol):無可用的
3、等張比容(90.2K):無可用的
4、表面張力(dyne/cm):無可用的
5、介電常數:無可用的
6、極化率(10-24cm3):無可用的
7、單一同位素質量:48.992844 Da
8、標稱質量:49 Da
9、平均質量:49.0072 Da
計算化學數據
1.疏水參數計算參考值(XlogP):無
2.氫鍵供體數量:0
3.氫鍵受體數量:2
4.可旋轉化學鍵數量:0
5.互變異構體數量:無
6.拓撲分子極性表面積23.8
7.重原子數量:3
8.表面電荷:0
9.復雜度:12.8
10.同位素原子數量:0
11.確定原子立構中心數量:0
12.不確定原子立構中心數量:0
13.確定化學鍵立構中心數量:0
14.不確定化學鍵立構中心數量:0
15.共價鍵單元數量:2
性質與穩定性
1.在1.34℃以下水溶液易結晶出來的氰化鈉,常含有1個或2個結晶水。34.7℃以上時,則失去結晶水,成為強堿弱酸鹽。易與酸作用,甚至很弱的酸亦能與之反應。鐵、鋅、鎳、銅、鈷、銀和鎘等金屬溶解于氰化鈉溶液,產生相應的氰化物。在氧的參與下,能溶解金和銀等貴金屬,生成絡合鹽。劇毒!
2.密度:立方晶體1.60g/cm3。溶解度g/100gH2O40.8(0℃),58.7(20℃),71.2(30℃)。稍溶于醇。
3.試劑有劇毒,對眼睛有強烈的刺激,具有吸濕性,易通過皮膚吸收。應避免吸入氰化鈉粉塵顆粒。如果氰化鈉不慎被吸入,吞服或者通過皮膚進入人體,將有致命危險。氰化鈉中毒能致使肺部疼痛和人體青紫(人體LDL0: 2857 μg/kg;或者鼠LD50: 6440 μg/kg)。應儲存在干燥的地方,使用時應在通風櫥中進行。與酸不共存,可以和二氧化碳反應。在潮濕的空氣和水中可能分解。熱分解產生有毒的氰化氫、一氧化碳、二氧化碳、氮氧化合物煙霧。
4.穩定性[19] 穩定
5.禁配物[20] 酸類、強氧化劑
6.避免接觸的條件[21] 潮濕空氣
7.聚合危害[22] 不聚合
貯存方法
儲存注意事項[23] 儲存于陰涼、干燥、通風良好的專用庫房內。實行“雙人收發、雙人保管”制度。遠離火種、熱源。庫內相對濕度不超過80%。包裝密封。應與氧化劑、酸類、食用化學品分開存放,切忌混儲。儲區應備有合適的材料收容泄漏物。
合成方法
1.目前工業生產以丙烯腈副產法為主。
(1)氨鈉法將金屬鈉和石油焦按一定比例,加入反應器中,加熱至650℃,通入氨氣,升溫至800℃,反應7h,金屬鈉全部轉化為氰化鈉。反應物經保溫650℃過濾,以除去過量石油焦,熔融物放出經澆鑄成型而得氰化鈉產品。其
(2)氰熔體法將氰熔體和氧化鉛加入萃取槽中,其配料比為(500~700):l,加入氧化鉛因生成PbS沉淀,起到脫硫作用。萃取液經沉降,排出清液含NaCN 80~90 g/L,在發生器中與濃硫酸反應生成氫氰酸氣體,經冷凝除水后,進入吸收反應器內用液堿吸收,生成氰化鈉。其反應如下:
(3)安氏法以天然氣、氨和空氣為原料。天然氣經水洗塔脫去無機硫和部分有機硫,經過濾使精制后的天然氣含硫量≤l mg/m3、C2以上的烴類在2%以下,液氨經汽化器汽化,空氣經過濾器精濾。將三種原料氣按氨:甲烷:空氣:1:(1.15~1.17):(6.70~6.80)的比例,經混合器混合進入氧化反應器,以鉑銠合金為觸媒,于1070~1120℃溫度下,反應生成含8.5%的混合氣體,經冷卻后進氨吸收塔,用硫酸吸收殘余氨,然后經水冷卻,用低溫水吸收氰化氫,尾氣經堿洗塔后排空。水吸收氰化氫溶液經換熱后進入解吸塔,塔頂得純度98%HCN,再與堿液反應,生成氰化鈉溶液,經蒸發、結晶、干燥、成型,制得成品。其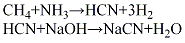
(4)火焰法以天然氣、氧氣、氨為原料,分別經過濾器濾去雜質,穩壓計量后進人混合器。氧氣一部分做主氧進混合器,另一部分直接進噴嘴作點火用。三種原料氣按一定比例配合,在溫度1500℃下進行合成氫氰酸的燃燒反應,反應氣經噴水淬冷、冷卻器冷卻,進氨吸收塔,以15%~20%硫酸吸收反應氣中的殘余氨,可回收硫酸銨。含氰化氫的反應氣經水冷,用低溫水吸收氰化氫而成1.5%溶液,經精餾塔精餾可得含量98%~99%的氰化氫,再經堿液吸收、蒸發、結晶、干燥、成型,制得氰化鈉成品。其主要反應如下: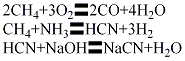
水吸收氰化氫后的尾氣含氫氣65%、一氧化碳約30%,可回收制合成氨、甲醇、草酸等產品。
(5)輕油裂解法將輕油和氨按比例在霧化器中混合,預熱至280℃,在電弧爐中裂解反應,以石油焦作載體,以氮氣作保護氣進行密閉防氧化,溫度1450℃,反應生成氫氰酸氣體,經除塵、冷卻后,再經除氨、水洗、吸收、精餾而得純凈的氫氰酸,再用堿液吸收生成氰化鈉。其反應如下: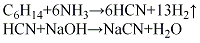
(6)丙烯腈副產法在丙烯氨氧化法制丙烯腈的過程中,副產氰化氫氣體(其量相當于丙烯腈產量的4%~10%),經堿液吸收,再經蒸發、濃縮、分離、干燥,制得氰化鈉產品。其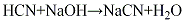
將1L含NaOH不超過40g的無水乙醇溶液用冰冷卻。向該溶液中加入稍過量的液體氰化氫。長時間放置此溶液,可析出結晶,抽濾,在P2O5干燥器中減壓干燥。
用途
1.用作各種鋼的淬火劑,鍍銅、銀、鎘、鋅等的主要組分,用于提取金、銀等貴重金屬,也是氰化物和氫氰酸的原料。
2.在機械工業中用作各種鋼的淬火劑。電鍍工業中作為鍍銅、銀、鎘和鋅等的主要組分。冶金工業中用于提取金、銀等貴重金屬。化學工業中是制造各種無機氰化物和發生氫氰酸的原料,也用于制造有機玻璃、各種合成材料、丁腈橡膠、合成纖維的共聚物。染料工業中用于制造三聚氰氯(活性染料中間體,又為生產增白劑的原料)。醫藥工業中用于制造氰乙酸甲酯和丙二酸二乙酯等。紡織工業中用作媒染劑,還用于鋼的液式滲碳,滲氮。
直接利用氰化鈉生產的重要無機氰化物主要有黃血鹽鈉、黃血鹽鉀、氰化鉀、氰化鋅、氰化鋇、氰化亞銅、硫氰化鈉、硫氰化鉀;有機氰化物有氰乙酸、丙二腈、蛋氨酸、氰芐、三聚氰氯等。利用氰化鈉發生氰化氫再生產的主要產品有:甲基丙烯酸甲酯、甲基丙烯酸丁酯、甲基丙烯酸、偶氮二異丁腈、偶氮二異庚腈、次氨基三乙酸、羥乙腈等。
3.在分析上用作掩蔽劑,在冶煉、電鍍工業中用作鉻合劑,還用于昆蟲激素的研究。
4.用于塑料、醫藥、農藥、染料、冶金、電鍍、選礦等行業,也用作制氫氰酸原料。絡合劑。掩蔽劑。提煉金銀礦用。
5.氰化鈉在電鍍溶液中可使陽極極化作用降低,保證陽極正常溶解,穩定鍍液并能提高陰極極化作用,獲得均勻的鍍層。
6.氰化鈉可以用來制備氰基化合物[2,3],氰醇類化合物[4,5],α-氨基氰基化合物[6],也可以用作催化劑,如安息香縮合反應。
氰基化合物的合成 在合適的溶劑中,活潑醇或鹵化物與氰化鈉反應可以得到氰化物,此反應為親核取代反應,是氰化物合成的通用方法。在DMSO中,氰化鈉與烷基氯反應時,氰基鈉比氰化鉀的反應產率高,且反應時間要短 (式1)[2]。

在微波條件下,氰化鈉與芳基鹵化物的反應是一種快速制備芳基氰化物的方法 (式2)[3]。反應快速且產率很高,是一種很好合成芳基氰化物的方法。
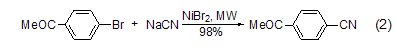
氰醇類化合物的合成 Gurjar和Joshi等人在合成順、反式羥基格列美脲的過程中,以β-羰基丁酸乙酯為原料,通過兩步反應生成腈醇類化合物,產率較高 (式3)[4]。
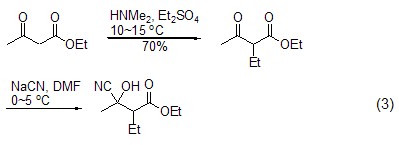
α-氨基氰基化合物的合成 在釕催化和氧氣存在下,三級胺與氰化鈉反應生成α-氨基氰化合物 (式4)[7],溶劑為甲醇和乙酸 (3:1) 的混合物。氧化氰化得到的叔胺是合成α-氨基酸的前體,因此,該方法提供了快捷方便的合成α-氨基酸的途徑。
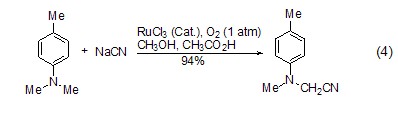
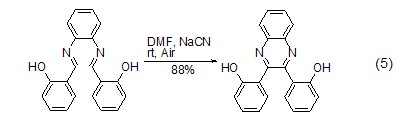
成環作用 氰化鈉可用作亞胺類化合物二聚成喹喔啉或吡嗪的催化劑,此反應類似于安息香縮合 (式5)[8]。在DMF、甲醇或二氯甲烷/水 (相轉移條件) 中,氰化鈉快速促進分子內環化得到六元環。
7.用于提煉金、銀等貴重金屬和淬火,并用于塑料、農藥、醫藥、染料等有機合成工業。[24]
安全信息
危險運輸編碼:UN1689 6.1/PG 1
危險品標志: 極毒
極毒  危害環境
危害環境
文獻
1. Perrin, D. D.; Armarego, W. L. F. Purification of Laboratory Chemicals, 3rd Ed.; Pergamon: New York, 1988; p 369. 2. Friedman, L.; Shechter, H. J. Org. Chem., 1960, 25, 877. 3. Arvela, R. K.; Leadbeater, N. E. J. Org. Chem., 2003, 68, 9122. 4. (a) Gurjar, M. K.; Joshi, R. A.; Chaudhuri, S. R.; Joshi, S. V.; Barde, A. R.; Gediya, L. K.; Ranade, P. V.; Kadam, S. M.; Naik, S. J. Tetrahedron Lett., 2003, 44, 4853. 5. Raj, I. V. P.; Sudalai, A. Tetrahedron Lett., 2005, 46, 8303. 6. Murahashi, S. -I.; Komiya, N.; Terai, H. Angew. Chem., Int. Ed., 2005, 44, 6931. 7. Murahashi, S. I.; Naruyoshi, K ; Hiroyuki, T.; Takahiro, N. J. Am. Chem. Soc., 2003, 125, 15312. 8. Reich, B. J. E.; Justice, A. K.; Beckstead, B. T.; Reibenspies, J. H.; Miller, S. A. J. Org. Chem., 2004, 69, 1357. [1~8]參考書:現代有機合成試劑<性質、制備和反應>;胡躍飛 付華 編著;化學工業出版社;ISBN 7-5025-8542-7 [9~24]參考書:危險化學品安全技術全書.第一卷/張海峰主編.—2版.北京;化學工業出版社,2007.6 ISBN 978-7-122-00165-8
備注
暫無
表征圖譜
統計數據
共收錄化學品數據
147579 條




 滬公網安備 31010602001115號
滬公網安備 31010602001115號