亞硝酸鈉 Sodium nitrite
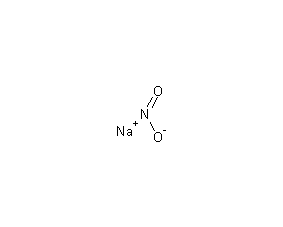
結構式
| 物競編號 | 0JWK |
|---|---|
| 分子式 | NaNO2 |
| 分子量 | 69.00 |
| 標簽 | 阻聚劑, 發色劑, 媒染劑, 漂白劑, 金屬熱處理劑, 電鍍緩蝕劑, 油墨所用原料及中間體 |
編號系統
CAS號:7632-00-0
MDL號:MFCD00011118
EINECS號:231-555-9
RTECS號:RA1225000
BRN號:暫無
PubChem號:24886427
物性數據
1.性狀:白色或淡黃色細結晶,無臭,略有咸味,易潮解。[11]
2.pH值:9(水溶液)[12]
3.熔點(℃):271[13]
4.沸點(℃):320(分解)[14]
5.相對密度(水=1):2.17[15]
6.溶解性:易溶于水,微溶于乙醇、甲醇、乙醚。[16]
毒理學數據
1.急性毒性[17]
LD50:180mg/kg(大鼠經口)
LC50:5.5mg/m3(大鼠吸入,4h)
2.刺激性[18] 家兔經眼:500mg(24h),輕度刺激。
3.致突變性[19] 微生物致突變:鼠傷寒沙門菌屬250μg/皿。程序外DNA合成:人Hela細胞6mmol/L。DNA抑制:人成纖維細胞2000ppm。DNA損傷:小鼠淋巴細胞105mmol/L。細胞遺傳學分析:猴肝265mg/L。
4.致畸性[20] 大鼠孕后10~19d,腹腔內給予最低中毒劑量(TDLo)400mg/kg,致中樞神經系統發育畸形,血液和淋巴系統發育畸形(包括脾和骨髓)。小鼠多代經口給予最低中毒劑量(TDLo)480mg/kg,致泌尿生殖系統發育畸形。
生態學數據
1.生態毒性 暫無資料
2.生物降解性 暫無資料
3.非生物降解性 暫無資料
4.其他有害作用[21] 該物質對環境有危害,應特別注意對水體的污染。
分子結構數據
1、摩爾折射率:無可用
2、摩爾體積(cm3/mol): 無可用
3、等張比容(90.2K):無可用
4、表面張力(dyne/cm):無可用
5、極化率:無可用
計算化學數據
1.疏水參數計算參考值(XlogP):無
2.氫鍵供體數量:0
3.氫鍵受體數量:3
4.可旋轉化學鍵數量:0
5.互變異構體數量:無
6.拓撲分子極性表面積52.5
7.重原子數量:4
8.表面電荷:0
9.復雜度:13.5
10.同位素原子數量:0
11.確定原子立構中心數量:0
12.不確定原子立構中心數量:0
13.確定化學鍵立構中心數量:0
14.不確定化學鍵立構中心數量:0
15.共價鍵單元數量:2
性質與穩定性
1.有氧化性,與有機物接觸能燃燒和爆炸,并放出有毒和刺激性的過氧化氮和氧化氮的氣體。
2.易潮解,在空氣中可被氧化成硝酸鈉。本品是食品添加劑中急性毒性較強的物質之一,攝入大劑量的亞硝酸鈉,可使血紅蛋白變成高鐵血紅蛋白而失去輸氧能力,造成身體組織缺氧,直至死亡。
3.吸濕性很強。常溫下在空氣中氧化極為緩慢,加熱至320℃以上分解釋放出氮氣、氧氣、一氧化氮,最終生成氧化鈉。與有機物接觸易燃燒和爆炸。晶體亞硝酸鈉在160~162℃間有一轉化點,此時膨脹性,導電性、比熱和壓電性等物理性質均發生變化。易溶于水和液氨,其水溶液呈堿性(PH=9)。微溶于無水乙醇、甲醇、乙醚。露置于空氣中緩慢氧化成硝酸鈉。加熱到320 ℃以上分解放出氧氣、氧化氮,最終生成氧化鈉。與有機物接觸易燃燒和爆炸。有毒!
4.易吸水,應保存于干燥密封的容器中,在空氣中亞硝酸鹽很容易被氧氣氧化。NaNO2溶液很不穩定,不能長時間保存。NaNO2遇酸會形成弱酸,并產生棕色氣體N2O3。亞硝酸鈉有毒,不能用口嘗。
5.NaNO2遇到不同的無機酸或羧酸會產生HNO2,在大多數的有機合成中,NaNO2都是以不穩定的HNO2形式參與反應的,而涉及到HNO2的反應通常很復雜,因為在溶液中還存在N2O3、ON+等。包括NOX、RNH2在內的一系列化合物都能發生重氮化和亞硝基化反應。
與氨及相關物質的反應 通常情況下,NaNO2的HCl溶液與氨反應能很快進行,而且多數下能定量反應。對伯胺而言,反應產生重氮離子中間體,然后消除一分子的N2形成碳正離子,再進一步與親電試劑反應 (式1)[1~3]。
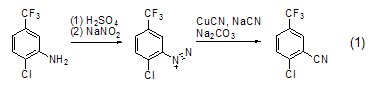
而當分子中存在多個親核官能團時,所形成的重氮基團則可能繼續反應 (式2)[4],在NaNO2作用下,伯胺首先形成重氮鹽,然后與仲胺發生關環反應。

C-亞硝化反應 烷烴的中心碳一般不發生亞硝化反應,除非連有酰基、芳酰基、羰基、羧基、硝基、氰基、亞氨基或苯基等吸電子基團。一般的產物是亞硝胺或肟,硝基的鄰位碳在NaNO2作用下生成肟 (式3)[5]。式4則是碳原子部位發生亞硝化,產物為亞硝胺[6]。

用NaNO2的HCl溶液對酚進行亞硝化會得到相應的亞硝基化合物。例如,苯酚一般生成4-亞硝基苯酚,同時會有少量2-取代的異構體 (約10%),而2-萘酚則會生成1-亞硝基-2-萘酚。如果用NaNO2與NaOH先作用后再加入乙酸,則可以在芳香環上直接引入亞硝基 (式5)[7]。
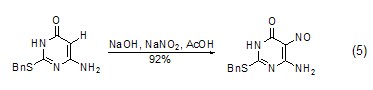
N-亞硝化 NaNO2除了可使碳原子發生亞硝化,也可使氮原子發生亞硝化,在加熱條件下,產物可脫去一分子氮氣而轉化為酯類化合物 (式6)[8]。
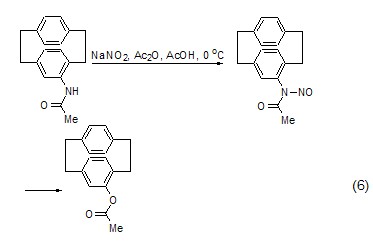
氧化反應 在催化劑等的作用下,NaNO2可將伯醇、仲醇等化合物氧化為相應的醛、酮 (式7)[9]。
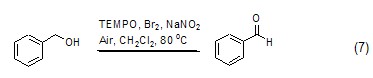
除了可以發生氧化反應以外,NaNO2同樣可以參與還原反應,如亞硝酸根能夠轉化為硝酸根,進而實現對某些化合物的還原[10]。
6.穩定性[22] 穩定
7.禁配物[23] 強還原劑、活性金屬粉末、強酸、銨鹽、可燃物粉末或氰化物
8.避免接觸的條件[24] 受熱
9.聚合危害[25] 不聚合
10.分解產物[26] 氮氧化物
貯存方法
儲存注意事項[27] 儲存于陰涼、干燥、通風良好的專用庫房內,遠離火種、熱源。庫溫不超過30℃,相對濕度不超過75%。包裝要求密封,不可與空氣接觸。應與還原劑、活性金屬粉末、酸類、食用化學品分開存放,切忌混儲。儲區應備有合適的材料收容泄露物。
合成方法
1.使氨氣氧化產生氧化氮氣體,用氫氧化鈉或碳酸鈉溶液吸收。
用鉛還原硝酸鈉,加熱熔化硝酸鈉,加少量金屬鉛,攪拌并繼續加熱至鉛全部氧化。生成的塊狀物邊冷卻邊分成小塊,用熱水萃取生成的氧化鉛數次。通入二氧化碳氣體使生成碳酸鉛沉淀,經過濾,用稀硝酸準確中和濾液后,蒸發、濃縮析出亞硝酸鈉結晶。經吸濾,用乙醇洗滌后干燥,再重結晶精制而得。
2.用燒堿溶液或純堿吸收硝酸或硝酸鹽生產中排出的含有少量NO和NO2的尾氣,尾氣中NO/NO2的比例要調節至使中和液中NaNO2與NaNO3的質量之比在8以下,在吸收過程中中和液應避免出現酸性,以免腐蝕設備。當中和液的相對密度為1.24~1.25,純堿含量為3~5g/L時送去蒸發,在132℃時吸收液蒸發濃縮,然后冷至75℃,析出亞硝酸鈉呈結晶,再經分離、干燥即得產品。反應方程式如下:

3.將硝酸合硝酸鹽生產時排除的尾氣中的一氧化氮合二氧化氮,用純堿或燒堿溶液吸收而得中和液,經蒸發、結晶,然后利用亞硝酸鈉與硝酸鈉在水中的溶解度不同而將二者分離,即得成品。
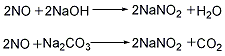
4.將42.5g硝酸鈉與100g金屬鉛在瓷(或鐵)坩堝中熔融攪拌,冷卻后用200mL熱水抽提,通入CO2數分鐘,以沉淀溶于水中的氧化鉛,鐵離子等。過濾,濾液用稀硝酸酸化后,蒸發濃縮至干。然后加200~250mL乙醇在殘渣上煮沸,過濾濾液以除去少量的硝酸鈉,蒸餾濾液除去乙醇,則得到白色粉末,亞硝酸鈉約20g。
提純方法:將100g亞硝酸鈉在70~80℃下溶于100mL水中,加入1~2g純氫氧化鈉以沉淀鐵,冷卻過濾,蒸發結晶,二次再結晶純度更高,產量為75g。
5.采用吸收法。將稀硝酸生產過程中排出的尾氣中一氧化氮和二氧化氨的比例調節到使中和液的亞硝酸和硝酸鈉的質量比在8以下。然后將尾氣自吸收塔底部通入,純堿溶液從吸收塔的頂部噴淋吸收氣體中的氧化氮,生成中和液。當中和液的相對密度為1.24~1.25、碳酸鈉含量為3~5g/l時,進行蒸發濃縮、冷卻結晶50~70℃析出亞硝酸鈉結晶,再經離心分離,制得亞硝酸鈉成品。其反應式如下。
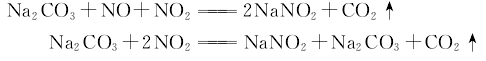
經離心分離出的母液,用作生產硝酸鈉的原料。
6.將1份工業品亞硝酸鈉溶解在1.5~2.0份70~80℃的純水中。添加固體試劑氫氧化鈉,調節PH值為12,靜置沉淀,然后過濾。濾液蒸發到密度為1.45時再過濾,濾液冷卻到室溫,析出的亞硝酸鈉晶體,用布氏漏斗抽濾,并不斷攪拌,用少量冷水洗滌,然后移入磨口瓶中。母液可再蒸發結晶而得到大量亞硝酸鈉,但需進行重結晶。
7.在氫氧化鈉醇溶液中加入亞硝酸乙酯,放置二天,進行如下反應:
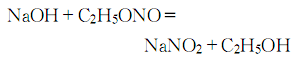
揮發物質,剩余物濾出(亞硝酸鈉含量高達91%~96%)后在水中進行重結晶,可得亞硝酸鈉含量95.5% ~99.8%。
用途
1.用作普通分析試劑、氧化劑和重氮化試劑,還用于亞硝酸鹽和亞硝基化合物的合成,食品添加劑(有毒,限量使用)。
2.用作媒染劑、漂白劑、金屬熱處理劑、電鍍緩蝕劑,醫藥上用作器械消毒劑、防腐劑等。
3.用于冰染染料、硫化染料、直接染料、酸性染料、分散染料、堿性染料、助染劑、H發孔劑的生產。也用于生產氨基偶氮苯、對位氨基苯酚等中間體。還用于有機顏料生產,如銀珠R、鮮艷大紅、大紅粉、燭紅、甲苯胺紫紅、猩紅色淀、立索爾大紅、紫醬色淀CK等。醫藥工業用于制造乙胺嘧啶、氨基吡啉等。用于生產香蘭素。用作絲綢和亞麻的漂白。織物染色的媒染劑。還用于金屬熱處理和電鍍緩蝕劑。用于切削油、潤滑油、抗凍液、液壓系統。
4.肉類制品加工中用作發色劑,可用于肉類罐頭、肉類制品。在肉制品中對抑制微生物的增殖有一定作用(對肉毒梭狀芽孢桿菌有特殊抑制作用),能提高腌肉的風味。
5.用作丁二烯與苯乙烯乳液共聚的終止劑之一。也用作織物染色的媒染劑,絲綢、亞麻的漂白劑,金屬熱處理劑,電鍍緩蝕劑,醫藥上利血管擴張劑及化學分析試劑以及制造亞硝酸鉀、硝基化合物、偶氮染料等的原料。
6.解毒藥。治療氰化物中毒的解毒過程與亞甲藍同,但作用較亞甲藍強。
7.用作丁二烯與苯乙烯乳液共聚的終止劑。還可用作織物染色的媒染劑,絲綢、亞麻的漂白劑,金屬熱處理劑,電鍍緩蝕劑,醫藥上作血管擴張劑及化學分析試劑,以及制造亞硝酸鉀、硝基化合物、偶氮染料等的原料。
8.用于冰染染料、硫化染料、直接染料、酸性染料、分散染料、堿性染料、助染劑。也用于生產對位氨基苯酚等中間體。還用于有機顏料生產,如銀珠R、鮮艷大紅、大紅粉、燭紅、甲苯胺紫紅、猩紅色淀、立索爾大紅及紫醬色淀CK等。醫藥工業用于制造乙胺嘧啶、氨基比林等。用于生產香蘭素。用于絲綢和亞麻的漂白,織物染色的媒染劑。還用于金屬熱處理和電鍍緩蝕劑。用于切削油、潤滑油、抗凍液及液壓系統。
9.用作水溶性膠黏劑和膠黏劑乳液的防腐劑。也用作制造硝基化合物、己內酰胺、偶氮染料、對氨基苯酚、硫化促進劑及香蘭素等的原料。醫藥上用于制造安乃近、氨茶堿、乙胺嘧啶及咖啡因等藥物。農藥工業中用于制造辛硫磷、殺螟松及退菌特等殺蟲劑。印染工業中用作棉纖維制品染色或印花的顯色劑、納夫妥染料染色的重氮化劑及拔染印花時底色保護劑。還用作絲綢、棉、麻漂白劑及丁烯氧化脫氫制丁二烯的精餾系統阻聚劑、電鍍緩蝕劑、金屬熱處理劑及抗凍劑等。食品級亞硝酸鈉用作食品添加劑時,最大使用量為0.15g/kg。殘留量:肉類罐頭≤0.05g/kg,肉制品≤0.03g/kg。
10.用于染料、醫藥工業制造染料和藥物,也用于有機合成。[28]
安全信息
危險運輸編碼:暫無
危險品標志: 有毒
有毒  氧化劑
氧化劑  危害環境
危害環境
文獻
1. Nielsen, M. A.; Nielsen, M. K.; Pittelkow, T. Org. Proc. Res. Dev., 2004, 8, 1059. 2. Siegrist, U.; Rapold, T.; Blaser, H.-U. Org. Proc. Res. Dev., 2003, 7, 429. 3. Jones, T. V.; Blatchly, R. A.; Tew, G. N. Org. Lett., 2003, 5, 3297. 4. Seela, F.; Lindner, M.; Glacüon, V.; Lin, W. J. Org. Chem., 2004, 69, 4695. 5. Matt, C.; Wagner, A.; Mioskowski, C. J. Org. Chem., 1997, 62, 234. 6. Hall, M. J.; McDonnell, S. O.; Killoran, J.; O’Shea, D. F. J. Org. Chem., 2005, 70, 5571. 7. Taddei, D.; Slawin, A. M.; Woollins, J. D. Eur. J. Org. Chem., 2005, 5, 939. 8. Glatzhofer, D. T.; Roy, R. R.; Cossey, K. N. Org. Lett., 2002, 4, 2349. 9. Liu, R.; Liang, X.; Dong, C.; Hu, X. J. Am. Chem. Soc., 2004, 126, 4112. 10. Sviridenko, F. B.; Stass, D. V.; Kobzeva, T. V.; Tretyakov, E. V.; Klyatskaya, S. V.; Mshvidobadze, E. V.; Vasilevsky, S. F.; Molin, Y. N. J. Am. Chem. Soc., 2004, 126, 2807. [1~10]參考書:現代有機合成試劑<性質、制備和反應>;胡躍飛 付華 編著;化學工業出版社;ISBN 7-5025-8542-7 [11~28]參考書:危險化學品安全技術全書.第一卷/張海峰主編.—2版.北京;化學工業出版社,2007.6 ISBN 978-7-122-00165-8
備注
暫無
表征圖譜
統計數據
共收錄化學品數據
147579 條




 滬公網安備 31010602001115號
滬公網安備 31010602001115號