高碘酸鉀 Potassium periodate
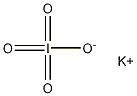
結構式
| 物競編號 | 0K7N |
|---|---|
| 分子式 | KIO4 |
| 分子量 | 230.00 |
| 標簽 | 偏高碘酸鉀, 偏過碘酸鉀, 高碘酸鉀, 過碘酸鉀, 過碘酸鉀, 過碘酸鉀, periodicacid(hio4),Potassiumsalt, Periodicacid(HIO4)potassiumsalt, Periodic acid potassium salt, Potassium periodate, Potassium Metaperiodate, potassium M- periodate, 氧化劑 |
編號系統
CAS號:7790-21-8
MDL號:MFCD00011407
EINECS號:232-196-0
RTECS號:暫無
BRN號:暫無
PubChem號:24852610
物性數據
1.性狀:無色結晶或白色粉末[1]
2.熔點(℃):582(爆炸)[2]
3.相對密度(水=1):3.62[3]
4.溶解性:微溶于冷水,溶于熱水。[4]
毒理學數據
1.急性毒性 暫無資料
2.刺激性 暫無資料
生態(tài)學數據
1.生態(tài)毒性 暫無資料
2.生物降解性 暫無資料
3.非生物降解性 暫無資料
分子結構數據
1、摩爾折射率:無可用的
2、摩爾體積(cm3/mol):無可用的
3、等張比容(90.2K):無可用的
4、表面張力(dyne/cm):無可用的
5、介電常數:無可用的
6、極化率:無可用的
7、單一同位素質量:229.847825 Da
8、標稱質量:230 Da
9、平均質量:230.0004 Da
計算化學數據
1.疏水參數計算參考值(XlogP):無
2.氫鍵供體數量:0
3.氫鍵受體數量:4
4.可旋轉化學鍵數量:0
5.互變異構體數量:無
6.拓撲分子極性表面積74.3
7.重原子數量:6
8.表面電荷:0
9.復雜度:118
10.同位素原子數量:0
11.確定原子立構中心數量:0
12.不確定原子立構中心數量:0
13.確定化學鍵立構中心數量:0
14.不確定化學鍵立構中心數量:0
15.共價鍵單元數量:2
性質與穩(wěn)定性
1.穩(wěn)定性[5] 穩(wěn)定
2.禁配物[6] 強還原劑、易燃或可燃物、活性金屬粉末、硫、磷、活性金屬粉末
3.避免接觸的條件[7] 受熱
4.聚合危害[8] 不聚合
貯存方法
儲存注意事項[9] 儲存于陰涼、通風的庫房。遠離火種、熱源、庫溫不超過30℃,相對濕度不超過80%。避免光照。包裝密封。應與易(可)燃物、還原劑等分開存放,切忌混儲。儲區(qū)應備有合適的材料收容泄漏物。
合成方法
1.氯氣氧化法 將碘在水介質中,通入氯氣進行氧化生成高碘酸,經分離雜質后,加入氫氧化鉀溶液中和至pH值為2~3,生成高碘酸鉀溶液,再經提純,分離雜質,蒸發(fā)濃縮,冷卻結晶,離心分離,干燥,制得高碘酸鉀成品。其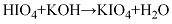
2.在堿性條件下用過二硫酸鉀氧化碘酸鉀制取。加熱將65g KIO3溶解在200mL 30%的KOH溶液中,把溶液加熱至沸,在攪拌下一點點加入100g K2S2O8。反應物繼續(xù)煮沸5~10min后冷至室溫。將溶液從K2SO4結晶中倒出,KIO4仍留在堿性溶液里。用少量水洗滌沉淀,洗滌水與堿液合并。用硫酸中和溶液到對甲基橙呈中性,濾出析出的KIO4,并用冰水洗到如下情況為止:把幾滴洗滌水加到硝酸酸化的BaCl2和AgNO3溶液中時,僅稍有渾濁。KIO4結晶在瓷皿中在100~105℃干燥。產量55~60g(依KIO3計產率80%~85%)。
3.將碘酸鉀溶解在30%的氫氧化鉀溶液中并加熱煮沸,攪拌下分次少量地加入過硫酸鉀,反應生成高碘酸鉀:

加完過硫酸鉀后繼續(xù)煮沸5~10min,停止加熱,冷卻至室溫,析出物為硫酸鉀(高碘酸鉀溶于氫氧化鉀,留在溶液中),濾出硫酸鉀沉淀,用少量水洗滌沉淀。洗液與濾液合并后,用硫酸中和溶液呈中性(用甲基橙檢驗),高碘酸鉀析出,過濾,用冰水洗滌結晶至 SO42-離子含量合格,離心甩干,于100~105℃ 下干燥,得分析純高碘酸鉀。
4.將工業(yè)品氯酸鉀溶于水中,濾去不溶物,加入升華結晶碘,再通氯氣鼓泡,并加熱5-10min,然后加入33%的過量的氫氧化鉀溶液(試劑級),加熱后繼續(xù)通入氯氣至溶液飽和,將溶液冷卻結晶,濾后甩干,再用14倍量的水進行重結晶,得到的是分析純高碘酸鉀。
用途
1.用作氧化劑,主要用于氧化錳酸鹽成高錳酸鹽。[10]
安全信息
危險運輸編碼:UN 1479 5.1/PG 2
危險品標志: 氧化劑
氧化劑  刺激
刺激
文獻
[1~10]參考書:危險化學品安全技術全書.第一卷/張海峰主編.—2版.北京;化學工業(yè)出版社,2007.6 ISBN 978-7-122-00165-8
備注
暫無
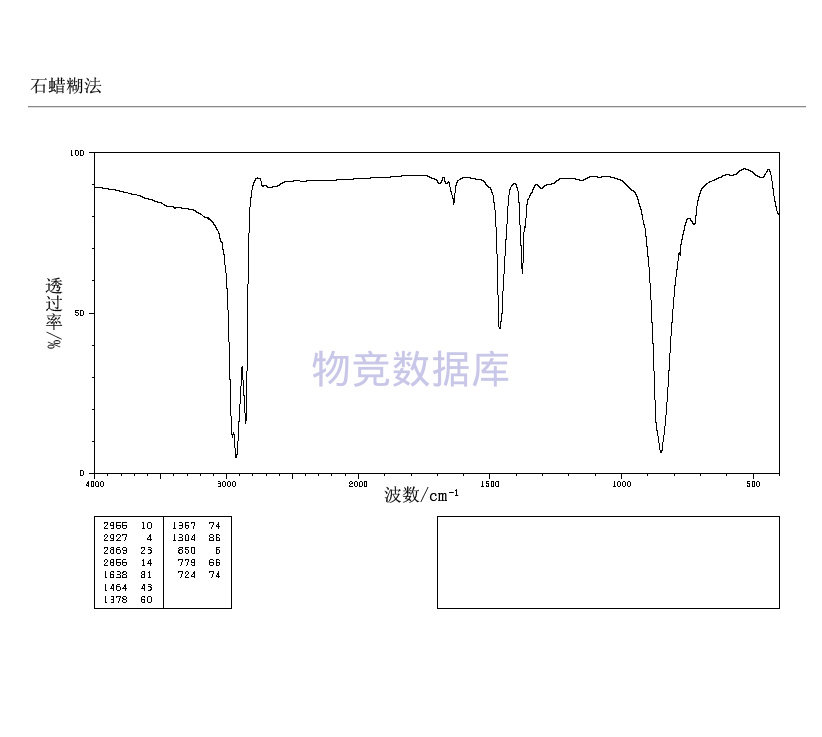
表征圖譜
統計數據
共收錄化學品數據
147579 條



 滬公網安備 31010602001115號
滬公網安備 31010602001115號