n-丁基鋰 n-Butyllithium

結(jié)構(gòu)式
| 物競編號 | 02ZL |
|---|---|
| 分子式 | C4H9Li |
| 分子量 | 64.05 |
| 標(biāo)簽 | 正丁基鋰, 太陽能電池化學(xué)品 |
編號系統(tǒng)
CAS號:109-72-8
MDL號:MFCD00009414
EINECS號:203-698-7
RTECS號:暫無
BRN號:1209227
PubChem號:24858234
物性數(shù)據(jù)
1.性狀:無色至黃色透明液體,接觸空氣發(fā)生燃燒。[15]
2.熔點(℃):-76[16]
3.沸點(℃):80~90(0.0133Pa)[17]
4.閃點(℃):-12[18]
5.溶解性:不溶于水,溶于戊烷、己烷、環(huán)己烷、苯、醚類、烴。[19]
毒理學(xué)數(shù)據(jù)
1.急性毒性 暫無資料
2.刺激性 暫無資料
生態(tài)學(xué)數(shù)據(jù)
1.生態(tài)毒性 暫無資料
2.生物降解性 暫無資料
3.非生物降解性 暫無資料
分子結(jié)構(gòu)數(shù)據(jù)
暫無
計算化學(xué)數(shù)據(jù)
1.疏水參數(shù)計算參考值(XlogP):無
2.氫鍵供體數(shù)量:0
3.氫鍵受體數(shù)量:1
4.可旋轉(zhuǎn)化學(xué)鍵數(shù)量:1
5.互變異構(gòu)體數(shù)量:無
6.拓?fù)浞肿訕O性表面積0
7.重原子數(shù)量:5
8.表面電荷:0
9.復(fù)雜度:7.6
10.同位素原子數(shù)量:0
11.確定原子立構(gòu)中心數(shù)量:0
12.不確定原子立構(gòu)中心數(shù)量:0
13.確定化學(xué)鍵立構(gòu)中心數(shù)量:0
14.不確定化學(xué)鍵立構(gòu)中心數(shù)量:0
15.共價鍵單元數(shù)量:2
性質(zhì)與穩(wěn)定性
1.正丁基鋰溶液暴露于空氣或濕氣時易起火。對正丁基鋰的操作應(yīng)在與水蒸氣和O2隔離后進(jìn)行,并穿戴好護(hù)目鏡、防腐手套等安全裝備。一旦著火,應(yīng)用干粉滅火器撲滅,千萬不可使用含水或氯代烷烴的滅火器。正丁基鋰參與的反應(yīng)應(yīng)在隔絕空氣和濕氣的氮氣或氬氣保護(hù)下,使用時一定要小心謹(jǐn)慎。
2.穩(wěn)定性[20] 穩(wěn)定
3.禁配物[21] 酸類、醇類、水、空氣、鹵素類和胺類
4.避免接觸的條件[22] 潮濕空氣
5.聚合危害[23] 不聚合
6.分解產(chǎn)物[24] 氧化鋰
貯存方法
儲存注意事項[25] 儲存于陰涼、干燥、通風(fēng)良好的專用庫房內(nèi),遠(yuǎn)離火種、熱源。庫溫不超過30℃,相對濕度不超過80%。包裝必須密封,切勿受潮。應(yīng)與酸類、醇類等分開存放,切忌混儲。不宜大量儲存或久存。采用防爆型照明、通風(fēng)設(shè)施。禁止使用易產(chǎn)生火花的機(jī)械設(shè)備和工具。儲區(qū)應(yīng)備有泄漏應(yīng)急處理設(shè)備和合適的收容材料。
合成方法
1.可以通過氯代正丁烷或溴代正丁烷與金屬鋰在乙醚或烴類溶劑中反應(yīng)制備而來。
用途
1.用于制備各種烷基、芳基衍生物的有機(jī)金屬化合物,是生產(chǎn)太陽能電池的原料。
2.是重要的鋰試劑。與鹵代烷和有機(jī)化合物中的活性氫交換而將鏗原子引入其中,繼而可進(jìn)行許多反應(yīng)。也用作聚合反應(yīng)引發(fā)劑。
3.正丁基鋰作為一個強(qiáng)堿,能夠作為含活潑氫底物的鋰化試劑,也能用于鋰-鹵交換反應(yīng)或鋰-金屬轉(zhuǎn)移金屬化反應(yīng)[1]。
作為異丁基鋰和叔丁基鋰的同類物質(zhì),正丁基鋰的堿性和反應(yīng)活性都較差一些,但對于含活潑氫的底物,卻是一個有效的脫質(zhì)子試劑,特別是當(dāng)形成的是雜原子陰離子或形成的碳陰離子能夠被共軛效應(yīng)穩(wěn)定(如陰離子在sp碳上)時。因而,多種含氧、氮、磷的有機(jī)底物,以及茚、三苯甲烷、乙烯基苯或甲基雜芳環(huán)化合物(如吡啶、喹啉等)等含苯基的底物,能夠很容易與正丁基鋰反應(yīng)形成鋰鹽。典型的如丙二烯依據(jù)不同的取代基位置及取代烷基空間大小的不同在C-1或C-3位發(fā)生的鋰化反應(yīng),或端炔在丁基鋰作用下生成炔基鋰的反應(yīng)都很容易實現(xiàn)。丙炔氫也很容易被正丁基鋰奪取,當(dāng)端炔與兩當(dāng)量的正丁基鋰反應(yīng)時會在丙炔基和端炔位發(fā)生雙鋰化反應(yīng) (式1)[2]。
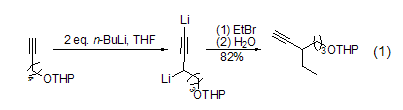
正丁基鋰的金屬化活性在給電子溶劑如THF或乙醚中要比在普通烴類溶劑中強(qiáng),這是因為給電子溶劑能夠與缺電子的鋰發(fā)生配位,進(jìn)而促進(jìn)低階有機(jī)鋰的聚集。而在普通烴類溶劑中,正丁基鋰會形成高階聚集。通常正丁基鋰都是在配體存在下使用的,如加入N,N,N′, N′-四甲基乙二胺 (N,N, N′, N′-Tetramethylethylenedi- amine, TMEDA) 或1,4-二氮雜二環(huán)[2.2.2]辛烷 (1,4-diazabicyclo[2.2.2]octane, DABCO) 都能活化正丁基鋰進(jìn)而促進(jìn)鋰化反應(yīng),如原本惰性的苯在這些添加物存在下也能與正丁基鋰作用發(fā)生鋰化或多鋰化反應(yīng)。烯丙基化合物或苯基α-位不含活化基團(tuán)的芐基苯也能在活化配體存在下與正丁基鋰反應(yīng) (式2)[3]。
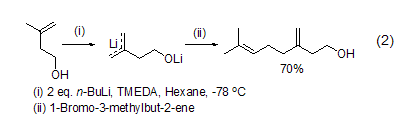
金屬醇化物也可以作為添加劑起到活化正丁基鋰的作用,如添加叔丁基鉀后的混合試劑n-BuLi/t-BuOK能夠?qū)崿F(xiàn)芳基炔的雙金屬化反應(yīng),進(jìn)而被親電試劑進(jìn)攻得到鄰取代芳基炔化合物 (式3)[4]。

含雜原子如氧、硫、氮的化合物能夠與正丁基鋰反應(yīng)能夠選擇性得到α-脫質(zhì)子產(chǎn)物。如1,3-二硫化合物能發(fā)生兩次α-位鋰化反應(yīng),揭示了1,3-二硫化合物作為保護(hù)基團(tuán)的用途 (式4)[5]。
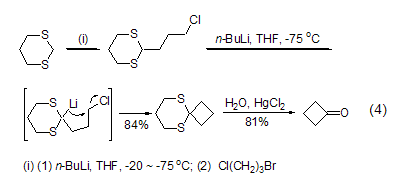
當(dāng)在足夠低的溫度 (如–78 oC)下 反應(yīng)時,α-位脫質(zhì)子過程要比同分子存在親電中心的親核加成反應(yīng)快,這是控制正丁基鋰反應(yīng)的一條重要策略。如先控制較低溫度發(fā)生鋰化反應(yīng),然后升溫發(fā)生對新形成C-Li鍵的分子內(nèi)親核加成反應(yīng) (式5)[6]。
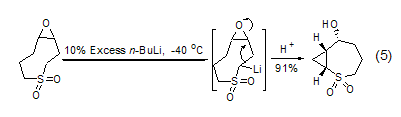
當(dāng)?shù)孜锖心芘cLi配位的雜原子如羰基氧時,雜原子鄰位的氫很容易被脫除發(fā)生鋰化反應(yīng),這是因為形成了“偶極穩(wěn)定”的碳陰離子。如2-烯基-N,N-二烷基氨基甲酸酯在–78 oC及正丁基鋰/TMEDA的作用下發(fā)生快速的α-脫質(zhì)子反應(yīng),得到的偶極穩(wěn)定的碳陰離子再與酮或醛作用就能高立體選擇性地形成γ-羥基烷基烯醇醚 (式6)[7]。
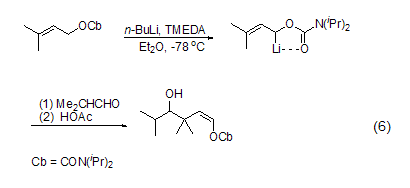
含雜原子取代基的芳香化合物與正丁基鋰作用會選擇性地發(fā)生鄰位鋰化反應(yīng),如NR2、CH2NR2、CH2CH2NR2、OMe、C=NR、SO2NR2等基團(tuán)都能促使芳香環(huán)上的鄰位鋰化反應(yīng),這種鄰位鋰化反應(yīng)在合成上具有非常重要的用途 (式7)[8]。
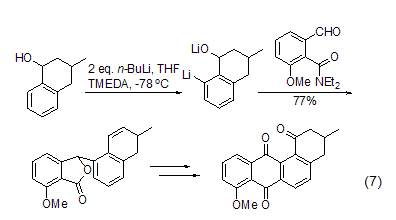
正丁基鋰的另一類重要反應(yīng)是與鹵代有機(jī)底物發(fā)生鋰-鹵交換反應(yīng),這是在有機(jī)合成上非常重要的一種獲得有機(jī)鋰化合物的方法,特別是對芳基鋰、乙烯基鋰和環(huán)丙基鋰的合成非常有用。與鹵素取代基發(fā)生交換反應(yīng)的活性按I > Br > Cl > F遞減,對于含氟取代基的芳香烴基本上不會與正丁基鋰發(fā)生反應(yīng) (式8)[9]。而對于碘化物,則很容易與正丁基鋰作用發(fā)生鋰鹵交換,進(jìn)而與醛或酮等親電試劑反應(yīng)得到加成產(chǎn)物 (式9)。
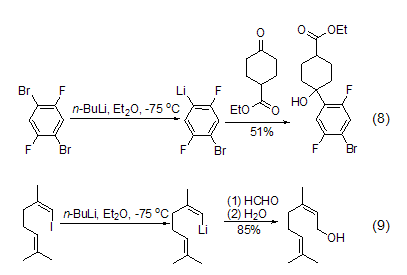
除了鋰鹵交換反應(yīng)外,正丁基鋰還很容易與其它含錫、硒、碲或汞的有機(jī)金屬試劑發(fā)生作用,發(fā)生轉(zhuǎn)移金屬化反應(yīng)。反應(yīng)通常在低溫和醚類溶劑中進(jìn)行。其中,錫-鋰交換反應(yīng)在合成上最為重要,可用于合成芳基和乙烯基鋰化合物 (式10,式11)[10,11]。

包括芐基、乙烯基、炔基和烷氧基鋰在內(nèi)的許多有機(jī)鋰試劑也可以通過Li-Te交換反應(yīng)而來 (式12)[12]。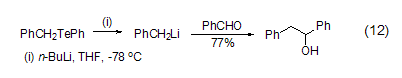
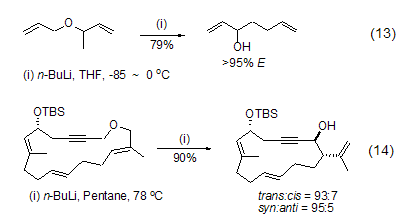
正丁基鋰也經(jīng)常用于陰離子重排反應(yīng)。如烯丙基醚或丙炔基醚在正丁基鋰作用下發(fā)生2,3-Wittig重排。反應(yīng)通常先在低溫下通過α-脫質(zhì)子反應(yīng)或Li-Sn交換反應(yīng)得到陰離子,然后再升溫發(fā)生分子內(nèi)重排 (式13,式14)[13,14]。
4.用作聚合催化劑、烴化劑、火箭燃料等。[26]
安全信息
危險運輸編碼:UN 3399 4.3/PG 1
危險品標(biāo)志: 易燃
易燃  腐蝕
腐蝕  危害環(huán)境
危害環(huán)境
安全標(biāo)識:S6 S9 S16 S26 S45 S61 S62 S36/S37/S39
危險標(biāo)識:R11 R34 R65 R67 R14/15 R50/53
文獻(xiàn)
1. (a) Mugesh, G.; Singh, H. B. Acc. Chem. Res., 2002, 35, 226. (b) Wakefield, B. J. The Chemistry of Organolithium Com- pounds, Pergamon: Oxford, 1974. (c) Wakefield, B. J. Organolithium Methods; Academic: San Diego, 1990. (d)Wardell, L. J. In Comperhensive Organometallic Chemistry, Wilkinson, G., Ed.; Pergamon: Oxford, 1982. Chapetr 2. 2. Takashi, K.; Konishi, K.; Ushio, M.; Takaki, M.; asami, R. J. Organometa. Chem., 1973, 50, 1. 3. Akiyama, S.; Hooz, J. Tetrahedron Lett., 1973, 41, 15. 4. Hommes, H.; Verkruijsse, H. D.; Brandsma, L. Tetrahedron Lett., 1981, 22, 2495. 5. Seebach, D.; Beck, A. K. Org. Synth., Coll. Vol., 1988, 6, 316. 6. Cere, V,: Paolucci, C.; Pollicino, S.; Sandri, E.; Fava, A. J. Org. Chem., 1991, 56, 4513. 7. Meyers, A. I.; Edwards, P. D.; Rieker, W. F.; Bailey, T. R. J. Am. Chem. Soc., 1984, 106, 3270. 8. (a) Slocum, D. W.; Jennings, C. A. J. Org. Chem., 1976, 41, 3653. (b) Turner, J. A. J. Org. Chem., 1983, 48, 3401. 9. Kitatani, K.; Hiyama, T.; Nizaki, H. J. Am. Chem. Soc., 1975, 97, 949. 10. Sawyer, J. S.; Macdonald, T. L; McGarvery, G. J. J. Am. Chem. Soc., 1984, 106, 3376. 11. Broka, C. A.; Shen, T. J. Am. Chem. Soc., 1989, 111, 2981. 12. Tomoki, H.; Kambe, N.; Ogawa, A.; Miyoshi, N.; Murai, S.; Sonoda, N. Angew. Chem. Ed. Int. Engl., 1987, 26, 1187 . 13. Nakai, T.; Mikami, K.; Taya.; S.; Fujira, Y. J. Am. Chem. Soc., 1981, 103, 6492. 14. (a) Marshall, J. A.; Robinson, E. D.; Lebreton, J. J. Org. Chem., 1990, 55, 227. (b) Takashi, T.; Nemoto, H.; Kanda, Yanda, Y.; Tsuji, J.; Fujise, Y. J. Org. Chem.,1986, 51, 4315. [1~14]參考書:現(xiàn)代有機(jī)合成試劑<性質(zhì)、制備和反應(yīng)>;胡躍飛 付華 編著;化學(xué)工業(yè)出版社;ISBN 7-5025-8542-7 [15~26]參考書:危險化學(xué)品安全技術(shù)全書.第一卷/張海峰主編.—2版.北京;化學(xué)工業(yè)出版社,2007.6 ISBN 978-7-122-00165-8
備注
暫無
表征圖譜
統(tǒng)計數(shù)據(jù)
共收錄化學(xué)品數(shù)據(jù)
147579 條




 滬公網(wǎng)安備 31010602001115號
滬公網(wǎng)安備 31010602001115號