乙醇 Ethanol
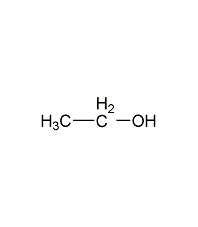
結構式
| 物競編號 | 01D6 |
|---|---|
| 分子式 | C2H6O |
| 分子量 | 46.07 |
| 標簽 | 無水酒精, 酒精, 火酒, 無水乙醇, Ethyl alcohol, Anhydrous alcohol, Ethylhydrate, 橡膠助劑, 防凍液, 燃料, 消毒劑, 醇類溶劑, 脂肪族醇、醚及其衍生物 |
編號系統
CAS號:64-17-5
MDL號:MFCD00003568
EINECS號:200-578-6
RTECS號:KQ6300000
BRN號:1718733
PubChem號:24872843
物性數據
1.性狀:無色液體,有酒香。[1]
2.熔點(℃):-114.1[2]
3.沸點(℃):78.3[3]
4.相對密度(水=1):0.79(20℃)[4]
5.相對蒸氣密度(空氣=1):1.59[5]
6.飽和蒸氣壓(kPa):5.8(20℃)[6]
7.燃燒熱(kJ/mol):-1365.5[7]
8.臨界溫度(℃):243.1[8]
9.臨界壓力(MPa):6.38[9]
10.辛醇/水分配系數:0.32[10]
11.閃點(℃):13(CC);17(OC)[11]
12.引燃溫度(℃):363[12]
13.爆炸上限(%):19.0[13]
14.爆炸下限(%):3.3[14]
15.溶解性:與水混溶,可混溶于乙醚、氯仿、甘油、甲醇等多數有機溶劑。[15]
16.黏度(mPa·s,15oC):0.6405
17.黏度(mPa·s,20oC):0.5945
18.黏度(mPa·s,25oC):0.5525
19.黏度(mPa·s,30oC):0.5142
20.閃點(oC,開口):16.0
21.閃點(oC,閉口):14.0
22.蒸發熱(KJ/mol,b.p.):38.95
23.熔化熱(KJ/kg):104.7
24.生成熱(KJ/mol,液體):-277.8
25.比熱容(KJ/(kg·K),20oC,定壓):2.42
26.沸點上升常數:1.03~1.09
27.電導率(S/m):1.35×10-19
28.熱導率(W/(m·K)):18.00
29.體膨脹系數(K-1,20oC):0.00108
30.臨界密度(g·cm-3):0.275
31.臨界體積(cm3·mol-1):168
32.臨界壓縮因子:0.241
33.偏心因子:0.637
34.Lennard-Jones參數(A):4.5564
35.Lennard-Jones參數(K):424.51
36.溶度參數(J·cm-3)0.5:26.421
37.van der Waals面積(cm2·mol-1):4.930×109
38.van der Waals體積(cm3·mol-1):31.940
39.氣相標準燃燒熱(焓)(kJ·mol-1):1410.01
40.氣相標準聲稱熱(焓)( kJ·mol-1) :-234.01
41.氣相標準熵(J·mol-1·K-1) :280.64
42.氣相標準生成自由能( kJ·mol-1):-166.7
43.氣相標準熱熔(J·mol-1·K-1):65.21
44.液相標準燃燒熱(焓)(kJ·mol-1):-1367.54
45.液相標準聲稱熱(焓)( kJ·mol-1):-276.98
46.液相標準熵(J·mol-1·K-1) :161.04
47.液相標準生成自由能( kJ·mol-1):-174.18
48.液相標準熱熔(J·mol-1·K-1):112.6
49.
毒理學數據
1.急性毒性[16]
LD50:7060mg/kg(大鼠經口);7060mg/kg(兔經口);7430mg/kg(兔經皮)
LC50:20000ppm(大鼠吸入,10h)
2.刺激性[17]
家兔經皮:20mg(24h),中度刺激。
家兔經驗:500mg,重度刺激。
3.亞急性與慢性毒性[18] 大鼠經口10.2g/(kg·d),12周,體重下降,脂肪肝。
4.致突變性[19] 微生物致突變:鼠傷寒沙門菌11%。顯性致死試驗:小鼠經口1~1.5g/kg(每天,2周)陽性。細胞遺傳學分析:人淋巴細胞2.5%(24h)。姐妹染色單體交換:人淋巴細胞500ppm(72h)。DNA抑制:人淋巴細胞220mmol/L。微核試驗:狗淋巴細胞,400μmol/L。
5.致畸性[20] 猴孕后2~17周經口給予最低中毒劑量(TDLo)32400mg/kg,致中樞神經系統和顱面部(包括鼻、舌)發育畸形。大鼠、小鼠、豚鼠、家畜孕后不同時間經口、靜脈內、腹腔內途徑給予不同劑量,致中樞神經系統、泌尿生殖系統、內分泌系統、肝膽管系統、呼吸系統、顱面部(包括鼻、舌)、眼、耳發育畸形。雄性大鼠交配前30d經口給予240g/kg,致泌尿生殖系統發育畸形。
6.致癌性[21] IARC致癌性評論:對動物致癌性證據有限。
7.其他[22] 小鼠腹腔最低中毒劑量(TDLo):7.5g/kg(孕9d),致畸陽性。
生態學數據
1.生態毒性[23]
LC50:13g/L(96h)(虹鱒魚,靜態);14.2~15.3g/L(96h)(黑頭呆魚);9268~14221mg/L(48h)(水蚤,靜態)
IC50:1450mg/L(72h)(藻類)
2.生物降解性[24]
好氧生物降解性(h):6.5~26
厭氧生物降解性(h):26~104
3.非生物降解性[25]
水中光氧化半衰期(h):8020~3.20×105
空氣中光氧化半衰期(h):12.2~122
分子結構數據
1、摩爾折射率:12.84
2、摩爾體積(cm3/mol):59.0
3、等張比容(90.2K):128.4
4、表面張力(dyne/cm):22.3
5、極化率(10-24cm3):5.09
計算化學數據
1.疏水參數計算參考值(XlogP):-0.1
2.氫鍵供體數量:1
3.氫鍵受體數量:1
4.可旋轉化學鍵數量:0
5.互變異構體數量:無
6.拓撲分子極性表面積20.2
7.重原子數量:3
8.表面電荷:0
9.復雜度:2.8
10.同位素原子數量:0
11.確定原子立構中心數量:0
12.不確定原子立構中心數量:0
13.確定化學鍵立構中心數量:0
14.不確定化學鍵立構中心數量:0
15.共價鍵單元數量:1
性質與穩定性
1.化學性質:乙醇是醇類的代表物質,化學性質如下所示。
① 生成金屬衍生物乙醇與鈉、鉀等堿金屬反應生成乙醇化物;低級醇容易發生此反應,有時有著火的危險
2C2H5OH + 2Na→2C2H5ONa + H2
高級醇反應較慢,特別是高級仲醇、叔醇反應速度小,不容易生成醇化物;鋁、鎂、鈣、鋇等金屬與醇一起煮沸,也能生成醇化物。
② 生成酯醇與有機酸、無機酸反應時脫水生成酯,反應是可逆的
C2H5OH + RCOOH→RCOOC2H5 + H2O
此反應常用強酸、金屬鹽、離子交換樹脂等作催化劑;甲醇的反應性最大,C2~C5的伯醇反應速度大致相等;仲醇、叔醇的反應性小,而且叔醇在酸性介質中容易脫水生成烯烴,一般用間接的方法制備叔醇的酯;酰氯和酸酐與醇更易進行酯化反應。
③ 生成鹵代烷乙醇與鹵代氫、亞硫酰氯或鹵化磷反應時,羥基被鹵原子置換,生成鹵代烷。
叔醇的反應速度最快,仲醇、伯醇的反應速度依次降低;鹵化氫以碘化氫最快,氯化氫最慢。
④ 脫水反應醇的脫水有分子間脫水和分子內脫水兩種方式;分子間脫水生成醚,分子內脫水生成烯烴。反應按哪種方式進行取決于醇的結構和反應條件;一般高溫有利于生成烯烴,低溫有利于生成醚;叔醇易脫水成烯,難以得到醚;反應常在催化劑存在下進行,常用的催化劑有硫酸、磷酸、三氧化二鋁、磷酸鋁等。
⑤ 縮醛的生成乙醇在室溫下與醛反應生成半縮醛,并放出熱量。在酸性催化劑如HCl、H2SO4或CaCl2存在下,進一步與1mol醇反應生成縮醛。
⑥ 氧化反應伯醇氧化生成醛,醛再繼續氧化成羧酸。仲醇氧化生成酮。叔醇難氧化,但在劇烈的條件下氧化生成碳原子數較叔醇少的產物。常用的氧化劑有重鉻酸鈉、硫酸或三氧化鉻和冰乙酸。乙醇氧化生成乙醛或乙酸。
⑦ 脫氫反應伯醇或仲醇的蒸氣在高溫下通過脫氫催化劑如銅、銀、鎳或銅氧化鉻時,則脫氫生成醛或酮。叔醇不能脫氫,只能脫水成烯烴。
⑧ 其他乙醇易與乙烯酮、環氧乙烷、異氰酸酯等反應性大的物質發生反應,分別生成乙酸酯、烷氧基醇和氨基甲酸乙酯;乙醇用漂白粉溶液氧化生成氯仿,用碘和氫氧化鉀氧化生成碘仿;與不含亞硝酸的硝酸作用生成硝酸乙酯;與汞和過量的硝酸作用生成雷酸汞Hg(ONC)2;與氧化汞和氫氧化鈉一起加熱生成爆炸性物質C2Hg6O4H2。
2.與鉻酸、次氯酸鈣、過氧化氫、硝酸、硝酸鉑、過氮酸鹽及氧化劑反應劇烈,有發生爆炸的危險。易揮發,極易燃燒,火焰淡藍色。蒸氣與空氣能形成爆炸混合物,爆炸極限4.3%~19.0%(vol)。具有吸濕性,與水形成共沸混合物。微毒。
3.穩定性[26] 穩定
4.禁配物[27] 強氧化劑、酸類、酸酐、堿金屬、胺類
5.聚合危害[28] 不聚合
貯存方法
儲存注意事項[29] 儲存于陰涼、通風的庫房。遠離火種、熱源。庫溫不宜超過37℃。保持容器密封。應與氧化劑、酸類、堿金屬、胺類等分開存放,切忌混儲。采用防爆型照明、通風設施。禁止使用易產生火花的機械設備和工具。儲區應備有泄漏應急處理設備和合適的收容材料。
合成方法
1. 發酵法:將富含淀粉的農產品如谷類、薯類等或野生植物果實經水洗、粉碎后,進行加壓蒸煮,使淀粉糊化,再加入適量的水,冷卻至60℃左右加入淀粉酶,使淀粉依次水解為麥芽糖和葡萄糖。然后加入酶母菌進行發酵制得乙醇。
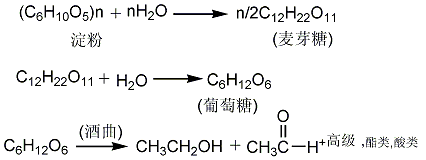
2. 水合法:以乙烯和水為原料,通過加成反應制取。水合法分為間接水合法和直接水合法兩種。間接水合法也稱硫酸酯法,反應分兩步進行。先把95-98%的硫酸和50-60%的乙烯按2:1(重量比)在塔式反應器吸收反應,60-80℃、0.78-1.96MPa條件下生成硫酸酯。
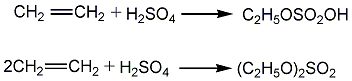
第二步是將硫酸酯在水解塔中,于80-100℃、0.2-0.29MPa壓力下水解而得乙醇,同時生成副產物乙醚。烯直接與水反應生成乙醇。
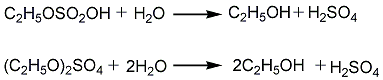
直接水合法即一步法。由乙烯和水在磷酸催化劑存在下高溫加壓水合制得。本法流程簡單、腐蝕性小,不需特殊鋼材,副產乙醚量少,但要求乙烯純度高,耗電量大。
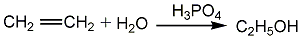
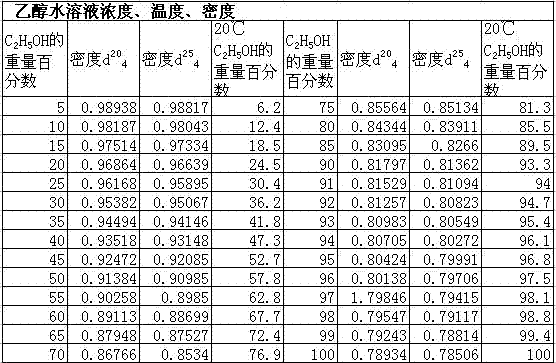
無論用發酵法或乙烯水合法,制得的乙醇通常都是乙醇和水的共沸物,即濃度為95%的工業乙醇。為獲得無水乙醇,可用下列方法進一步脫水。(1)用生石灰處理工業乙醇,使水轉變成氫氧化鈣,然后蒸出乙醇,再用金屬鈉干燥;這是最老的方法。(2)共沸精餾脫水是目前工業上常用的方法。(3)用離子交換劑或分子篩脫水,然后再精餾。
3.在磷酸、硅藻土催化劑存在下,乙烯直接與水反應生成乙醇。
4.以工業乙醇為原料,經脫水處理,再在高效精餾塔內進行精餾,所得成品用微孔濾膜過濾即可。
5.選擇含氧化鈣高,鐵、鎂、硫雜質少的干燥生石灰,破碎成直徑30mm 的小塊,并去除老灰、石頭及消石灰,然后與2倍質量的工業乙醇混合,加熱使乙醇回流,約18h后,脫水結束。快速蒸出乙醇,經精餾,去除少量頭液,即可得99.5%以上的試劑無水乙醇。也可將95%的乙醇通過孔徑4.2×10-9的Na型分子篩進行脫水和脫甲醇,然后再精餾。該分子篩可于400~500℃高 溫 下 烘3h,活 化 后,重 新使用。
6.以乙二醇醋酸鉀溶液為萃取劑,與工業乙醇等量混合后,在高效精餾塔中精餾,可獲得99.7%以上的無水乙醇。
7.用戊烷或石油醚作為共沸劑于0.3~0.7MPa下精餾,可獲得99.9%以上的無水乙醇。
8.在帶有氯化鈣干燥管的容器中加入制得的無水乙醇和適量金屬鈣,使金屬鈣充分吸收水分后,蒸餾可得符合氣相色譜標準的無水乙醇,乙醇含量大于99.95%。也可以工業乙醇為原料,經恒沸精餾、氣相制備色譜分離和純化而得符合氣相色譜標準的無水乙醇。
9.純制制絕對乙醇時,可用金屬鎂或金屬鈉去除無水乙醇中的微量水份。含水量較大的乙醇不能直接用來制絕對乙醇。用金屬鎂去除水份的方法:在裝有回流冷凝器(頂端帶氯化鈣干燥管〕的1升園底燒瓶中,依次放入2一3克潔凈的鎂條,0.3克碘和30毫升99.5帕乙醇,在水浴上加熱至碘粒完全消失(如果不起反應,可再加入幾小粒碘)。繼續加熱,待鎂完全溶解后,加入500毫升99.5%乙醇。回流1小時后,蒸出乙醇,棄去10毫升前餾分,其余收集于干燥瓶內貯存。此乙醇的純度>99.95%。用金屬鈉去除水份的方法:裝置同上。將500毫升99.5%乙醇和3.5克鈉依次加入瓶中,待完全作用后,再加入幾粒沸石和12.5克丁二酸乙醋或14克鄰苯二甲酸二乙醋,回流2小時,然后蒸餾。棄去10毫升前餾分,其余收集于干燥的瓶內貯存。乙醇中微量水分測定:加入乙醇鋁的苯溶液,若有大量白色沉淀生成,表明乙醇中水分含量超過0.05%。
用途
1.乙醇是重要的有機溶劑,廣泛用于醫藥、涂料、衛生用品、化妝品、油脂等各個方法,占乙醇總耗量的50%左右。乙醇是重要的基本化工原料,用于制造乙醛、乙二烯、乙胺、乙酸乙酯、乙酸、氯乙烷等等,并衍生出醫藥、染料、涂料、香料、合成橡膠、洗滌劑、農藥等產品的許多中間體,其制品多達300種以上,但目前乙醇作為化工產品中間體的用途正在逐步下降,許多產品例如乙醛、乙酸、乙基乙醇已不再采用乙醇作原料而用其他原料代替。75%的乙醇水溶液具有強殺菌能力,是常用的消毒劑。經過專門精制的乙醇也可用于制造飲料。與甲醇類似,乙醇可作能源使用。有的國家已開始單獨用乙醇作汽車燃料或摻到汽油(10%以上)中使用以節約汽油。
2.用作黏合劑、硝基噴漆、清漆、化妝品、油墨、脫漆劑等的溶劑以及農藥、醫藥、橡膠、塑料、人造纖維、洗滌劑等的制造原料,還可作防凍液、燃料、消毒劑等。在微電子工業中,用作脫水去污劑,可與去油劑配合使用。
3.用作分析試劑,如作溶劑。還用于制藥工業。
4.用于電子工業,用作脫水去污劑及去油劑配料。5.用于溶解一些不溶于水的電鍍有機添加劑,在分析化學中也用作六價鉻的還原劑。
5.用于制酒工業、有機合成、消毒以及用作溶劑。[30]
安全信息
危險運輸編碼:UN 1170 3/PG 2
危險品標志: 易燃
易燃  有毒
有毒  有害
有害
危險標識:R10 R11 R20/21/22 R36/37/38 R39/23/24/25
文獻
[1~30]參考書:危險化學品安全技術全書.第一卷/張海峰主編.—2版.北京;化學工業出版社,2007.6 ISBN 978-7-122-00165-8
備注
暫無
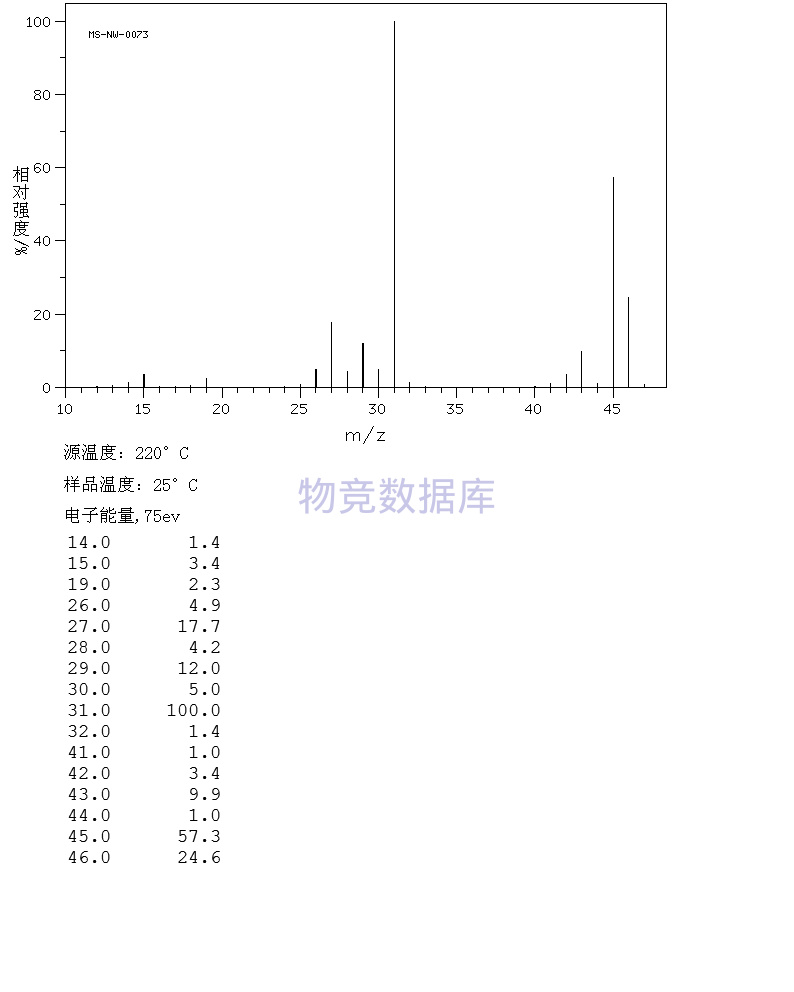
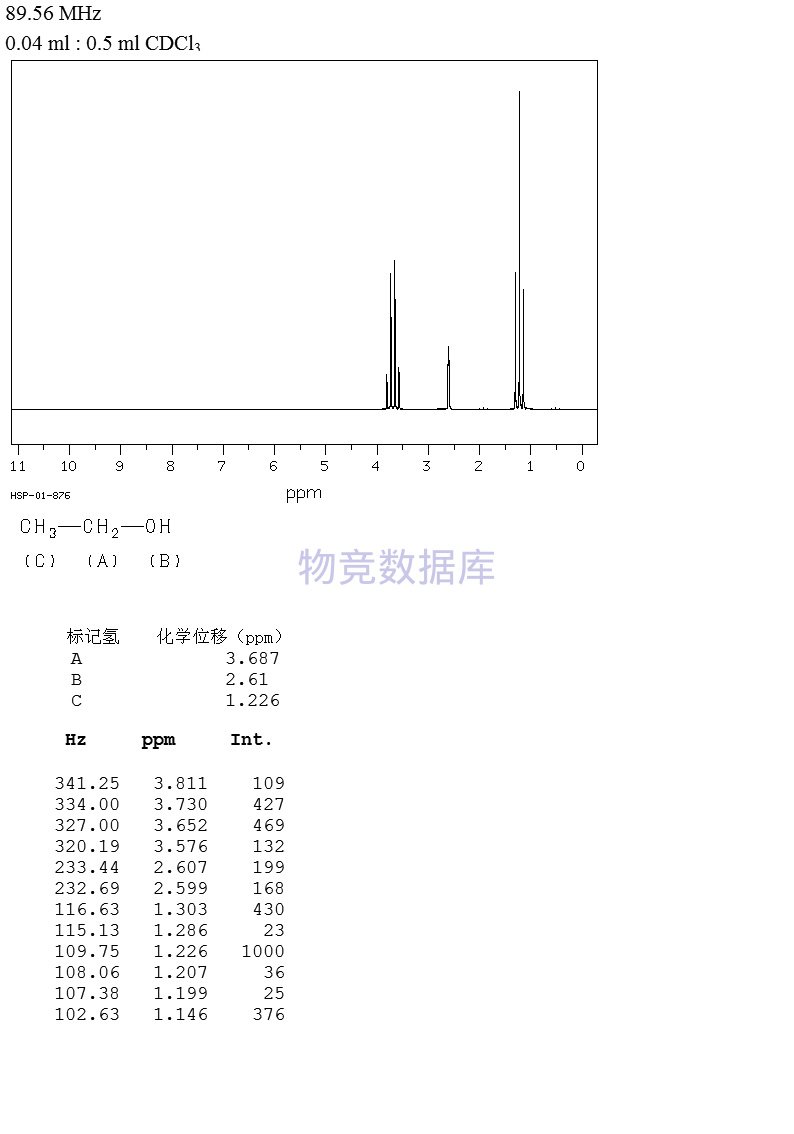
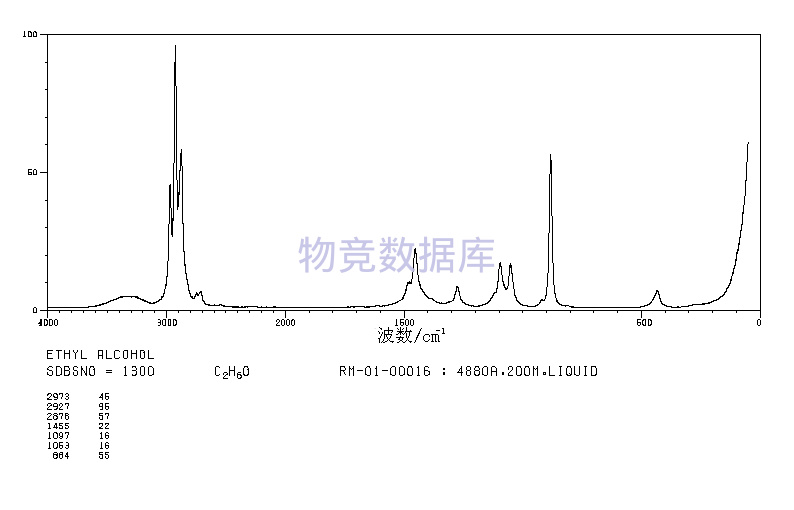
表征圖譜
統計數據
共收錄化學品數據
147579 條





 滬公網安備 31010602001115號
滬公網安備 31010602001115號